昨日,康方生物宣布获得 CDE 同意提交其 PD-1/CTLA-4 双抗 AK104 的新药上市申请并获得优先审评资格。这是国产首款报产的双抗产品,AK104 走向上市之路,意味着这一赛道竞逐的发令枪已经打响。
双特异性抗体(BsAb,Bispecific Antibodies)通过同时识别并结合两种不同抗原,以期实现 1+1>2 的疗效及更优的安全性。近年来,国内双抗项目申报数量激增,从 2015 年至 2021 年每年新申报项目数都稳定增长。2021 年更是厉害,才到 8 月,新申报的双抗项目数已近 2020 年全年申报量的两倍。
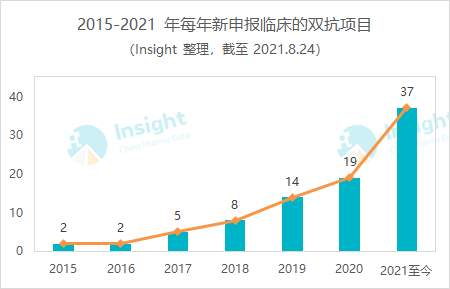
而就国产项目而言,目前累计已经有 67 款双抗已经进入临床阶段。
集火 PD-1/PD-L1,
企业竞相研发「二代 PD-1」?
PD-1 单抗赛道内卷严重,无论是为了追逐昔日 PD-1 先发者的辉煌,还是另辟蹊径试图避开已经过热的单抗赛道,企业已经把目光投向其他生物药,双抗也是其中炙手可热的一个方向。不过,尽管全球范围内尚未有同类产品上市,过多企业的入局似乎使 PD-1/L1 相关双抗也「卷」了起来。
根据 Insight 数据库,在国产 67 个临床阶段双抗项目中,有 35 款产品的靶点之一都是 PD-1/L1,其次是双抗经典靶点 CD3,共有 15 个项目。值得一提的是,全球范围内的 PD-1/L1 相关双抗共 77 款,国内项目又占到了近半数。
根据 Insight 数据库,除了已经递交新药上市申请的康方生物之外,国内另有两款双抗紧追其后,早在 2020 年就已经进入到 III 期临床,分别是信达生物的 PD-1/PD-L1 双抗 IBI318 以及康宁杰瑞的 PD-L1/CTLA-4 双抗 KN046。想了解国内双抗研发详情?戳这里可以查询
已启动临床的国产双抗
(截至 2021.8.24,不包括融合蛋白)
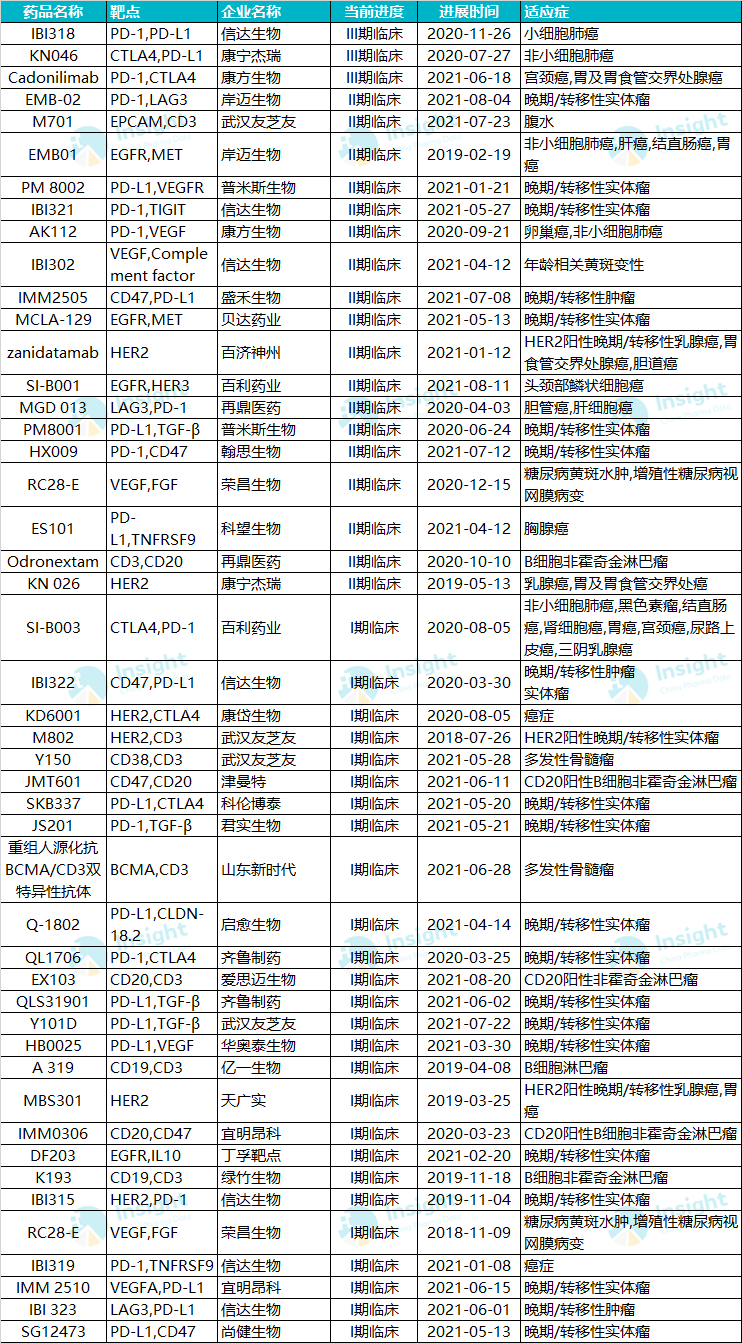
信达的 IBI318 是一款重组全人源 IgG1 双特异性抗体,靶向 PD-1/L1,旨在通过阻断 PD-1 与 PD-L1/PD-L2 信号通路,及阻断 PD-L1 结合 CD80 信号通路,恢复 T 细胞激活及抗肿瘤功能。该药于 2019 年启动首项临床,目前进展最快的是 2020 年 11 月启动的一项 Ib/III 期临床,评估 IBI318 联合紫杉醇用于经标准一线及以上化疗失败的小细胞肺癌患者。
康宁杰瑞的 KN046 采用机制不同的 CTLA-4 与 PD-L1 单域抗体融合组成,可靶向富集于 PD-L1 高表达的肿瘤微环境及清除抑制肿瘤免疫的 Treg。康宁杰瑞与康方生物被认为是国内双抗赛道「双子星」,KN046(PD-L1/CTLA-4)和 AK104(PD-1/CTLA-4)也是进度相近,目前来看是康方快了一步。
根据 Insight 数据库,目前 KN046 在国内启动了 12 项临床,其中包括一项 2/3 期临床和一项 3 期临床,均针对 NSCLC。此外,KN046 在澳大利亚、中国及美国已开展覆盖非小细胞肺癌、三阴乳腺癌、食管鳞癌、胸腺癌、肝癌、胰腺癌等 10 余种肿瘤的不同阶段临床试验。
PD-1/L1 的搭档们:
最热的是谁?
据 Insight 统计,国产 PD-(L)1 双抗的搭档靶点既不是经典联用靶点 CTLA-4,也不是近期备受热捧的 CD47,而是 TGFβ。
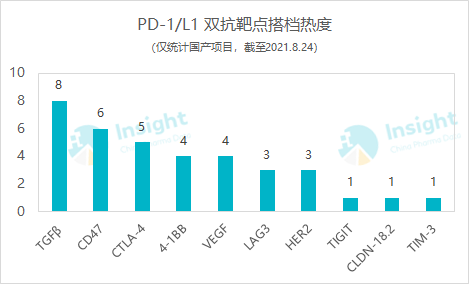
包括双靶点融合蛋白在内,目前国内有 8 款 PD-(L)1/TGFβ 双抗或双靶点融合蛋白在研。进展最快的是恒瑞,SHR-1701 针对非小细胞肺癌、小细胞肺癌、结直肠癌、头颈部鳞状细胞癌、胰腺癌、鼻咽癌等多个癌种都开展了临床研究,其中结直肠癌进展最快,已启动了一项 II/III 期临床。这款产品亦是恒瑞成功出海的产品之一,其韩国权益已以 1.29 亿美元授权给东亚公司。
普米斯生物的 PM8001 仅次于恒瑞,已经启动针对晚期实体瘤的 I/IIa 期临床。君实的 JS201、友芝友的 Y101D、齐鲁的 QLS31901 这三款产品也已经进入 I 期临床。
PD-(L)1/TGFβ 研发火热很大程度上来自于默克的 M7824。在 2018 ASCO 上,M7824 用于 NSCLC 的临床试验(NCT02517398)数据惊艳亮相。该研究入组 80 例未曾使用过 PD-1 抑制剂的晚期 NSCLC 患者。
结果显示,在 1200 mg 剂量组的 40 例患者中,M7824 二线治疗晚期 NSCLC,总人群 ORR 为 27.5%,PD-L1 阳性(≥1%)患者的 ORR 达到了 40.7%(11/27),PD-L1 高表达(≥80%)患者的 ORR 更是高达 71.4%(5/7),比一般 PD-1 疗效数据翻倍。2019 年 2 月,葛兰素史克以总额 37 亿英镑与默克集团签署合作协议,授权引入 M7824 双功能融合蛋白免疫疗法。
2020 年 ESMO 大会上公布了该研究的三年随访结果,数据仍然优异,1200 mg 剂量组在 12、24 和 36 个月的 OS 率分别为 66.2%,39.7% 和 23.2%。PD-L1 阳性(≥1%)患者的中位 OS 为 21.7 个月,PD-L1 高表达患者(≥80%)仍尚未达到中位 OS。PD-L1 阳性患者的 36 个月 OS 率为 33.6%,PD-L1 高表达患者为 66.7%。与目前的 PD-1 单抗的 3 年 OS 率相比,特别是在 PDL1 高表达人群,均有显著提升。
然而,这款明星药目前境况看起来似乎不太积极。今日,默克宣布了 M7824 一线治疗胆管癌 II 期临床的失败,终止了该项探索。这已经是 M7824 第 3 项失败的临床了。
M7824 首项失败的临床来自于与 K 药头对头 PK 的 3 期临床。基于 M7824 在肺癌二线优效数据,M7824 继续探索了与 K 药头对头比较一线治疗 PD-L1 高表达(TPS≥50%)人群的三期临床(NCT03631706)数据。然而在 2021 年 1 月 20 日,默克宣布 INTR@PIDLung 037 研究疗效未达预期,与 K 药的头对头翻车了。
3 月 16 日,德国默克宣布 M7824 又一项临床失败,未能达到预设的主要终点。这是一项二线治疗胆管癌(BTC)的 II 期临床。
今日,默克又宣布一线治疗胆管癌 II 期临床的失败。连续多项临床的失败已经给这一曾被认为希望无限的重磅药蒙上了阴影。
目前,M7824 仍在探索一线和二线宫颈癌、进展型 NSCLC、三阴乳腺癌适应症。希望这款重磅药后续进展顺利,也期待国产同类产品的未来数据能为这个领域带来新的曙光。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..