1月13日,美国强生公司(Johnson & Johnson)表示,其开发的试验性新冠疫苗(Ad26.cov2-s)在早期安全性试验研究中已显示出持久的免疫反应,在单剂接种后至少能诱发71天的免疫反应,这可能意味着一剂疫苗就足以预防新冠病毒。
据彭博社14日报道,该试验中期结果已于周三(1月13日)发表在《新英格兰医学杂志》(NEJM)上,共有805位18岁及以上的人群参与了1-2a期试验。

Jerald Sadoff et al. Interim Results of a Phase 1-2a Trial of Ad26.COV2.S Covid-19 Vaccine. N Engl J Med,January 13,2021.DOI: 10.1056/NEJMoa2034201
文章称,超过90%的参与者在接种此次强生新冠疫苗29天内产生中和抗体免疫蛋白,所有参与者在57天内形成了抗体,且参与者的免疫反应持续了71天。该研究还发现,在两个月后注射第二剂强生疫苗,中和抗体增加了三倍。
此次候选疫苗Ad26.cov2-s是一种腺病毒载体疫苗,在非人灵长类动物模型中,Ad26.cov2-s可诱导强烈的中和抗体反应,预防鼻内和气管内途径SARS-CoV-2感染。
由于强生疫苗有可能成为第一种仅需一剂就有成效的冠病疫苗,从而使大规模疫苗接种活动变得更加简易,顶级传染病专家一直密切关注其疫苗的进展。
本次研究招募年龄分别在18-55岁(队列1)和65岁以上(队列3)的志愿者,分别接受5×1010个病毒粒子(低剂量)、1×1011个病毒粒子(高剂量)疫苗和安慰剂,按计划志愿者接受1或2次疫苗接种,在队列2中收集单剂量方案和两剂量方案的长期比较数据,这些结果不在此报告中。研究的主要终点是安全性和免疫原性。
805名志愿者接种了疫苗,接种后最常见的不良事件为疲劳、头痛、肌痛和注射部位疼痛。最常见的系统性不良事件为发热。65岁以上志愿者的系统性不良事件率低于中青年志愿者,低剂量组的不良事件率低于高剂量组。在首次疫苗接种后第29天,90%的志愿者体内可检测到野生型病毒中和抗体,滴度为224-354,在57天后中和抗体阳性率达到100%,滴度上升至288-488,直至接种后71天,抗体滴度仍较为稳定。二次接种可提高抗体滴度,滴度范围上升至827-1266。尖峰结合抗体反应类似于中和抗体反应,在接种后14天,队列1中,志愿者CD4+T细胞反应率为76-83%,队列3为60-67%,中青年志愿者的尖峰结合抗体反应较老年志愿者强烈,且更为稳定。
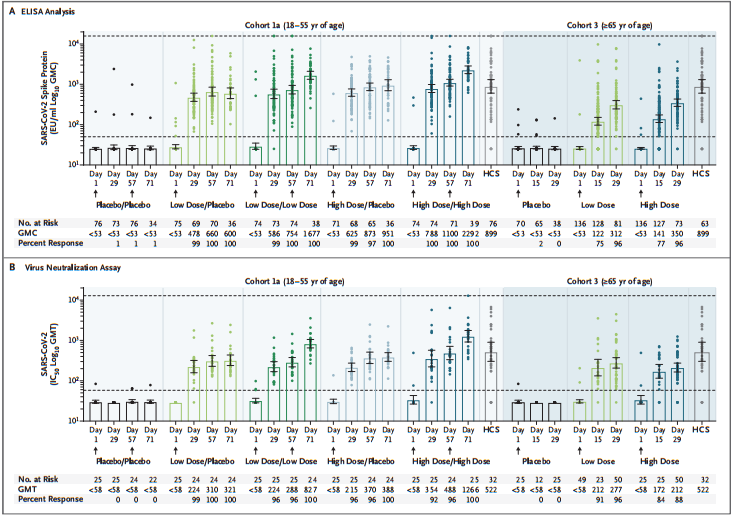
Ad26.COV2.S免疫原性
研究认为,Ad26.COV2.S表现出良好的安全性及免疫原性,其新冠肺炎预防效果需进一步的验证。
“从这些抗体产生情况来看,在公司的末期临床试验中,疫苗奏效应该很有希望、很有理由的,”强生首席科学官Paul Stoffels此前周二在接受采访时说。相比其他两剂型新冠疫苗,强生的单剂型疫苗产生的中和抗体更高。但是,这些竞争对手的两剂接种得到的反应数据与强生单剂疫苗处于相同区间。
目前,强生公司仍在评估单剂疫苗所提供的免疫效果将持续多长时间,以及是否需要更高的抗体水平才能对抗变种病毒。
此前英国政府官员表示,强生的单剂疫苗最快在2月获批,有望成为英国第4款获批的新冠疫苗。英国政府目前已订购3000万剂强生疫苗,也可随时额外加购2200万剂。英国政府官员相信强生疫苗一旦获批,有助政府于2月中旬为4类高危群体优先接种疫苗。
该公司希望在下个月初从最终阶段的研究中获得确切的成效数据,并可能在今年三月份获得监管机构批准使用。
强生公司的新冠疫苗为摆脱最严重的新冠流行带来了巨大的希望。该疫苗以单剂形式交付,没有辉瑞和摩德纳公司的疫苗的极端温度储存要求,如果证明有效,它可以加快全球接种速度。
但周三,《纽约时报》报道称,该公司在疫苗制造方面正面临延误,使其落后于最初的生产计划两个月。该报道是在人们对强生公司的疫苗3期试验数据越来越期待的情况下发布的,预计该数据将在未来几周内公布。
联邦官员被告知,该公司落后于原定的生产计划,要到4月底才能赶上。根据强生公司与 "战速行动 "最初签订的10亿美元合同,该公司应在2月底前提供1200万剂疫苗,6月底前提供1亿剂。该公司预计到今年年底将实现交付10亿剂疫苗的目标。但根据周三《纽约时报》的报道,该公司正在落后于其向联邦政府 "战速行动 "做出的生产承诺。
根据8月份宣布的那份协议条款,该公司同意以10亿美元的价格向美国政府交付1亿剂疫苗。该公司当时没有透露具体的生产时间表目标,但《纽约时报》周三报道称,该公司的目的是在2月底前准备好1200万剂疫苗。
《泰晤士报》称,现在生产计划推迟了两个月。一位接受《泰晤士报》采访的强生公司官员没有就生产问题发表评论,但一位 "战速行动 "的官员向该报证实了延迟生产的消息。泰晤士报》报道称,该公司现在有望在4月底前赶上原定的生产计划。届时,该公司原计划交付超过6000万剂。
"现在谈论我们候选疫苗供应的具体细节还为时过早,因为我们还没有3期数据,也没有申请或获得紧急使用授权,"该公司在周三向巴伦的一份声明中表示。"我们仍在与监管机构进行积极的讨论,包括对我们制造工艺的批准和验证。" 该公司表示,生产已经开始,它有信心能够实现对各国政府的承诺,并预计 "在实现其中一些步骤后 "将提供更多细节。"
强生公司的股价在早盘交易中下跌0.5%。该股在过去12个月中上涨了7%。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..