6月29日,FDA批准罗氏开发的抗体鸡尾酒疗法Phesgo(帕妥珠单抗/曲妥珠单抗/hyaluronidase–zzxf)上市,皮下注射给药,用于治疗成人HER2+转移性乳腺癌以及早期HER2+乳腺癌。此批准日期比预定的10月18日期限提前了近4个月。
Phesgo采用了Halozyme Therapeutics公司基于重组人透明质酸酶PH20 (rHuPH20)开发的Enhanze药物递送技术,将固定剂量的帕妥珠单抗、曲妥珠单抗和hyaluronidase复方组合在一起实现皮下注射给药。rHuPH20可以降低体内透明质酸的活性,以帮助皮下注射药物的渗透和吸收。给药时间方面,Phesgo首次皮下注射达到负荷剂量需要8分钟,此后皮下注射达到维持剂量每次只需5分钟。相比之下,按照Perjeta和Herceptin各自的标准静脉注射方式,完成负荷剂量给药需要150分钟,维持剂量给药则需要60~150分钟。相当于给药时间可以从2~5小时缩短至5分钟。
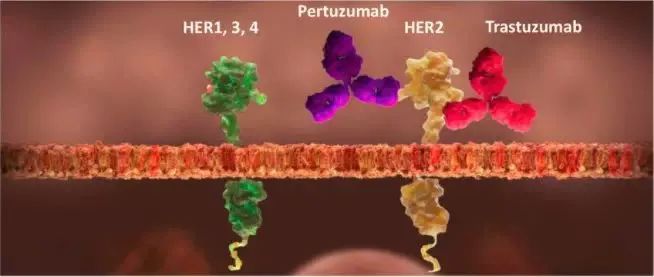
曲妥珠单抗和帕妥珠单抗均是由罗氏开发的anti-HER2单抗药物,但是二者与Her2蛋白的结合位点不同。帕妥珠单抗是跟Her2蛋白的CR1区域结合,可以阻止Her2与其他Her受体形成异源二聚体,阻断Her2信号通路。帕妥珠单抗+曲妥珠单抗联合使用则可以充分阻断Her2信号通路,起到协同增效的作用。
静脉注射Perjeta+Herceptin+化疗药物这种方案当前已经在全球超过100个国家获批,用于治疗早期或转移性乳腺癌患者。对于早期乳腺癌患者,静脉注射Perjeta+Herceptin+化疗作为新辅助治疗方案相比静脉注射Herceptin+化疗可以使pCR几乎翻倍(42% vs 23%)。而作为辅助治疗方案,也可以显著降低患者的疾病复发或死亡风险(APHINITY研究,HR=0.82, 95% CI 0.67-1.00, p=0.047)。
罗氏此次推出的抗体鸡尾酒疗法Phesgo也进一步提高了患者治疗的依从性。Phesgo初次使用是在医院与化疗联用。待化疗疗程结束之后,可以在家里由符合资质的医疗护理人员进行给药。罗氏此前在评论中指出:对于同样的药物,相比静脉注射给药的途径,大多数患者都倾向于选择皮下注射剂,他们给出的最常见理由就是可以节省在诊所的时间。
一项涉及500例正在接受新辅助治疗和辅助治疗的HER2+早期乳腺癌患者的随机、开放标签、III期FeDeriCa研究结果显示,与标准静脉注射 Perjeta相比,按照设定的周期间隔皮下注射该固定剂量复方,患者体内的Perjeta血药浓度达到非劣水平,到达了研究的主要终点。研究同时到达了Herceptin血药浓度非劣和病理学完全应答率(pCR)可比的次要终点。安全性方面,皮下注射固定剂量复方联合静脉注射化疗药物与分别静脉注射Perjeta、Herceptin和化疗药物的安全性一致,未发现新的安全性事件。
Phesgo最常见的不良反应包括脱发、恶心、腹泻、贫血和乏力,也可能导致化疗引起的中性粒细胞减少恶化。Phesgo的标签中含有一个黑框警告,警示医疗保健人员和患者Phesgo潜在的心力衰竭、胎儿伤害和肺毒性风险。 医疗保健人员使用Phesgo时应监测与静脉注射帕妥珠单抗和曲妥珠单抗相同的参数。
HER2+乳腺癌是罗氏的传统优势业务,Hercepin、Perjeta、Kadcyla三款药物的合计收入占到罗氏整个制药业务的20%以上。为了延长Hercepin的生命周期,罗氏开发的皮下注射型的Herceptin Hylecta(曲妥珠单抗、透明质酸酶)已经在2019年2月获得FDA批准,但是阻止不了来自安进、Bicon/Mylan的Herceptin生物类似药在欧洲、美国陆续获批上市销售,2019年Herceptin的全球收入出现双位数跌幅,但可喜的是,Perjeta、Kadcyla都已成长为中坚力量,覆盖患者全程用药管理,确保罗氏HER2+乳腺癌业务整体平稳。
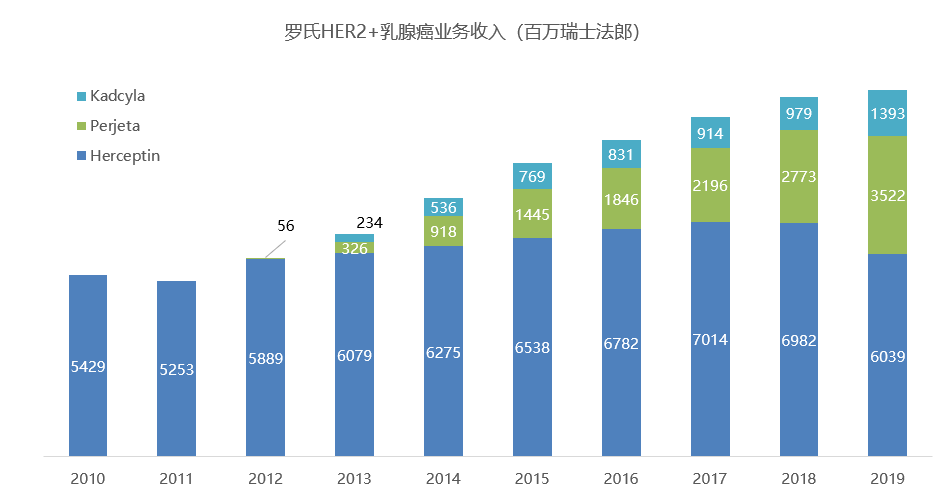
来源:公司财报、医药魔方
毫无疑问,Herceptin在2020年面临的生物类似药的市场竞争会更加激烈。但是Perjeta+Herceptin+化疗组合构建的临床疗效门槛一时间还是会让很多对手难以企及。而Perjeta/Herceptin二合一皮下注射剂的推出可以进一步帮助罗氏抵御仿制药厂家的竞争,提高对患者的黏性。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..