Alexion是一家致力于罕见病新药研发的生物制药公司。近日,该公司宣布,欧盟委员会(EC)已批准Ultomiris(ravulizumab)一个新的适应症,用于治疗非典型溶血性尿毒综合征(aHUS)患者的治疗,具体为:先前没有接受过补体抑制剂治疗(初治)或已接受Soliris(eculizumab)治疗至少3个月且有证据表明对Soliris治疗有反应、体重≥10公斤的aHUS)儿童和成人患者。
用药方面,在负荷剂量(loading dose)后2周开始,Ultomiris维持剂量可每8周或每4周(取决于体重)静脉输注一次。之前,Ultomiris已被批准用于治疗阵发性夜间血红蛋白尿(PNH)成人患者。
值得一提的是,Ultomiris是第一个也是唯一一个被批准用于治疗aHUS的长效C5抑制剂,该药可每月或每2个月(取决于体重)给药一次,可减轻aHUS儿童和成人的治疗负担,有潜力成为欧洲aHUS临床治疗的新护理标准。在美国,Ultomiris已于2019年10月获得
FDA批准,用于治疗aHUS成人和儿科(≥1个月)患者,以抑制补体介导的血栓性微血管病(TMA)。目前,Ultomiris治疗aHUS的新适应症申请正在接受日本监管机构的审查。
Ultomiris是获得监管批准的第一个也是唯一一个长效C5补体抑制剂。在美国和日本,Ultomiris之前已被批准用于治疗阵发性夜间血红蛋白尿(PNH)成人患者;在欧盟,Ultomiris已被批准用于治疗有临床症状表明疾病活动度高、对Soliris治疗至少6个月后处于临床稳定的PNH成人患者。
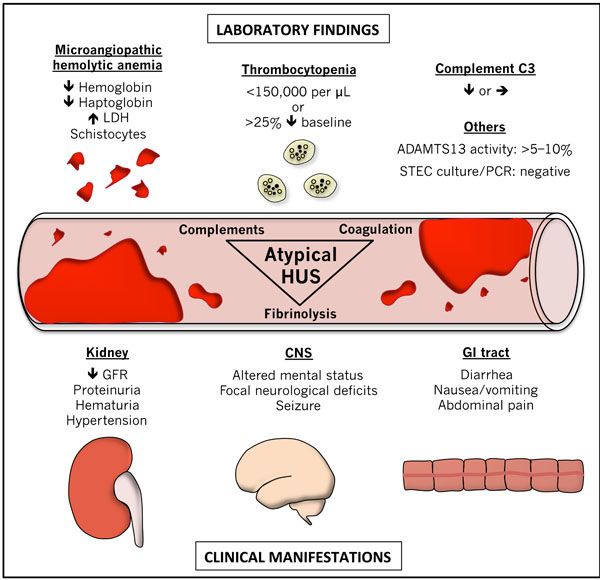
aHUS是一种极为罕见的疾病,可通过对血管壁的损伤以及血栓对重要器官(主要是肾脏)造成渐进性损害。aHUS影响成人和儿童,许多患者在医院病危,通常需要在重症监护病房接受支持性护理,包括透析。aHUS可导致器官突然衰竭或随时间缓慢丧失功能,可能导致需要移植,在某些情况下甚至死亡。aHUS的预后很差,56%的成人和29%的儿童在确诊一年内发展为终末期肾病或死亡。因此,除了治疗外,及时准确的
诊断对改善患者预后至关重要。
德国汉诺威大学肾病诊所Hermann Haller教授表示:“aHUS的后果是非常严重的,并可能危及生命,给患者及其家属带来重大挑战和不确定性。aHUS治疗的目标是通过抑制不受控制的C5补体激活(人体免疫系统的一部分)来防止机体攻击自身。临床研究结果显示,在Ultomiris第一次给药后,成人和儿童aHUS患者获得了立即、完全的C5抑制,持续长达8周。Ultomiris除了对aHUS患者具有临床意义的益处之外,还提供了更大的自由度,每年的输液次数显著减少。”
Alexion执行副总裁兼研发主管John Orloff医学博士表示:“在Alexion,我们的目标是继续改善受aHUS和其他严重罕见病影响的患者及其家庭的生活。Ultomiris治疗提供了方便的8周剂量,我们认为这是患者的首选,因为它可为患者提供更大的灵活性和更高的生活质量,同时也减轻了许多国家目前面临巨大压力的医疗系统的负担。今天的欧盟批准标志着我们在努力将Ultomiris确立为aHUS患者群体新护理标准方面迈出了重要的一步。”
aHUS(图片来源:benthamopen.com)
此次aHUS新适应症批准,基于2项全球性、单臂、开放标签研究(一项针对成人aHUS、另一项针对儿童aHUS)的数据。目前,2项研究正在进行中。21例补体抑制剂初治儿童中有18例、58例补体抑制剂初治成人中有56例被纳入中期分析。完全TMA缓解的疗效评估采用血液学正常化参数(血小板计数和乳酸脱氢酶[LDH])和改善肾功能(通过血清肌酐较基线水平提高≥25%来衡量)来评价。
结果显示,在最初26周治疗期间,54%的成人、77.8%的儿童(中期数据)表现出完全的TMA缓解。Ultomiris治疗在84%成人和94%儿童中使血小板计数正常化、在77%成人和90%儿童使LDH(溶血标志物)正常化、在59%成人和83%儿童(中期数据)中使肾功能改善(对于入组时接受透析的患者,基线是在其脱离透析后确定的)。
在52周的随访期内,另有4例成人患者和3例儿童患者在26周的初始评估期后证实了完全TMA缓解,导致成人和儿童的总体完全TMA缓解分别为61%和94%(中期数据)、在86%成人和94%儿童中LDH(溶血标志物)正常化、在63%成人和94%儿童(中期数据)肾功能改善(对于入组时接受透析的患者,基线是在其脱离透析后确定的)。
儿科研究中还纳入了第二个队列,共有10例先前接受过Soliris治疗的儿科患者;该队列显示,由Soliris转向Ultomiris治疗可以维持疾病控制、血液学和肾脏参数稳定,对安全性没有明显影响。
这些研究中,最常见的
不良反应是上呼吸道感染、腹泻、恶心、呕吐、头痛、
高血压和发热。在接受Ultomiris治疗的患者中发生了严重的脑膜炎球菌感染。为了最大限度地降低患者的风险,为Ultomiris制定了具体的风险缓解计划,包括风险管理计划(RMP)。
Ultomiris是一种长效C5补体抑制剂,能抑制人体免疫系统补体级联反应中的C5蛋白。该药被定位为Alexion公司重磅药物Soliris(每2周一次静脉输注)的升级版,后者于2007年首次获准上市,已获批治疗4种超级罕见病,分别为:PNH、非典型溶血性尿毒综合征(aHUS)、抗乙酰胆碱受体抗体阳性全身型重症肌无力(gMG)、抗AQP4抗体阳性视神经脊髓炎谱系障碍(NMOSD)。
目前,Alexion严重依赖Soliris,该公司超过80%的销售额来自该产品。Soliris是全球最昂贵的药品之一,定价高达50万美元/年,自上市以来,Soliris已累积为Alexion公司带来了超过150亿美元的销售额,该药也是全球最畅销的孤儿药之一,2019年的全球销售额达到了39.46亿美元。业界预测,2019年8月批准的NMOSD适应症将为Soliris新增约7亿美元的销售额。
除了不断扩大Soliris适应症之外,Alexion公司也正在开发升级版产品Ultomiris,该药在美国、日本、欧美已被批准治疗PNH适应症,在美国和欧盟已被批准治疗aHUS。
Ultomiris是第一种也是唯一一种可8周给药一次的长效C5补体抑制剂,在治疗PNH的III期临床研究中,Ultomiris每2个月(8周)输注一次与Soliris每2周输注一次在全部11个终点方面均达到了非劣效性。
业界预测,基于强劲的临床数据和差异化特征,Ultomiris将成为PNH和aHUS临床治疗的新标准。医药市场调研机构EvaluatePharma此前预测,Ultomiris在2024年的销售额将达到34.3亿美元。目前,Alexion公司正在积极推动Ultomiris的市场渗透,同时也正在积极开发Ultomiris的其他适应症(包括gMG)以及开发皮下注射(SC)剂型Ultomiris。
就在最近,SC剂型(每周一次)的III期临床研究获得了成功,这款新剂型产品通过皮下注射给药,耗时约10分钟,而Ultomiris静脉制剂(IV)每次给药时间在1.3-3.8小时(剂量根据体重调整)。
目前,Alexion公司也正在评估Ultomiris和Soliris治疗新型冠状病毒肺炎(COVID-19)患者中过度激活的炎症反应。(生物谷Bioon.com)