编译丨newborn
在本月初宣布对新冠肺炎(COVID-19)抗体检测产品加强监管之后,美国FDA从上周四已经开始公布被列入删除名单的商业制造商,这些制造商要么没有提交紧急使用授权(EUA)申请,要么自愿撤回根据该机构之前的政策在分发抗体检测产品前所发送给FDA的通知。
相关阅读:FDA对COVID-19抗体检测产品“动刀”,数据不达标面临退市风险!
在3月发布的最初政策中,FDA表示,只要抗体产品得到验证,且在销售之前已经向该机构发送通知,在没有FDA审查或授权的情况下,不反对实验室或商业制造商开发和使用这些抗体检测产品。
由于陆续有报告对市场上部分抗体检测产品准确性提出质疑,FDA在5月初修订了政策,要求商业制造商在新政策出台或从制造商向该机构发送通知之日起10个工作日内提交EUA申请。
现在,FDA更新了SARS-CoV-2检测的常见问题网页,其中包括一份“删除名单”。
FDA局长Stephen Hahn表示:“这项行动是FDA采取的一个重要步骤,以确保美国人民获得值得信赖的抗体检测产品。我们已经看到了希望正确实现这一点的开发人员的高度协作和参与,我们将继续与业界广泛合作,帮助他们开发准确的检测产品。”
目前,这份“删除名单”中共包括了20多家主要位于美国或中国的公司所开发的29款检测产品,这些公司已从该机构的通知名单中被移除。这29款检测产品通知中,有11款已被商业制造商自愿撤回(标注为*)。
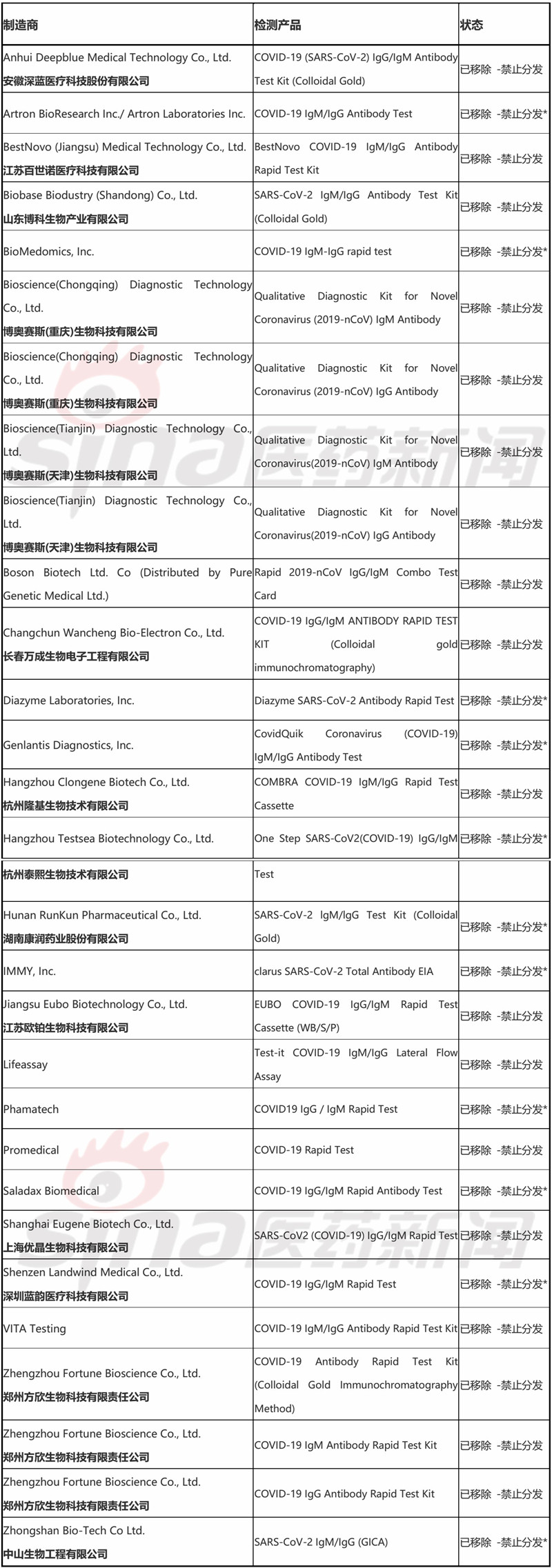
注:截至2020年5月22日。
FDA表示,被列入“删除名单”中的检测产品将不能够再被分发,除非“并且直到”被授予EUA。这意味着,这份“删除名单”中的这些抗体检测产品将不能够基于通知进行分发。
目前,尚不清楚美国到底有多少抗体检测产品在销售,但相关信息称可能多达数百种。其中,仅有十余种产品获得了FDA授予EUA。
FDA还表示,这仅仅是一个开始,该机构将会对这份“删除名单”持续更新。目前已被列入“删除名单”的这些检测产品,均没有获得EUA。有意思的是,在过去两周里,FDA没有对任何新的抗体检测产品授予EUA。
参考来源:
1、FDA names companies removed from antibody test list
2、FAQs on Testing for SARS-CoV-2
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..