文 | 白话文
根据EvaluatePharma报道,2019年FDA共通过加速批准的方式批准14个新药申请(包括首次申请和补充申请),少于2018年的18个。
加速批准这一监管方式允许FDA通过替代终点(surrogate endpoint)或者中间终点(intermediateclinical endpoint)来加速重大疾病药物的批准,而不只是直接衡量临床益处。根据FDA发布的数据,通过加速批准的药物主要以抗癌药为主,尤其是最近今年。例如,Keytruda目前为止已经通过替代终点的方式获得了14项批准,其中有4项已经转换为完全批准。
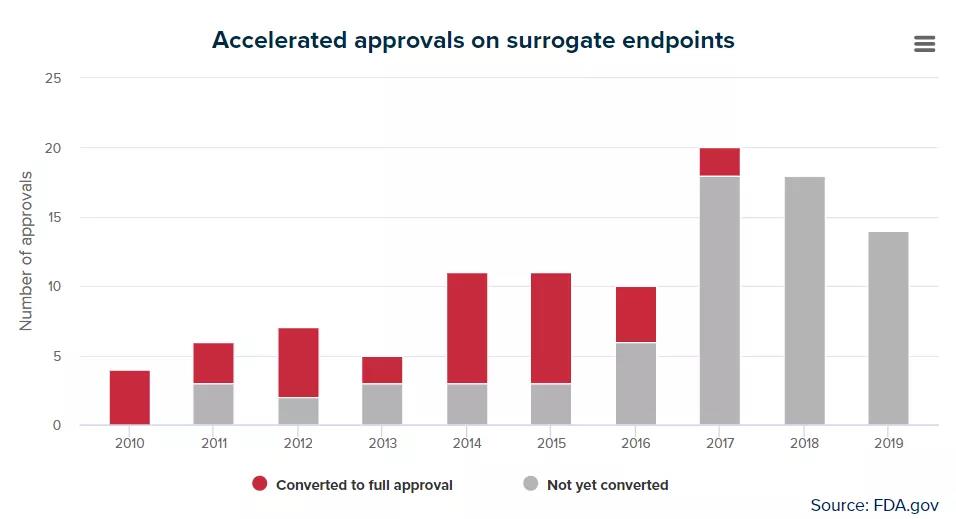
当然,从上图也可以看出,很少有最近批准的新药就能够转换为完全批准,但真正令人担忧的是,部分上市多年的药物,仍然未能转换成完全批准,这意味这些药物依然缺乏足够的数据支持。
2019/10/29,FDA专家组以9:7的票数支持一款治疗早产的药物Makena撤市,该药于2011年2月获得FDA的加速批准,但上市后的两项III期研究均已失败告终。2019年4月,礼来的晚期软组织肉瘤新药Lartruvo因上市后的大型III期研究数据不佳选择了全球撤市。
同样值得注意的是,Keytruda去年分别在肝癌和胃癌的临床试验中宣布失败,但FDA对于是否取消这两个适应症的加速批准还尚未表态。
对于将加速批准转换为完全批准的时间,EvaluatePharma也做了统计。如下图最上角的是GSK的乳腺癌药物Tykerb,GSK花了8年多时间才将该药在2010年获得的加速批准新适应症转换为完全批准。
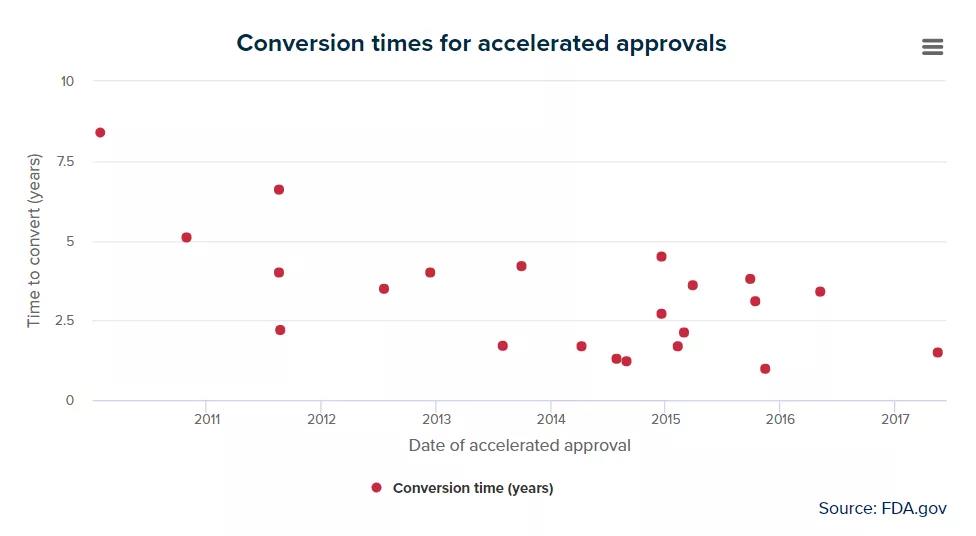
来源:
EvaluatePharma.FDA keeps the faith in surrogate endpoints
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..