蓝鸟生物(bluebird)是一家行业领先的基因治疗公司。近日,该公司宣布,在德国推出Zynteglo(LentiGlobin,含βA-T87Q珠蛋白编码基因的自体CD34+细胞),这是一种一次性的基因疗法,用于适合造血干细胞(HSC)移植但没有人类白细胞抗原(HLA)匹配的HSC供体、年龄在12岁以上、非β0/β0基因型输血依赖性β地中海贫血(TDT)患者的治疗。
在欧盟,Zynteglo于2019年5月获得有条件批准,成为全球首个治疗TDT的基因疗法。在美国,Zynteglo尚未获得批准,蓝鸟生物已启动向
FDA滚动提交生物制品许可申请(BLA),预计在2020年上半年完成BLA提交。
β地中海贫血(TDT)是一种严重的
遗传病,由β-珠蛋白基因突变引起,导致成人血红蛋白(HbA)显著减少或缺失。为了生存,TDT患者通过终生慢性输血维持血红蛋白水平。由于不可避免的铁超载,这些输血有进行性多器官损害的风险。Zynteglo将改良版本的β珠蛋白基因(βA-T87Q-珠蛋白基因)的功能拷贝添加到患者自身的造血
干细胞(HSC)中,一旦回输体内后,患者就拥有了βA-T87Q-珠蛋白基因,有潜力在体内产生足够水平的HbAT87Q,这是一种
基因治疗来源的血红蛋白,从而消除或显著减少输血需求。

Zynteglo是一种一次性的
基因治疗方法,可解决TDT的内在基因病因,有潜力使患者摆脱输血依赖(输血非依赖),一旦实现这一点,预计将持续终身。
由于在罕见疾病中实施
基因治疗的高度技术性和专业性,蓝鸟生物正与在
干细胞移植和治疗TDT患者方面具有专业知识的机构合作,以创建合格的治疗中心来实施Zynteglo。蓝鸟生物已与海德堡大学医院合作,成为德国首个合格的治疗中心。
此外,蓝鸟生物还与德国的多家法定医疗保险公司签订了基于价值的支付协议,以帮助确保患者及其医疗保健提供者能够获取Zynteglo,并且支付方仅在治疗兑现承诺的情况下支付。蓝鸟生物提出的创新模式限于五次分期付款。首次付款是在Zynteglo输注时支付。只有在患者此后不需要输血治疗TDT的情况下,才支付剩余的四次分期付款,每年一付。
蓝鸟生物首席商务官Alison Finger表示:“对于TDT患者,为了生存,需要终生慢性输血。我们很高兴地宣布,Zynteglo现在将可用于患有这种严重疾病的欧盟患者。除了确认我们的合作伙伴apceth Biopharma GmbH的生产准备就绪外,蓝鸟生物还向德国联邦联合委员会(G-BA)提交了一份用于药品效益评估的档案。我们要感谢我们的合作者承诺通过接受创新的支付模式帮助我们改变医疗体系,我们期待着很快治疗我们的第一位商业患者。”
Zynteglo在欧盟的有条件批准基于多项
临床试验的疗效、安全性、耐受性数据,包括I/II期HGB-205研究、已完成的I/II期Northstar(HGB-204)研究、正在进行的III期Northstar-2(HGB-207)研究和Northstar-3(HGB-212)研究、长期随访研究LTF-303,数据截止日期为2018年12月13日。
在这些
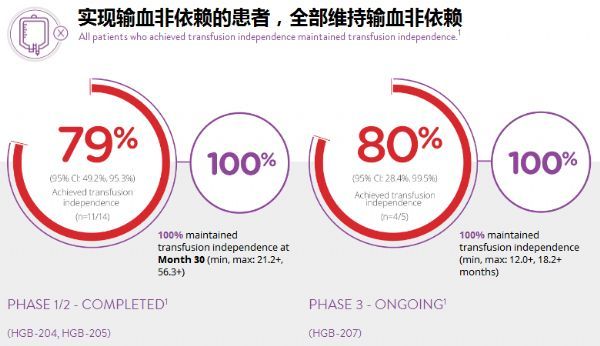
临床试验中,高达75%-80%的患者摆脱了对输血的依赖。在数据截止时,所有已摆脱输血依赖的患者均维持输血非依赖,已有患者近6年(56个月)没有接受输血。和过去频繁的输血相比,是一个重大进步。
安全性方面,临床试验中观察到的Zynteglo治疗引起的非严重不良事件包括:潮红、呼吸困难、腹痛、四肢疼痛和非心脏性胸痛。一例血小板减少症严重不良事件(SAE)被认为可能与Zynteglo有关。
临床试验中观察到的其他
不良反应与已知的HSC收集和白消安骨髓消融的副作用一致,包括静脉闭塞性疾病SAE。在最后随访时临床项目中接受Zynteglo治疗的所有患者仍然存活。
定价方面,Zynteglo在欧洲的价格标签高达157.5万欧元(约合1210万人民币),是继
诺华脊髓性肌萎缩症(SMA)一次性基因疗法Zolgensma之后全球第二贵药物,后者的官宣定价为212.5万美元,约合人民币1460万元。
但2款基因疗法的付款模式略有不同。Zynteglo付款基于
基因治疗的效果,分为5期,可在5年内分摊。Zolgensma付款也是分期5年支付,每年支付42.5万美元,但付款并不取决于治疗的效果。
随着基因疗法的迅速发展,该领域迫切需要新的支付模式,以适应获取这些疗法的高成本。
诺华为Zolgensma提供的年金模式,以及蓝鸟死亡为Zynteglo提供的基于治疗结果的分期支付模式,可能被证明是未来几年
基因治疗开发商唯一可行的解决方案。
再生医学联盟(ARM)去年7月发表的一份报告呼吁欧洲领先国家的医疗报销系统迅速采用新的支付模式,包括有条件报销、按效果支付、基于年金的支付。(生物谷Bioon.com)