英国制药巨头阿斯利康(AstraZeneca)近日在法国巴黎举行的欧洲心脏病学会(ESC)2019年会上公布了口服降糖药Farxiga(中文品牌名:安达唐,通用名:dapagliflozin,达格列净)治疗心力衰竭的里程碑III期DAPA-HF研究的详细结果。该研究显示,在射血分数降低的心力衰竭(HFrEF)患者(有或无2型糖尿病)中,联合标准护理时,Farxiga同时降低了心血管死亡发生率和心力衰竭的恶化。
值得一提的是,DAPA-HF是评估一种SGLT2抑制剂联合标准护理药物(包括血管紧张素转化酶[ACE]抑制剂、血管紧张素II受体阻滞剂[ARB]、β-受体阻滞剂、盐皮质激素受体拮抗剂[MRA]和脑啡肽酶抑制剂)治疗HFrEF成人患者(伴有和不伴有2型
糖尿病)的首个心力衰竭结局研究。
DAPA-HF是一项国际性、多中心、平行组、随机、双盲研究,在射血分数降低(LVEF≤40%)的心衰患者(HFrEF)中开展,包括伴有和不伴有2型
糖尿病的患者。研究评估了每日一次10mg剂量Farxiga与安慰剂,联合标准护理治疗的疗效和安全性。研究的主要终点是心衰恶化事件(住院或等效事件,例如紧急心衰就诊)或心血管(CV)死亡的时间。
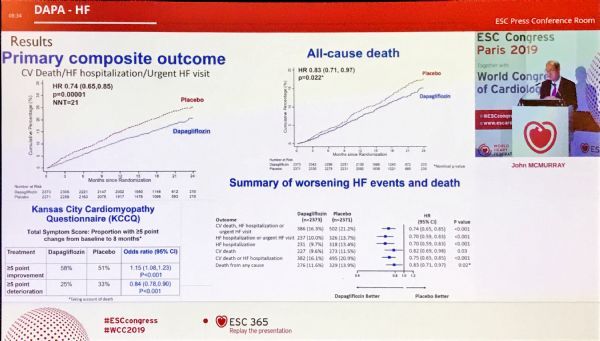
结果显示,该研究达到了主要复合终点:与安慰剂相比,Farxiga将心血管(CV)死亡或心衰恶化复合终点显著减少了26%(p<0.0001),并显示出复合终点的每个单独组分都减少了,具体数据为:发生首次心衰恶化的风险降低了30%(p<0.0001)、死于心血管原因的风险降低了18%(p=0.0294)。Farxiga对主要复合终点的影响在所研究的关键亚组中大体一致。
此外,结果还显示:堪萨斯城心肌病调查问卷(KCCQ)测量的患者报告结果显著改善,全因死亡率名义上显著降低17%(每100患者年发生一次事件的患者为7.9 vs 9.5),数据有利于Farxiga。
该研究中,Farxiga的安全性与该药已确定的安全性一致。容量不足(7.5% vs 6.8%)和肾脏不良事件(6.5% vs 7.2%)的患者比例与安慰剂相当,这是在治疗心力衰竭时通常关注的事件。两个治疗组的重大低血糖事件(0.2% vs 0.2%)都很少见。
目前,阿斯利康也正在开展另外2项临床研究,评估Farxiga治疗射血分数保留心力衰竭(HFpEF)患者(DELIVER研究)、治疗HFrEF和HFpEF患者(DETERMINE研究)的疗效和安全性。
阿斯利康生物制药研发执行副总裁Mene Pangalos表示:“Farxiga在治疗2型
糖尿病方面已经建立了很好的基础。来自DAPA-HF研究令人兴奋的新发现提供了临床上有意义的见解,以了解该药在减轻心衰患者严重疾病负担方面的潜力。基于该研究,Farxiga成为同类产品中第一个在标准护理基础上证明治疗心力衰竭(有或无2型糖尿病)患者疗效和安全性数据的SGLT2抑制剂。当前,一半的心力衰竭患者会在五年内死亡,这仍然是住院治疗的主要原因之一。”
格拉斯哥大学心血管研究中心心血管和医学科学研究所John McMurray医学博士表示:“Farxiga在DAPA-HF研究中的益处非常显著,心血管死亡或住院的主要复合结局显著降低。我们很高兴Farxiga在我们的试验中如此有效,它做了我们希望任何药物治疗心力衰竭的所有事情,包括改善症状、减少住院人数、提高生存率。更妙的是,Farxiga对无糖尿病的心力衰竭患者和有糖尿病的心力衰竭患者同样有效。我们希望这些令人兴奋的新发现最终将有助于减轻由心力衰竭引起的严重疾病负担,并有助于改善患者的预后。”
Farxiga是一种首创、选择性SGLT2抑制剂,主要通过抑制表达于肾脏的SGLT2(是一种转运蛋白,参与肾脏近端肾小管的葡萄糖重吸收作用),减少肾脏对葡萄糖的重吸收,增加尿液中葡萄糖的排泄,从而达到降低血糖水平的效果,并且该降糖效果不依赖于β细胞功能和胰岛素抵抗。
Farxiga拥有一个强大的临床试验项目,包括在超过3.5万例患者中开展的超过35项已完成和正在进行的IIb期/III期
临床试验,以及超过250万患者年的经验。
目前,Farxiga已获批作为一种单药疗法,用于2型糖尿病成人患者改善其血糖控制。此外,Farxiga也已获欧盟和日本批准,作为胰岛素的口服辅助治疗药物,用于接受胰岛素治疗但血糖水平控制不佳并且身体质量指数(BMI)≥27kg/m2(超重或肥胖)T1D成人患者,改善其血糖控制。
在中国,Farxiga于2017年3月获批,用于2型糖尿病成人患者的治疗。此次批准,使Farxiga成为中国上市的首个SGLT2抑制剂,Farxiga为口服片剂,每片含有5mg或10mg达格列净,该药的推荐起始剂量为每次5mg,每日早上服用1次。(生物谷Bioon.com)