尽管目前针对乙肝病毒感染已经有疫苗和抗病毒药物作为预防和治疗手段,然慢性乙肝病毒感染仍是全球范围内主要的公众健康问题。据估计,全球范围内约有2.5亿至3.5亿的慢性乙肝病毒感染者。乙肝病毒的持续感染会导致肝硬化甚至肝癌的发生。目前基于干扰素和/或核苷(酸)类似物为基础的治疗药物临床疗效有限,治愈率相对不理想,因此,寻求新的能够治愈该疾病的药物变得尤为迫切。
目前已有研究证实乙肝病毒进入抑制剂被认为是具有抗病毒效用的能够控制病毒载量和治疗乙肝的一类新型药物。2012年,北京生命科学研究所的李文辉博士发现了乙肝和丁型肝炎病毒进入人体肝细胞所需的受体:肝细胞膜上的钠离子-牛磺胆酸-协同转运蛋白(NTCP)开启了了解病毒进入细胞的分子机制并识别这类进入抑制剂的大门。近期,在肝脏病学杂志(Journal Of Hepatology)中刊登了一篇法国学者关于该类抑制剂的最新研究综述。现肝脏巴士(HeparBus)微信公众号编辑就该份综述内容进行编译以飨读者。
在肝脏中,HBV病毒颗粒结合NTCP——一种在肝细胞基底外膜表达的胆汁酸转运蛋白,触发病毒进入细胞内。HBV包膜的前S1区与转运蛋白的胆汁酸口袋位点相互作用,对应于蛋白质的157至165位氨基酸,进而干扰其转运蛋白功能。
NTCP同时还被作为抗病毒治疗的靶点被详细研究。事实上,跟NTCP相互作用的小分子的确表现出抗病毒活性,包括免疫抑制药物环孢菌素A(CsA)。此外,来自HBV包膜并特异性结合受体的preS1肽已显示在细胞培养物,动物模型和患者中表现出显著的抗病毒活性。
然而,由于HBV和胆汁酸与NTCP共享相同的相互作用位点,所以目前的HBV NTCP进入抑制剂也能够干扰胆汁酸摄取。这可能通过损害肝细胞中Na + - 胆固醇的转运来诱导产生推定的不良反应。实际上,NTCP的缺乏会导致高胆固醇血症,并且在一些用myrcludex B(一种与NTCP结合的preS1肽)治疗的患者中观察到甘氨酸结合的胆汁酸浓度的增加,myrcludex B 目前已在临床试验中进行评估。虽然胆汁酸相关的不良反应似乎有限或不存在,但,不影响NTCP转运蛋白功能的HBV进入抑制剂的发现仍代表着一个概念的进步,其有望助力于解决潜在的安全问题。
在同期的肝脏病学杂志杂志中发表了另一份 Shimura 及其同事对这个问题进行探讨的文章,为了证实CsA衍生物在抑制HBV感染的同时是否对胆汁酸转运的能力是否存在干扰,他们利用了基于过表达NTCP的HepG2细胞系,名叫HepG2-hNTCP-C4 建立了HBV感染模型,这种细胞系使HBV感染成为可能。研究人员合成了十一种CsA衍生物并表征了它们抑制病毒感染的活性。观察到其中五种能够以泛基因型方式抑制HBV感染,他们证实其中四种(命名为SCY806,SCY446,SCY450和SCY995)没有免疫抑制活性,能够在人原代肝细胞(PHH)中抑制HBV感染。为进一步表征这些化合物的抗病毒活性,他们随后测试了它们在病毒感染的不同阶段的抑制作用。通过使用非敏感HBV复制细胞,他们证实CsA衍生物对HBV复制没有影响。为进行对比,研究人员利用特异性结合NTCP荧光标记的preS1肽,结果显示这些药物能够阻止preS1-NTCP相互作用,证实了CsA衍生物能通过干扰病毒与其受体结合的能力抑制HBV进入。
研究人员使用表面等离振子共振分析验证了这些发现,显示CsA衍生物能够与重组NTCP蛋白(如CsA本身)相互作用。由于已知CsA靶向NTCP介导的胆汁酸摄取,作者建立了基于HepG2-hNTCP-C4细胞系的胆汁酸摄取测定以评价CsA衍生物对NTCP转运蛋白功能的推定效应。有趣的是,尽管SCY806和SCY446抑制胆汁酸吸收作用类似于CsA,但是其它两种衍生物SCY450和SCY995对于NTCP介导的胆汁酸转运没有影响,尽管他们HBV抑制作用强,这表明胆汁酸转运蛋白和HBV NTCP的受体功能可以潜在地分开。这一假说进一步由磺基溴菌素(NTCP与蛋白质的胆汁酸口袋位点相互作用的底物)获得证实,它能显示抑制胆汁酸摄取而不影响HBV感染。最后,作者得出结论,因不影响NTCP的胆汁酸转运蛋白功能,开发靶向NTCP的HBV进入抑制剂是可以的。
这些结果对于了解HBV进入以及作为抗病毒药的HBV进入抑制剂的发展具有影响。首先,Shimiura 等人表明介导HBV进入和胆汁酸转运的NTCP结构域可能不完全相同。新鉴定的化合物可以作为进一步阐明HBV细胞进入期间病毒-NTCP相互作用的工具。此外,他们的发现可以推动HBV进入抑制剂的进一步发展:虽然宿主靶向制剂(HTAs)已被证明对HBV,HDV和HCV感染有效,然而,靶标-特异的不良反应仍需要仔细研究处理。
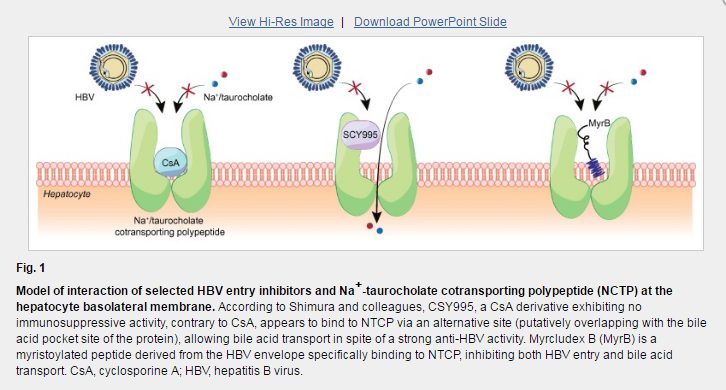
尽管已经提示辅助转运蛋白可以在不存在NTCP的情况下维持肠肝循环,但不能排除胆汁酸转运收受到长期的药理学调节可能导致先前未发现的不良反应。 Shimura 和同事鉴定发现CsA衍生物既不表现出免疫抑制活性也不干扰NTCP介导的胆汁酸转运,至此,上述疑问获得解决。机械地,他们的研究还表明与天然CsA相比,SCY995分子可以靶向NTCP的替代位点(推定与胆汁酸口袋位点重叠),这就可以实现抑制病毒进入而不阻断胆汁酸摄取(图1)的功能。然而,重要的是注意,虽然在研究中使用的浓度范围没有观察到效果,但不能排除SCY995在较高浓度下干扰NTCP胆汁酸转运蛋白功能。此外,研究SCY995是否干扰最近认为的由NTCP胆汁酸转运蛋白功能介导的抗病毒先天免疫应答是有意义的。
总的来说,Shimura 等人通过研究表明:(i)似乎有可能解剖HBV进入和胆汁酸转运蛋白功能;(ii)通过潜在地增加其特异性和减少潜在的不利影响提供优化进入抑制剂的机会。然而,重要的是评估化合物是否还有其它脱靶效应,例如干扰其它转运蛋白(例如肝有机阴离子转运多肽OATP)。仍需要对其在动物模型和HBV感染患者中的功效和安全性进行详细研究,以评估由 Shimura 和同事介绍的方法与进入抑制剂 myrcludex B 和其他HTAs及其他临床许可的HBV抗病毒药。
最后,该文是一篇介绍目前多种作用机制慢乙肝在研新药的一类——乙肝病毒细胞进入抑制剂的类综述文章,此类作用机制的新药目前公布消息最多的是 myrcludex B,已处在 Phase II 期临床。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..