|
上个月Biocentury也对ASCO 2016做了相关分析,结果是类似的:肿瘤免疫相关的靶点占据了半壁江山。如今连FDA肿瘤大佬Richard Pazdur也在ASCO的采访中提出:肿瘤免疫“me-too”药物大爆发。
|
本文转载自“百家汇科技创业社区”(翻译:SCR ZH),原标题“2016看完ASCO你该记住什么?美国知名生物医药VC博主的心底箴言”。
随着2016 ASCO的落幕,肿瘤药物研发人员各回各家。其中很多人可能都在家里做着同一件事,主攻同一个方向——肿瘤免疫疗法。
过去5年里这个领域的迅速扩张有目共睹:临床数据令人振奋、生存曲线有了切实改变、资本不断涌入,对于患者和业界来说好消息不断。
但这也带来肿瘤长期研发战略的问题。过去我们曾多次关注到:2012年美国医药研究与制造商协会(PhRMA)发布了900多个在研肿瘤项目的pipeline,激酶抑制剂扎堆,特别是其中有近70个VEGF抑制剂;2015年,我们对当年ASCO的摘要进行分析后得出,ErB家族(比如EGFR、HER2等)以及肿瘤免疫哨卡成为了香饽饽。上个月Biocentury也对ASCO 2016做了相关分析,结果是类似的:肿瘤免疫相关的靶点占据了半壁江山。如今连FDA肿瘤大佬Richard Pazdur也在ASCO的采访中提出:肿瘤免疫“me-too”药物大爆发。
本文分为两个部分:肿瘤免疫治疗研发的现状;以及对于业界的一些战略思考。
有多少肿瘤免疫产品正在开发?
距首个免疫哨卡抑制剂Yervoy(Ipilumumab,CTLA4抑制剂)获批才五年,现在全球已经有多少个肿瘤免疫产品在研?利用多个数据库进行了分析,结果如下。至少有16个PD1/PDL1项目在临床阶段,包含临床前项目的话则有70个在研的PD1/PDL1,其中有一些已进展到临床II-III期。此外还有二十多个CTLA-4项目正在开发,以及大量“新兴”的免疫哨卡抑制剂项目,包括TIM3、LAG3、OX40等。

单就目前已获批的四个免疫哨卡抑制剂及两个晚期阶段的PDx项目来看(如下图),在ClinicalTrials.gov里就有近1000个相关的试验,其中大部分都在进行中。仅Keytruda一个项目就有包含联用在内的近300个相关临床试验。这还仅仅是已公布的试验,我相信还有一些学术机构发起的试验尚未公布。
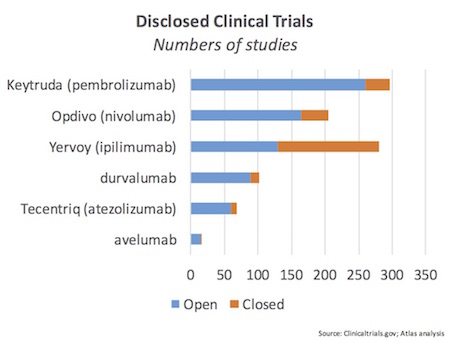
以上图表中不包含“其它”肿瘤免疫项目,比如CART疗法等,有十几个甚至更多的在研项目是针对同一个B细胞标记物CD19,正在开发白血病和淋巴瘤适应症。
基于以上数据,以及FDA Pazdur本人的言论,不难看出,如今业界对于同一肿瘤免疫靶点投入了巨大的(有可能是过剩的)资源和精力。
战略思考
爆发式的肿瘤免疫项目来袭,自然也带来了很多战略问题,我们认为其中最主要的四个是:
(一)、这一大波肿瘤免疫产品面临着巨大的产品差异化的挑战。如今Opdivo已经在市场上击败了Keytruda,主要是因为后者需要在处方前进行PDL1基因检测。但Keytruda开展了大量的临床研究。这两个PD1抗体都属于肿瘤免疫的基础疗法,外加刚刚获批的罗氏的PDL1单抗Tecentriq,那么其他后来者,如duralumab、avelumab等等十多个临床阶段的PDx药物如何才能找到自己的区分优势?大部分临床医生都认为Keytruda和Opdivo具有相似的有效性,给药剂量上有细微差别,各自的临床数据都在说明书上有显示等等。但是否所有的PDx和CTLA4药物,包括它们的各种复方,都具有相似的作用?如果不同,又如何证明?这些PDx抗体在抗原表位、亲和力、Fc功能、糖基化等方面都有差异,这些差异均可影响到药物的作用,但药物作用的差异在临床前工作中很难预见的到。此外,这些细微的差异很可能被疾病的复杂性抹平。我猜需要大量的临床试验和患者才能分出优劣。当产品首次出现了“表现不佳”的信号时,是否会导致项目立即终止?在这样一个高竞争的环境下,研发机构的项目管理机制显得格外重要。
(二)、所有相同免疫靶点的临床试验将面临入组和实施上的激烈竞争。如前文所说,如今有超过1000个免疫哨卡临床相关的临床试验正在开展,意味着有5万~10万肿瘤病人已入组这些试验。肿瘤病人入组一直是挑战,尤其是在肿瘤免疫方面。在顶尖肿瘤中心,病人入组已是面临着巨大的瓶颈,无法想象MSK、Dnan Farber、MD Anderson这些知名肿瘤中心能够同时开展十几个不同的PDx抗体项目。此外,在市场上已有免疫哨卡抑制剂获批的情况下,对于对照组的患者(可能是使用标准疗法组合),医生为什么不给其使用PDx抗体?如今的大部分临床试验已是使用PDx加或不加标准治疗,而非仅仅与传统方法对照,虽然对患者是好事,但无疑也大大增加了后来者的准入门槛。除了入组外,临床试验的实施方面还将遇到如下问题:在RECIST肿瘤大小和负荷终点都无法使用的情况下来定义反应率,需要定义新的免疫反应率,以及这些反应率与总生存期之间的关系。这使得临床试验环境变得尤为挑战:能够开展大规模全球多中心试验,能够聚集众多临床专家和临床机构,将成为肿瘤药厂商的核心竞争优势之一。
(三)、在联合治疗中区分信号和噪声会变得越来越困难。如果一项PDx疗法单药能带来X%的响应率,那么在联用治疗中能再增加10%~15%,对于患者来说是大好事。我在ASCO上看到了大量联用试验的喜人结果,例如CHECKMATE12试验是Yervoy和Opdivo的联用试验,将NSCLC的总反应率从单药的23%提升至了47%;PDL1疗法加MEK抑制剂用于结直肠癌展现了良好的活性;OX40和CD137的联用试验也公布了早期的优良数据,更加安全;此外还有IDO/TDO疗法、STING疗法等等。但是如果超过100种的联用方案在不同的组合中都展现出了反应率的提高呢(例如PDx加上各种肿瘤免疫靶点外加标准化疗)? 那么医生将如何为患者选择合适的联用?制药企业和投资者又该如何分配研发资源?在如今有大量试验开展的情况下,以PDx为基础的联用疗法几乎都能带来一些改善,那么区分信号和噪音就变得格外挑战,筛选患者的标记物以及如何进行最有效的联用将是未来几年开发和投资的重点之一。
(四)、这些肿瘤免疫疗法和组合的定价将成为一个焦点问题。当这些相似的疗法全部迈入市场时,其中大部分都会采用联用组合,累加的定价模型将无法适用。这些肿瘤药物的联用方式,在支付者看来并不是1+1=2。此外,支付者还会说服药厂进行价格竞争:“把PDx按照批发价折扣,我们就会把它作为肿瘤患者的基础疗法”。这一现象在一些拥挤的领域(例如TNFs和他汀类药物)里已经发生了。然而肿瘤药物相对于一般药物来说价格要高得多,这些高价肿瘤药的联用将会导致胜出者能够在支付者渠道里有着深层渗透,建立各种捆绑定价模型。药厂们是否会首次真正在同一类疗法上进行价格战?此外,由于生存曲线的不断延长,更多的肿瘤患者将会有更长的时间来使用更多的疗法。希望支付者们能够合理地建立这些假设和价格模型,不至于像如今的丙肝治愈疗法那样打得措手不及。
而这些问题给了生物医药界带来了许多战略上的机会挑战:
肿瘤免疫五强药企:这五家在肿瘤免疫哨卡抑制剂和细胞疗法上已基本站稳脚跟的大药企(BMS、默克、罗氏、阿斯利康、诺华)正聚焦于巩固他们“基础疗法”的地位,着眼于提升在各种适应症中的治疗地位(例如进入NSCLC的一线治疗),战略要点就是开展尽可能多的临床试验和尽可能多的联合疗法。这五强的BD们也都在关注着尽可能多的联用疗法合作机会。当这一切尘埃落定时,这五家的PDx在使用上估计无法相互替换,而竞争中取胜的方式之一就是获取大量的有效临床数据。
其他大药企:如果没有强有力的临床阶段免疫哨卡项目来打基础,可能就已经错失这波机会了,毕竟在现如今加入这一战局需要进行对外合作方面的巨大战略赌注。获得一个基础性的PDx产品成为关键,将自己现有的肿瘤管线与合适的肿瘤免疫产品联用是一个有效的战略(例如将自家的MEK激酶抑制剂与别家的PDx产品联用等),但除非在合作交易方面有独创性的部分,否则因为主导的PDx产品不是自己的,定价问题将会成为巨大阻碍(前文提到的1+1≠2的问题)。这些药企可能会考虑直接跳入下一代产品的平台(例如溶瘤病毒、双功能抗体、下一代CART/细胞疗法等)或者靶点(例如TAMs/MDSCs等),以此来换取PDx产品机会。这部分企业还将面临许多战略问题。我们可以大胆假设一下,一个目前没有PDx产品的企业可以和支付者们达成协议来共同开发PD1/PDL1单抗的生物仿制药,以“成本价”供应,前提是使用其开发的联合疗法,甚至联合用药中的PDx可以免费供应。无法预测这一方式现实中是否能真正能实行(这将是是Optivo/Keytruda问世十几年后的事了),但支付者们总会对廉价的PDx的感兴趣的。更多的有创意的想法将是这些目前没有PDx产品的公司所需要的。
新兴生物技术公司:传统的免疫哨卡领域,T细胞肿瘤免疫方式将会是代价越来越高的玩法,作为一家小型生物公司,无论是否上市企业,都会需要海量的资金来支撑肿瘤免疫新项目的开发。对于许多企业来说充沛的资金来源目前不是问题(例如Forty Seven、 Gritstone、 Surface等),但现实情况是多个适应症的平行1b/2a期试验(或者篮子试验)需要超出风险的资金和超大的专业团队来运行,对于大部分新兴的生物技术公司来说难以实现。此外,与Opdivo或者Keytruda这些药物的联用需要强大的谈判能力来控制临床试验的用药花费,因此长期看来,选择一个拥有肿瘤资源的财大气粗的大药厂合作伙伴将无疑是一条最佳途径。对于这些选择合作的生物技术公司而言,如何保留住关键市场的产品权益来获取长期发展,或者如何获取未来最佳的并购价值,将成为重要的一环。
初创企业与风投:考虑到之前提到的种种问题:管线拥堵、信号噪音区分、竞争激烈、商业化等,建立一家新的专攻免疫检查点抑制剂的生物公司在目前看来并不是一个好选择。进入这一领域的新公司必须要有真正的区分优势:包括新的模式、全新靶点、全新方式等。但是仅有新颖性也不够,还需要转化医学的前期研究以及尽早寻找出如何与基础疗法联用,最好能在临床前就能证明。另一个严峻的挑战就是人才招募,有经验的肿瘤免疫专家以及CMO/CSO恐怕是如今整个业界最炙手可热的人才。在初始阶段就考虑到未来与药企合作也是十分重要的:哪些药企会最“需要”这些产品来完善他们现有的管线(例如肿瘤免疫五强药企),或是哪些药企需要这一前沿项目来迈入肿瘤免疫领域(例如其他药企)。对于这一领域的投资和周期而言,意识到初创企业与药企合作的需求也是很重要的。比如,如果每家企业都已经有了一个PDx或者CTLA4项目,你如何有信心你自己的会有吸引力?这些靶点如今已不再受到投资老手的青睐。
伴随着突破性的临床数据发布,肿瘤生存期和涵盖的肿瘤种类都已经得到了巨大改善,肿瘤免疫治疗的大爆发无疑对患者是一个好消息。但是如同所有的高竞争领域一样,肿瘤免疫疗法的战场上有赢家也会有输家,肿瘤药企面对这一快速变革领域制定的战略将会左右他们的命运。未来的五年将会无比值得期待。
推荐原文
I/O: The Strategic Supernova In Cancer Today(来源:lifescivc.com)。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..