编者按:2025年,美国FDA旗下的药物评价和研究中心(CDER)批准了46款创新药。作为创新赋能者、客户信赖的合作伙伴以及全球医药及生命科学行业的贡献者,药明康德将持续通过独特的“CRDMO”业务模式,助力更多合作伙伴,为全球病患带来突破性创新疗法。根据PDUFA的目标日期,预计2026年3月,美国FDA将对4款创新药物是否获批做出监管决定,本文将对这些疗法进行相关介绍。
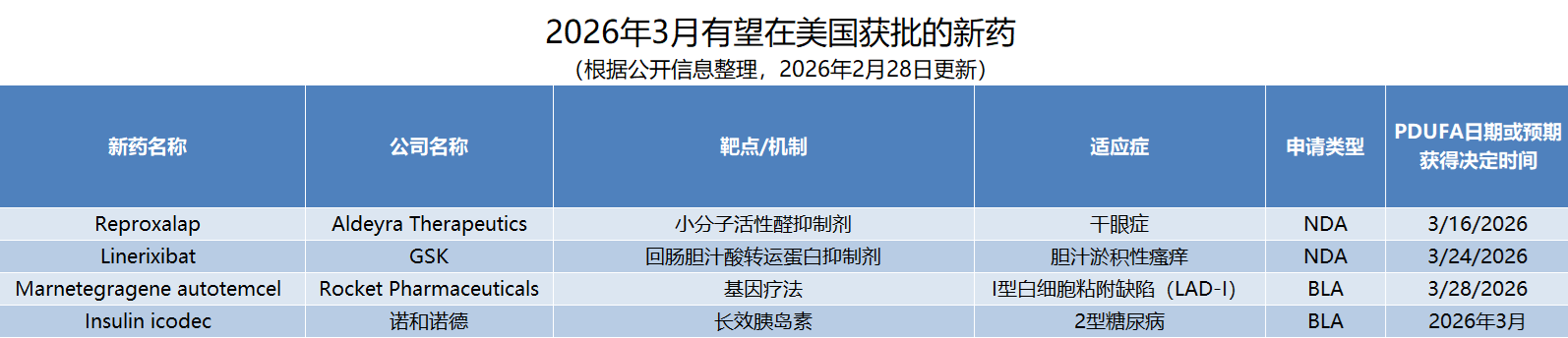
▲3月美国FDA可能批准的新药
活性成分:Reproxalap
适应症:干眼症(DED)
公司名称:Aldeyra Therapeutics
Reproxalap是一款潜在“first-in-class”的在研小分子活性醛抑制剂。活性醛含量会在眼部或系统性炎症时上升,造成眼睛发炎、发红、泪水分泌降低以及改变泪水内脂质组成,许多干眼症患者具有较高的活性醛含量。
2025年5月,Aldeyra Therapeutics宣布reproxalap在一项随机双盲、载体对照的3期临床试验中达到主要终点,在改善眼部不适的主要终点方面,reproxalap在统计学上显著优于载体(P=0.002)。在这项3期临床试验中,患者在进入干眼室(dry eye chamber,一个让患者更容易出现干眼症状的不良环境)前接受reproxalap或载体。在随机分配的116名患者中,58名患者接受了reproxalap治疗,58名患者接受了载体。主要终点为干眼室暴露80至100分钟期间的眼部不适评分变化。试验结果显示接受reproxalap治疗的患者眼部不适显著降低。
活性成分:Linerixibat
适应症:原发性胆汁性胆管炎(PBC)患者的胆汁淤积性瘙痒
公司名称:GSK
Linerixibat是一种回肠胆汁酸转运蛋白(IBAT)口服抑制剂,具有治疗与PBC相关的胆汁淤积性瘙痒的潜力。通过抑制胆汁酸的重吸收,linerixibat旨在解决胆汁淤积性瘙痒的根本原因。
Linerixibat的申请基于3期临床试验GLISTEN的积极结果。2025年5月公布的结果显示,GLISTEN试验达到主要终点,接受linerixibat治疗的患者(n=119)在24周内瘙痒显著改善,优于安慰剂组(n=119)。通过最严重瘙痒程度的数值评分量表(WI-NRS)进行评估,两组之间的最小二乘均值差为-0.72(95% CI:-1.15,-0.28,P=0.001)。该结果显示,linerixibat有望缓解PBC患者的一项主要症状——顽固性瘙痒。
该研究还达成多个关键次要终点,包括第2周瘙痒评分改善及24周内瘙痒相关睡眠干扰评分的改善,具体表现如下:
瘙痒改善起效迅速,第2周即优于安慰剂组,差异具有统计学意义(最小二乘均值差为-0.71,95% CI:-1.07,-0.34,P<0.001),且疗效在整个试验周期内持续维持。在24周的治疗周期中,与安慰剂相比,linerixibat显著改善了瘙痒引起的睡眠干扰,该症状对患者生活质量影响显著。到第24周,linerixibat组中有56%的患者瘙痒评分改善具有临床意义(WI-NRS降低≥3分),而安慰剂组为43%,治疗组之间的差异为13%(95% CI:0,27)。
活性成分:Marnetegragene autotemcel
适应症:严重I型白细胞粘附缺陷(LAD-I)
公司名称:Rocket Pharmaceuticals
Marnetegragene autotemcel是一款用以治疗LAD-I的在研基因疗法,该疗法通过慢病毒对患者的自体造血干细胞进行基因工程化改造,以递送ITGB2基因的功能性拷贝。该基因编码β2整合素成分CD18,这是一种促进白细胞粘附并使其从血管中渗出以抵抗感染的关键蛋白质。
该疗法全球1/2期关键研究的数据显示,在18至45个月的随访期间,接受marnetegragene autotemcel治疗的全部9名严重LAD-I患者皆展现持续的疗效与安全性。在没有进行造血干细胞移植(HSCT)的情况下,所有9例患者在输注后至少18个月时观察到100%的生存率;所有在入组时年龄小于12个月的患者在没有进行HSCT的情况下,生存时间皆超过了24个月。该试验达到所有主要和次要终点,marnetegragene autotemcel同时表现出良好的安全性。
活性成分:依柯胰岛素(insulin icodec)
适应症:2型糖尿病
公司名称:诺和诺德
依柯胰岛素是人胰岛素类似物,其氨基酸结构有三处进行了替换,并附加了C20二十烷脂肪二酸链,使该分子能够可逆地与白蛋白结合,从而将半衰期延长至196小时(约7天),并在经过连续3至4周、每周一次给药后达到稳定状态。该疗法被设计为一周一次皮下注射使用,用于给使用每日胰岛素注射的2型糖尿病成人患者提供每周一次的治疗选择。
依柯胰岛素的申请得到了包含5项随机、活性对照临床试验的3期临床项目ONWARDS的支持。该项目共纳入约4000名2型糖尿病成人患者,这些临床试验比较了依柯胰岛素和每日一次注射的胰岛素的疗效,主要终点为糖化血红蛋白(A1C)与基线相比的变化。所有试验结果均已发表。相较于每日注射的胰岛素,依柯胰岛素在2型糖尿病患者中达到了更优的血糖降幅和更优的血糖处于目标范围内的时间。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..