本期看点:
1. GSPT1靶向分子胶降解剂用于治疗转移性去势抵抗性前列腺癌(mCRPC)的早期临床试验结果积极,携带雄激素受体(AR)突变患者的靶病灶均观察到缩小,疾病控制率达100%。
2. PRO-XTEN双掩蔽CD3 T细胞衔接器(TCE)VIR-5500用于治疗mCRPC,在一项1期临床试验中使82%的可评估高剂量队列组患者实现前列腺特异性抗原(PSA)下降≥50%(PSA50)。
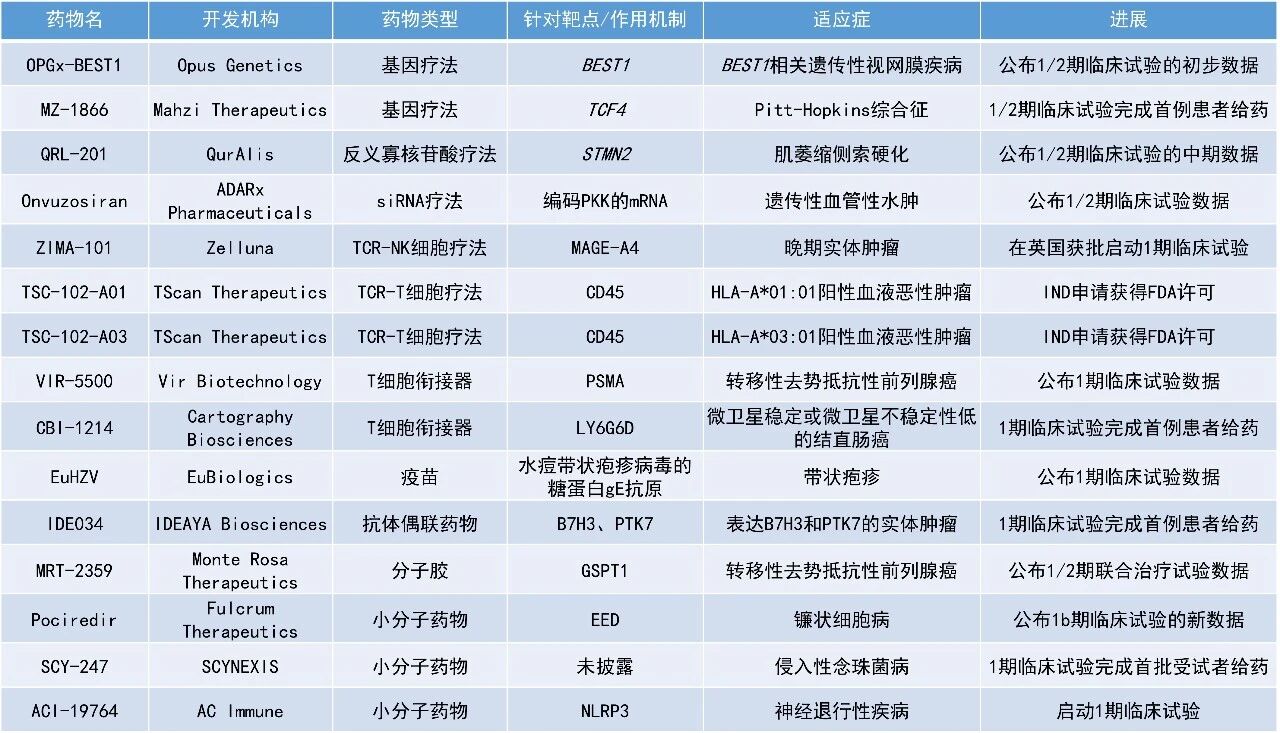
MRT-2359:公布1/2期联合治疗试验数据
Monte Rosa Therapeutics公司公布了一项进行中的1/2期临床研究的最新临床数据。MRT-2359是一款高效、高选择性、口服生物利用度良好的在研GSPT1靶向分子胶降解剂。包括前列腺癌在内的MYC驱动型肿瘤依赖增强的致癌蛋白翻译以支持快速生长。MRT-2359通过选择性降解翻译终止因子GSPT1以破坏蛋白翻译过程,从而产生治疗效果。MRT-2359治疗可降低多种与前列腺癌相关的致癌蛋白水平,包括AR、MYC及细胞周期蛋白D1-E2F,并在多种mCRPC临床前模型中显示出显著的抗肿瘤活性。
该研究评估其在研分子胶降解剂MRT-2359联合恩扎卢胺(enzalutamide),在既往接受多线治疗的mCRPC患者中的疗效。分析显示,整体15例可评估患者的RECIST疾病控制率达到67%(10/15),包含10例患者靶病灶出现缩小。携带AR突变患者的靶病灶均观察到缩小,疾病控制率达100%。数据显示治疗效果具有持续性,尤其是在AR突变患者或既往未接受AR抑制剂治疗的患者中更为明显。在AR突变患者中,5例中有2例治疗持续10个周期或更长,且截至数据截止日仍有2例继续接受治疗。安全性方面,MRT-2359联合恩扎卢胺总体耐受性良好,不良事件可控。公司计划于2026年第三季度启动一项新的验证性2期研究,针对携带AR突变的患者开展评估。
VIR-5500:公布1期临床试验数据
Vir Biotechnology公司公布了其在研药物VIR-5500用于治疗晚期mCRPC的1期临床试验数据。VIR-5500是一款靶向前列腺特异性膜抗原(PSMA)的PRO-XTEN双掩蔽CD3 T细胞衔接器,可在到达肿瘤微环境前保持非活性状态,从而降低脱靶效应并提升治疗指数。近日,安斯泰来(Astellas Pharma)与Vir Biotechnology达成超17亿美元的全球战略合作,将共同推进VIR-5500的开发与商业化。
此次公布的数据显示,IR-5500单药具有良好的安全性和耐受性,迄今未观察到剂量限制性毒性。截至2026年1月9日的数据,在≥3,000 µg/kg的高剂量队列中,82%(14/17)的可评估患者达到PSA50,53%(9/17)达到PSA下降≥90%(PSA90);在RECIST可评估患者中,客观缓解率(ORR)达45%(5/11),其中4例已确认缓解。PSMA-PET影像也证实了多发肿瘤病灶(包括内脏转移灶)的显著缩小。
Pociredir:公布1b期临床试验的新数据
Fulcrum Therapeutics公司公布了其在研疗法pociredir在镰状细胞病(SCD)患者中开展的1b期PIONEER临床试验的新数据。Pociredir是一种靶向胚胎外胚层发育蛋白(EED)的口服小分子抑制剂。通过抑制EED,pociredir可有效下调关键的胎儿珠蛋白阻遏蛋白(包括BCL11A),从而导致胎儿血红蛋白(HbF)水平升高。
此次公布的数据显示,pociredir治疗表现出快速、显著且具有临床意义的疗效:12例患者在第12周时平均HbF的绝对水平从7.1%提升至19.3%(增加12.2个百分点),表达HbF的红细胞比例从31%升至63%,显示泛细胞型HbF诱导。58%(7/12)患者的HbF水平≥20%,所有患者的HbF水平均至少提升6.5个百分点。同时,溶血标志物改善、红细胞生成增强,并实现总血红蛋白平均升高超1 g/dL。截至2025年12月23日的数据,pociredir总体耐受性良好,未出现治疗相关严重不良事件(SAEs),亦无患者因治疗相关不良事件而停药。58%(7/12)的患者在治疗期间未发生任何血管阻塞危象(VOC)。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..