近期,全球多肽和寡核苷酸(TIDES)领域迎来系列进展。Ionis Pharmaceuticals公司用于治疗严重高甘油三酯血症(sHTG)的反义寡核苷酸(ASO)疗法olezarsen的3期临床试验结果亮眼,患者的空腹甘油三酯水平显著降低,急性胰腺炎事件减少85%。诺华连续达成两起大额RNA干扰(RNAi)疗法交易,聚焦突触核蛋白病及心血管疾病。本文将节选其中部分重要进展做简单介绍,仅供读者参阅。
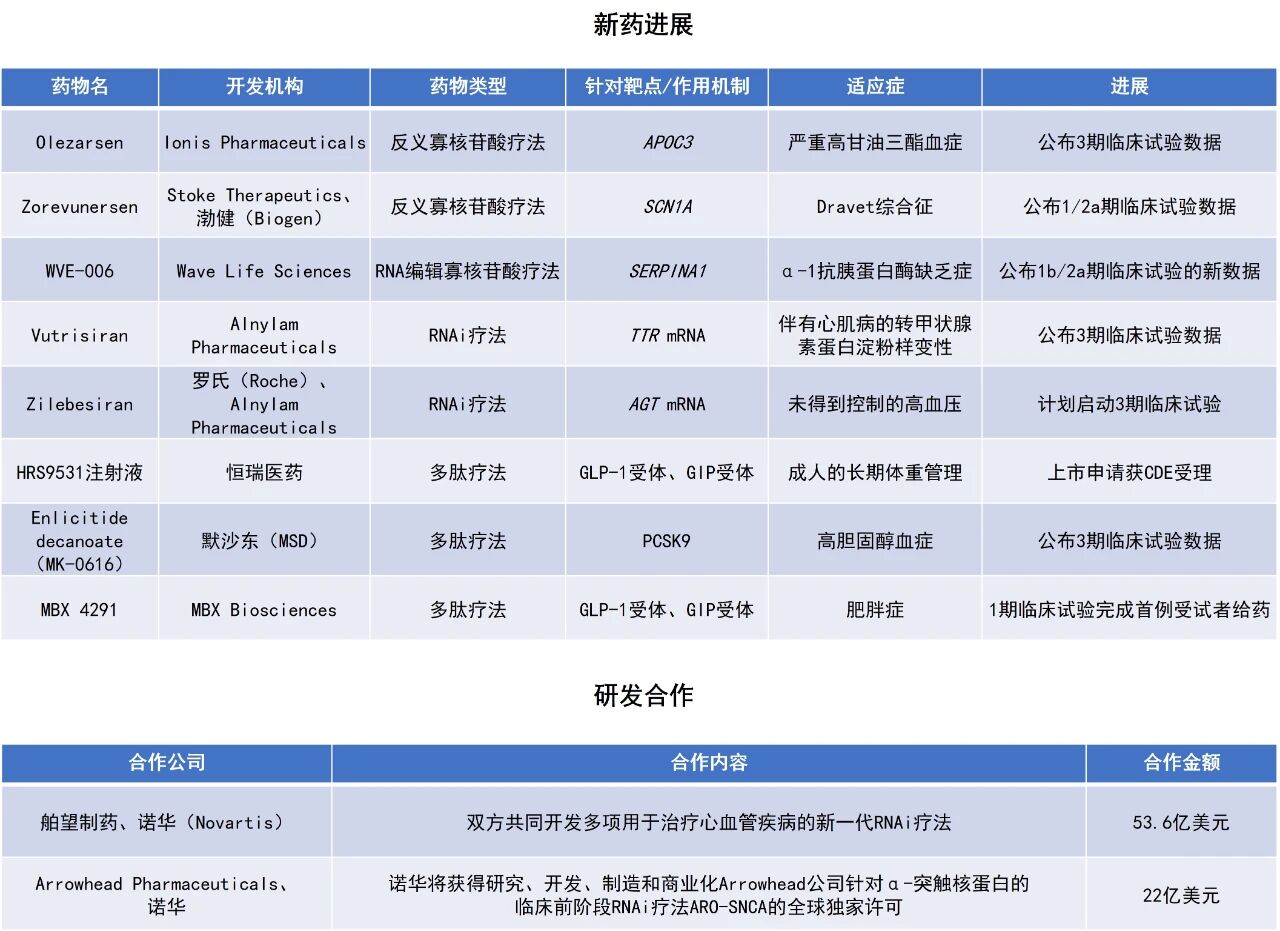
Olezarsen:公布3期临床试验数据
Ionis Pharmaceuticals公司宣布,其ASO疗法olezarsen用于治疗严重高甘油三酯血症的关键性3期CORE和CORE2研究取得积极结果。Olezarsen旨在抑制机体产生载脂蛋白C-III(apoC-III,一种在肝脏中产生的调节血液中TG代谢的蛋白)。美国FDA于2024年2月授予该疗法孤儿药资格和突破性疗法认定(BTD),并在12月批准其用于作为饮食控制的辅助治疗,以降低家族性乳糜微粒血症综合征成人患者的甘油三酯。
此次公布的分析显示,CORE和CORE2研究达到主要终点:在第6个月时,olezarsen与安慰剂比较均显示出高统计学显著性的空腹甘油三酯水平降低,经安慰剂调整,接受80 mg与50 mg的剂量患者的甘油三酯水平分别平均降低72%与63%(p<0.0001)。研究还达到了急性胰腺炎事件减少的次要终点。与安慰剂相比,olezarsen使事件发生率显著降低了85%(p=0.0002)。此外,olezarsen显示出良好的安全性和耐受性。根据此积极结果,Ionis计划在年底前向美国FDA提交补充新药申请(sNDA)。
Ionis首席执行官Brett Monia博士在接受行业媒体Endpoints News采访时表示:“这一结果史无前例,具有突破性,令人瞩目。在这一患者群体中,从未有过急性胰腺炎事件减少85%的结果。”
诺华达成两起大额RNAi疗法交易
9月2日,Arrowhead Pharmaceuticals公司宣布与诺华达成一项全球授权与合作协议,诺华将获得研究、开发、制造和商业化其临床前阶段的RNAi疗法ARO-SNCA的全球独家许可。该药物靶向α-突触核蛋白,旨在治疗帕金森病等突触核蛋白病。协议还涵盖利用Arrowhead公司专有的靶向RNAi分子(TRiM)平台开发的其他合作靶点。根据协议条款,交易完成后,Arrowhead公司将获得2亿美元的首付款,并有资格获得最高20亿美元的潜在里程碑付款等款项。
9月3日,舶望制药宣布与诺华达成一项新战略合作协议,双方将共同开发多项心血管产品。此次新达成的协议是在双方现有合作基础上的进一步拓展。根据协议,双方将共同探索ANGPTL3联合疗法用于治疗血脂异常,同时协议还包含诺华对舶望制药管线中下一代分子的许可选择权;诺华获得舶望制药一项目前处于IND支持性研究阶段的RNAi候选分子的权益。舶望制药将获得1.6亿美元的预付款,并可能获得潜在高达52亿美元的里程碑付款等款项。
Enlicitide decanoate(MK-0616):公布3期临床试验数据
默沙东(MSD)宣布,其在研药物enlicitide decanoate在3期临床试验CORALreef Lipids中取得了积极的顶线结果。Enlicitide是一种新型口服、每日一次的小分子环肽类药物,能够与PCSK9结合并抑制PCSK9与LDL受体相互作用,旨在通过与目前获批的注射型PCSK9抑制剂相同的生物学机制降低低密度脂蛋白胆固醇(LDL-C)。根据新闻稿,enlicitide有望成为全球首个口服PCSK9抑制剂,为高胆固醇血症患者提供一种无需注射的新型治疗选择。
该临床试验达到了所有主要和关键次要终点。与安慰剂相比,enlicitide在第24周时显著且具有临床意义地降低了LDL-C,同时在非高密度脂蛋白胆固醇(non-HDL-C)、载脂蛋白B(ApoB)和脂蛋白(a)等关键指标上也实现了统计学和临床意义上的显著改善。安全性方面,两组间的不良事件(包括严重不良事件)的发生率相似,因不良事件导致的停药率低且组间无明显差异。
HRS9531注射液:上市申请获CDE受理
中国国家药监局药品审评中心(CDE)官网公示,恒瑞医药申报的1类创新药HRS9531注射液的上市申请获受理,适用于在控制饮食和增加运动基础上,初始身体质量指数(BMI)符合以下要求的成人的长期体重管理:≥28 kg/㎡(肥胖),或≥24 kg/㎡(超重)并伴有至少一种体重相关合并症(例如高血糖、高血压、血脂异常、阻塞性睡眠呼吸暂停、脂肪肝等)。
HRS9531注射液是恒瑞医药自主研发的胰高血糖素样肽-1(GLP-1)和葡萄糖依赖性促胰岛素肽(GIP)双重受体激动剂,具有改善胰岛素抵抗、抑制食欲、降低血糖和减轻体重等作用。此次申报上市,是基于一项在肥胖或超重成人受试者中开展的多中心、随机、双盲、安慰剂平行对照的3期临床试验HRS9531-301的积极结果。与安慰剂相比,HRS9531所有剂量组(2 mg、4 mg、6 mg)在共同主要终点及全部关键次要终点均达到优效性;6 mg组平均减重19.2%,且未达平台期,有44.4%的受试者体重降低≥20%。此外,HRS9531注射液的安全性和耐受性良好,与其他GLP-1类药物相似。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..