3 月 13 日,CDE 官网显示,礼来 1 类新药 LY3549492 片的临床申请获得 CDE 受理。这是该药首次在国内申报临床。LY3549492 是一款胰高血糖素样肽-1 受体(GLP-1R)非肽类激动剂(NPA),目前正在海外开展一项双盲 Ⅱ 期临床研究(NCT06683508),以比较每天使用一次 LY3549492 与安慰剂对肥胖或超重成人受试者进行体重管理的效果。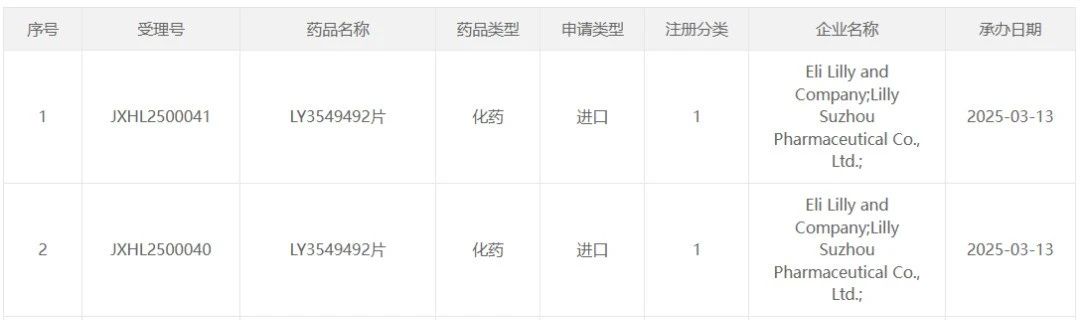
图源:CDE 官网口服 GLP-1 是当前减肥药领域竟争的新高地。虽然诺和诺德的口服版司美格鲁肽早已获批上市,但其仍属于多肽药物,生物利用度仍有提升空间。此外,成本和产能也是传统多肽药物的弊端。与传统的肽类 GLP-1R 激动剂相比,GLP-1R 非肽类小分子激动剂具有诸多优势,包括:可口服给药,提高患者依从性;生物利用度更高;化学稳定性高,在储存和运输中更稳定,不易降解;生产成本低,更容易实现大规模生产等等。因此,口服小分子 GLP1 已成为当下的研发热点。礼来在该领域早有布局。除了 LY3549492,礼来开发的 Orforglipron(LY3502970)也是一种非肽类口服 GLP-1R 小分子激动剂,该药可谓是小分子 GLP-1R 药物的先驱。Orforglipron 最早由日本公司中外制药株式会社研发,2018 年礼来以 5000 万美元首付款拿到了它的全球开发和商业化权利。目前, Orforglipron 正在开展治疗肥胖、2 型糖尿病,、阻塞型睡眠呼吸暂停等适应症的 Ⅲ 期临床,是研究进度最快的 GLP-1R 小分子激动剂。国内药企中,恒瑞(HRS-7535)、闻泰医药/箕星药业(VCT220)的 GLP-1R 小分子也已进入 Ⅲ 期。
