齐鲁制药利托那韦片、枸橼酸伊沙佐米胶囊仿制药同日获批
2月7日,国家药监局官网显示,齐鲁制药申报的仿制药利托那韦片、枸橼酸伊沙佐米胶囊同日获批生产并视同过评。其中,枸橼酸伊沙佐米胶囊为国内首仿+首家过评。伊沙佐米是一款口服的高选择性的蛋白酶体抑制剂,可与来那度胺和地塞米松联合,用于治疗既往至少接受过一线治疗的多发性骨髓瘤。
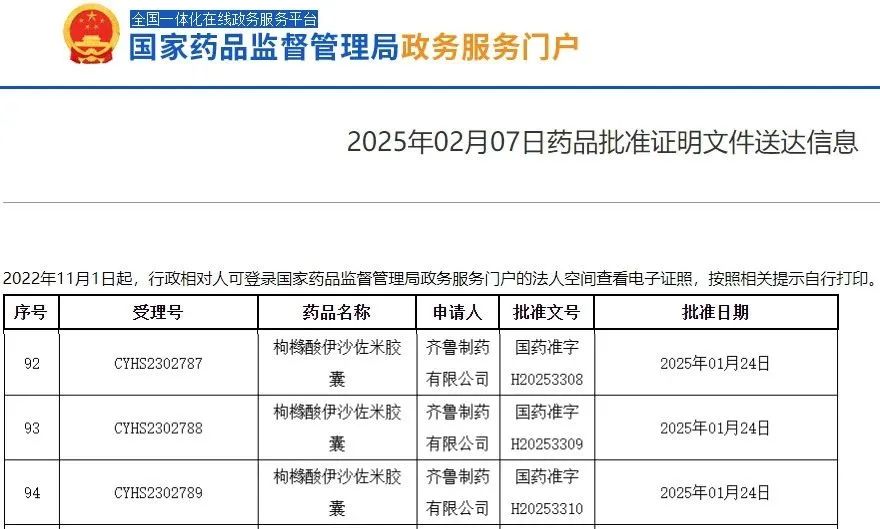
据悉,仿制药申报方面,齐鲁制药的枸橼酸伊沙佐米胶囊于2023年10月报产,并于近日顺利获批生产,为国内首仿+首家过评。此外,中美华东、天士力等企业的产品正在开展BE试验,尚未报产。
2月8日,中国国家药监局(NMPA)官网最新公示,神州细胞申报的1类新药菲诺利单抗注射液上市申请已获得批准。这是神州细胞自主研发的重组人源化抗PD-1 IgG4型单克隆抗体注射液,获批适应症为与含铂化疗联合用于复发性和/或转移性头颈部鳞状细胞癌的一线治疗。
头颈部鳞状细胞癌(HNSCC)是全球常见癌症,该病侵袭性强并且难于治疗,HNSCC通常与高度心理压力和生活质量降低相关。复发/难治性HNSCC患者预后较差,在接受一线铂类标准治疗失败后,目前二线标准治疗的中位生存期仅为8个月左右,临床需求亟待满足。
菲诺利单抗(finotonlimab,产品代号为SCT-I10A)为抗PD-1的功能性单克隆抗体,可通过阻断PD-1与其配体的结合,增加肿瘤部位的T细胞和炎性细胞因子供给量,减少肿瘤微环境中的调节性T细胞和髓系来源的抑制细胞的比例,改变肿瘤微环境,恢复和提高T细胞的免疫杀伤功能,从而抑制肿瘤的生长。
在人的心血管系统、皮肤、平滑肌及胃部的靶细胞中至少有着4种亚型的组胺受体(H1受体、H2受体、H3受体和H4受体)。其中组胺H1受体主要分布于血管内皮、气道平滑肌等多种细胞,与过敏反应的关系非常密切。靶向组胺H1受体的抗组胺药可将被组胺激活的受体下调至未激活的状态,下调过敏性炎症,减少促炎症细胞因子和细胞黏附分子的表达,并减弱嗜酸性粒细胞等的趋化作用,进而发挥生物学效应。
根据赛诺菲此前新闻稿介绍,非索非那定是二代新型抗组胺药,具有起效快、24小时长效,且不引起嗜睡,脑部受体占有率低等特点。其对H1受体的亲和力较高,表明其较好的心脏安全性。
2021年,赛诺菲研发的盐酸非索非那定片剂剂型获NMPA批准上市,用于过敏性鼻炎及慢性特发性荨麻疹的治疗。目前,赛诺菲已经针对该产品开发了胶囊、片剂、复方制剂等多种剂型。2006年,该产品的儿童口服混悬液在美国获批上市。公开资料显示,口服混悬液相比于片剂剂型,有可能帮吞咽困难的人提供更方便的治疗选择。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..