华海药业「阿达木单抗」生物类似药申报上市
12月14日,中国国家药监局药品审评中心(CDE)网站最新公示,华海药业阿达木单抗注射液生物类似药上市申请已获得受理。
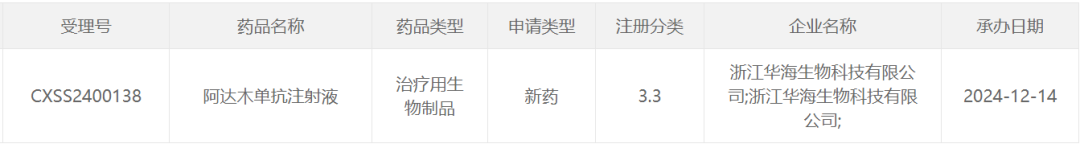 截图来源:CDE官网
截图来源:CDE官网
阿达木单抗为全人源化抗TNF-α单抗,原研产品由艾伯维(AbbVie)研发。该产品可特异性地与TNF-α结合,阻断其与TNF受体p55和p75的相互作用,从而有效阻断TNF-α介导的一系列致炎作用,对多种自身免疫疾病起到有效持久的控制。凭借在自免疾病领域良好的疗效和安全性,阿达木单抗已经获多个全球权威自免类诊疗指南的推荐。根据华海药业此前新闻稿介绍,该公司此前从美国Oncobiologics公司引进了阿达木单抗生物类似药产品。根据中国药物临床试验登记与信息公示平台官网,华海药业控股子公司华奥泰生物已经完成一项3期临床研究,该研究旨在评价重组全人源抗肿瘤坏死因子-α单克隆抗体注射液(HOT-3010)与阿达木单抗原研产品治疗成年中重度慢性斑块状银屑病的有效性和安全性。
礼来重磅新药「替尔泊肽」在中国申报第五项上市申请
12月14日,中国国家药监局药品审评中心(CDE)网站最新公示,礼来(Eli Lilly and Company)重磅药物GIP/GLP-1受体双重激动剂替尔泊肽注射液新适应症上市申请获得受理,具体适应症尚未披露。根据CDE官网查询,这是替尔泊肽在中国递交的第五项上市申请,其中两项上市申请此前已经获NMPA批准。
替尔泊肽(tirzepatide)是一款葡萄糖依赖性促胰岛素多肽(GIP)和胰高血糖素样肽-1(GLP-1)受体激动剂,每周一次注射。该产品分别于2022年5月和2023年11月获得美国FDA批准,用于糖尿病以及肥胖和超重患者。在中国,替尔泊肽于今年5月获批首个适应症,用于成人2型糖尿病患者血糖控制。今年7月,该产品再次获NMPA批准用于改善成人肥胖或伴有至少一种体重相关合并症的超重患者长期体重管理。根据礼来官网的管线资料,替尔泊肽还针对多项适应症处于3期临床研究阶段,包括用于降低肥胖的发病率和死亡率、减少2型糖尿病患者的不良CV结局等。近日,该公司还公布了一项最新3b期试验积极数据,接受替尔泊肽治疗的受试者平均减重50.3磅(22.8公斤),而接受活性对照药物的受试者则平均减重33.1磅(15.0公斤)。
豪森药业和朱养心药业拿下「司来帕格片」首仿
12月12日,据NMPA官网显示,豪森药业与朱养心药业的司来帕格片于同日获批上市,皆为该品种首仿。据公开资料显示,该药物用于治疗肺动脉高压等疾病。
原研司来帕格是Nippon Shinyaku与Actelion Pharmaceuticals(已被强生收购)合作开发的一款前列腺素I2(PGI2)受体激动剂,于2015年12月首次在美国获批上市,用于治疗肺动脉高压(PAH,WHO I组),以延缓疾病进展并降低因PAH住院的风险。2018年11月,司来帕格片在中国获批上市。原研司来帕格的化合物中国专利已于2022年到期。
 截图来源:CDE官网
截图来源:CDE官网