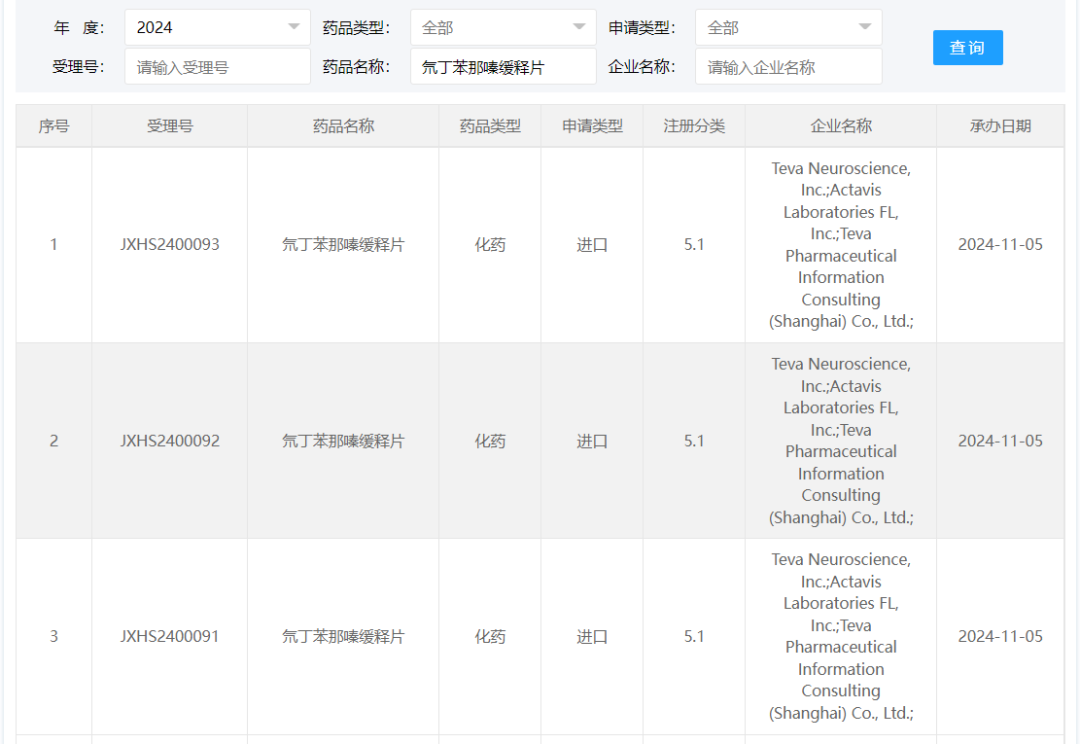
11月5日,CDE官网显示,梯瓦递交的「氘丁苯那嗪缓释片」的5.1类进口申请获CDE受理,相关受理号为:JXHS2400088/89/90/91/92。
氘丁苯那嗪是囊泡单胺转运蛋白 2(VMAT2)抑制剂丁苯那嗪的氘代药物。2008年,FDA加速批准Prestwick公司研发的丁苯那嗪(商品名:Xenazine),治疗亨廷顿舞蹈病,这也使丁苯那嗪成为美国首个获批治疗亨廷顿舞蹈病的药物。
氘丁苯那嗪是丁苯那嗪的衍生类似化合物,具有丁苯那嗪骨架结构,其中6个氢原子被氘原子代替。氘的掺入会降低药物代谢的速度,从而减少频率的给药。相比丁苯那嗪母体,氘代丁苯那嗪具有更长的半衰期,药代动力学特征得到明显的改善。
2017年4月,Auspex Pharmaceuticals(2015年被梯瓦斥资35亿美元收购)开发的氘丁苯那嗪片(deutetrabenazine,Austedo/安泰坦)被FDA批准用于治疗与亨廷顿舞蹈症相关的“舞蹈病症状“,成为FDA批准的第二款亨廷顿舞蹈病药物。2017年8月,该药又被FDA批准用于治疗成人迟发性运动障碍。2024年5月,FDA批准氘丁苯那嗪缓释片(Austedo XR)用于治疗成人迟发性运动障碍和亨廷顿病相关舞蹈症。
与氘丁苯那嗪片相同的临床获益下,氘丁苯那嗪缓释片将给药频次从每日两次降低到每日一次,可明显提高患者和护理者的依从性,并减少给药后的血药浓度波动。
在国内,氘丁苯那嗪片于2020年5月被NMPA批准用于治疗成人与亨廷顿病有关的舞蹈病及迟发性运动障碍,成为我国首个获批上市的亨廷顿病治疗药物。2024年2月,恩华药业宣布与梯瓦达成合作,获得氘丁苯那嗪片在中国大陆的独家商业化权益。值得一提的是,南京正大天晴制药已于2024年5月首家提交了氘丁苯那嗪片的4类仿制上市申请。
此次氘丁苯那嗪缓释片在上市申请获CDE受理,距离其在国内获批上市又近一步,期待其早日获批,造福亨廷顿舞蹈病和迟发性运动障碍患者。
亨廷顿病(HD)是一种罕见且致命的神经退行性疾病,由HTT基因1号外显子的CAG重复数异常扩增所致,由于患者会出现不自主运动的运动障碍,又称亨廷顿舞蹈病,临床表现为运动障碍、精神症状和认知障碍。迟发性运动障碍(TD)是长期使用抗精神病药物等多巴胺受体阻滞剂后,患者出现的迟发发作的锥体外系不良反应,主要特征为静坐不能、肌阵挛、抽搐等异常不自主运动,是精神分裂药物治疗过程中存在的共性痛点问题。
囊泡单胺转运蛋白2(VMAT2)对于大脑中所有生物胺的突触传递至关重要,包括5-羟色胺、去甲肾上 腺素、组胺和多巴胺。由于在中枢神经系统的神经生理学和药理学中的重要作用,VMAT2被认为是各种中枢神经疾病领域的重要治疗靶点。
VMAT2抑制剂是治疗TD和HD临床疗效和安全性得到验证的唯一类别药物。除了丁苯那嗪和氘丁苯那嗪,FDA于2017年4月批准Neurocrine Biosciences的VMAT2抑制剂缬苯那嗪(valbenazine,Ingrezza)用于治疗成人TD。缬苯那嗪是FDA批准的首 个TD治疗药物,2023年8月又被FDA批准用于治疗亨廷顿式病成人患者的舞蹈症状。而且,2024年4月,FDA还批准了缬苯那嗪胶囊装颗粒剂,用于治疗迟发性运动障碍和亨廷顿病的舞蹈症状,商品名为Ingrezza Sprinkle。Ingrezza Sprinkle方便吞咽困难或不愿服用胶囊的患者服药,患者可以将其打开并撒在软食物上服用。
此外,目前全球还有几款在研VMAT2抑制剂,如绿叶制药的LY03015、Neurocrine Biosciences的NBI-1065890。
其中LY03015是绿叶制药开发的新一代VMAT2抑制剂,可通过抑制突触前神经元多巴胺(DA)的释放,避免DA对超敏D2受体刺激的同时,也不阻滞突触后膜的D2受体,从而减轻迟发性运动障碍、亨廷顿舞蹈病的症状。临床前结果表明,LY03015能够避免脱靶效应带来的抑郁及自杀风险;具有更理想的消除半衰期和组织分布特性,可实现每天口服一次的用药方式,降低心脏QT间期(心室除极和复极总时间)延长的风险。2021年9月和2022年9月,LY03015先后在国内和美国获批临床。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..