医药行业如火如荼地发展,对相关配套技术也提出了更高的要求,一次性设备的对接技术是大势所趋,以减少隐性的人工成本和人工干预风险,保证产品的质量等,同时减轻监管负担,它显著降低了药品的污染风险,为制药厂等无菌需求严苛的场所提供了坚实的保障。值得一提的是,随着行业标准的日益完善,由上海市包装技术协会主导制定的《制药工艺一次性无菌连接器》(T/SHBX 006—2024)将于2024年09月07日正式实施。这一规范不仅为制药工艺一次性无菌连接器性能参数提供了明确依据,同时也为药品生产企业在制药工艺一次性无菌连接器验收使用过程中提供了宝贵的参考指南。那么,GMP药品生产企业的质量管理员该如何进行制药工艺一次性无菌连接器的验收确认呢?下面,让我们一起探索这个问题,为药品生产的安全与效率保驾护航。
一、一次性无菌连接器分类和工作原理
一次性无菌连接器,英文Single-Use Sterile Connectors,是指在不依赖洁净环境保护条件下,能够实现两套无菌组件之间无菌对接操作的可抛弃型接头产品。
按照不同的使用功能分为:
(1) “抽纸”原理的一次性无菌连接器:以一张透气或不透气的薄膜作为接头的盲端。两个无菌连接器对接后,将两层薄膜从中间抽走,实现两个接头的连通。两个对接的接头有公母设计,也有不分公母的设计。
(2) “alpha-beta对接”原理的一次性无菌连接器:结构设计类似于隔离器的“alpha-beta对接”阀门。在对接过程中,连接器将在环境中暴露过的两个堵头,密封地转移至一个密封腔室内,从流路中移除,并实现两个组件之间的无菌对接。该原理通常分公母接头设计。
二、制药工艺一次性无菌连接器主要技术参数要求
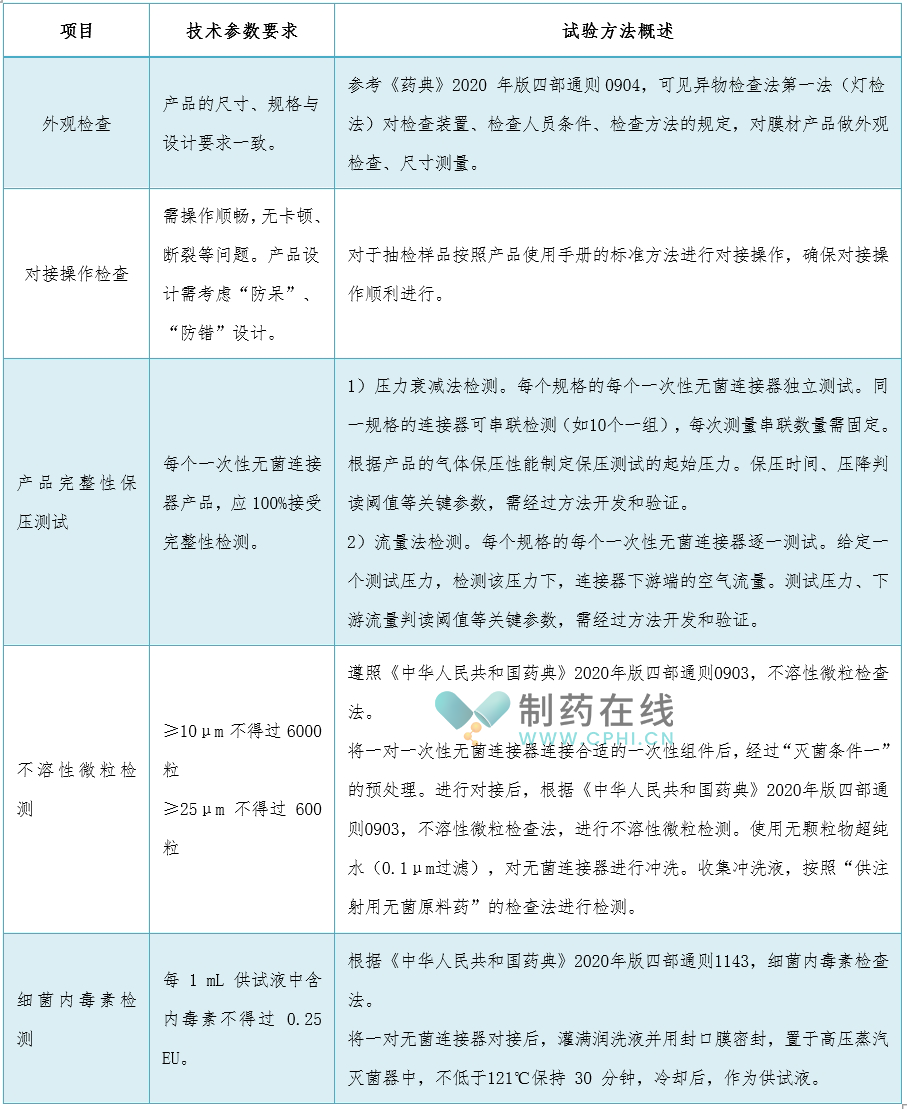
在无菌药品生产领域,作为高度关注产品质量与使用安全性的药品生产企业,对于所采用的一次性无菌连接器产品,其供应商管理尤为重要。企业需严格确保供应商对产品批次进行合理而明确的定义,以追踪每一批次产品的来源、生产日期及关键生产参数,保障产品的可追溯性与质量控制。供应商应遵循GB/T 2828.1《计数抽样检验程序第1部分:按接收质量限(AQL)检索的逐批检验抽样计划》的标准要求,科学计算并执行抽样方案。通过合理的抽样比例,从每批次产品中随机抽取代表性样品,进行严格的出厂检测。检测项目应全面覆盖产品的关键质量特性,包括但不限于:外观、操作性完整性、不溶性微粒、细菌内毒素,所有项目指标都合格时,则判定该批产品为验收合格,常见技术参数和试验方法见下表:
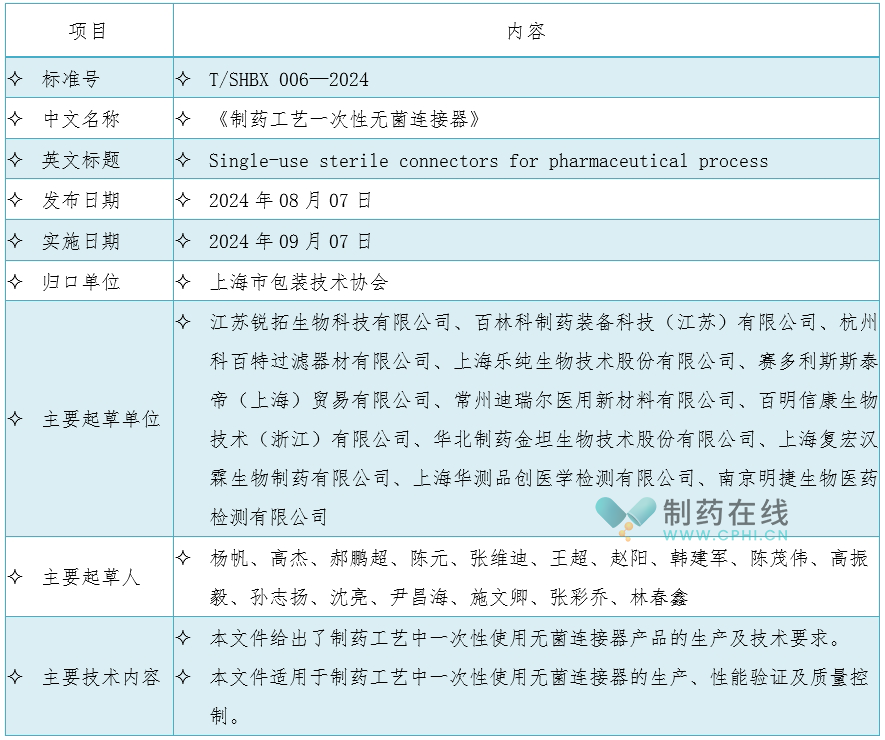
三、《制药工艺一次性无菌连接器》标准信息 备注:标准购买信息:目前该团体标准文本还未对外公布,解读参考了征求意见稿部分内容。 参考文献
[1] www.ttbz.org.cn等
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..