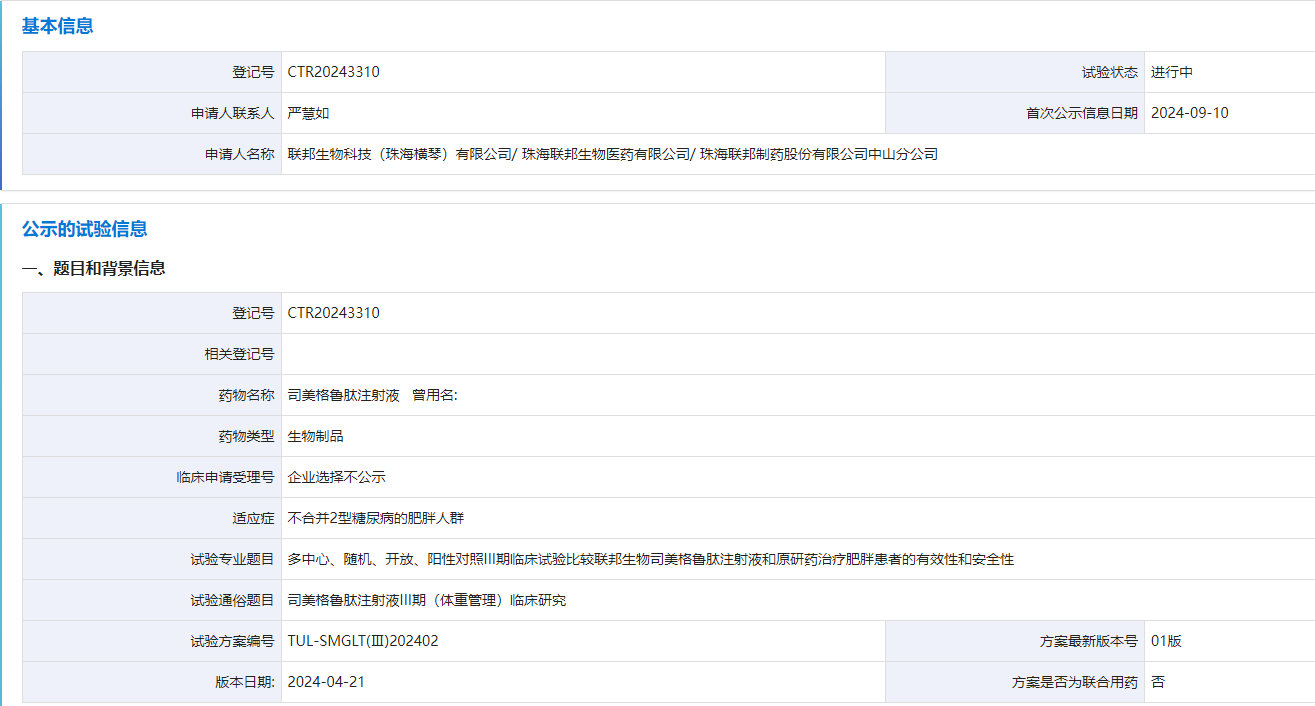
9 月 10 日,CDE 官网显示,联邦制药启动一项多中心、随机、开放、阳性对照 III 期临床试验,比较联邦生物司美格鲁肽注射液和原研药治疗肥胖患者的有效性和安全性。值得注意的是,这是国内第三款启动肥胖 III 期临床的司美格鲁肽。
 截图来源:CDE 官网
截图来源:CDE 官网
Insight 数据库显示,联邦制药的司美格鲁肽类似药用于 2 型糖尿病适应症已在 2023 年 2 月启动 III 临床。在 GLP-1 靶点上,联邦制药除了布局生物类似药外,还有创新药。UBT251 是一款 GCGR/GIPR/GLP1R 三靶点创新药,目前用于 2 型糖尿病、代谢功能障碍相关脂肪性肝病、肥胖适应症正在开展 1 期临床。
Insight 数据库显示,司美格鲁肽在中国的核心序列专利将在 2026 年 3 月 20 日 到期,目前除了报上市的两款类似药外,还有 11 款处于 III 期临床阶段的国产改良新/类似药,包括齐鲁、石药、正大天晴、联邦制药、翰宇药业等等,预计 2026 年将迎来国产司美格鲁肽上市密集期。
四川省医药保化品质量管理协会关于2026
各会员单位: 当前,制药行业正..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..