4 月 15 日,据 CDE 官网显示,信达递交的 IBI133 临床试验申请获得默示许可(受理号:CXSL2400085)。
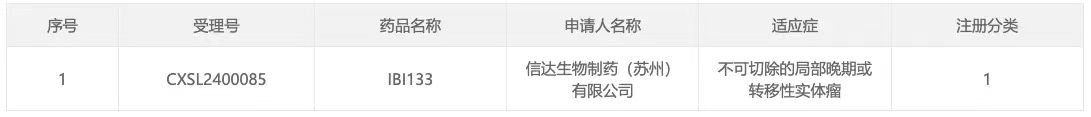
来自:CDE 官网
IBI133 是一款 HER3 ADC,从全球来看,已在去年 12 月在澳大利亚启动了一项 I/II 期临床试验,针对实体瘤患者(登记号:NCT06170190)。在国内,其临床试验申请于 2 月获 CDE 受理,并于今日获批。
目前全球范围内尚未有 HER3 ADC 获批上市,进展最快的为第一三共/默沙东HER3-DXd(U3-1402),BLA 申请已获 FDA 受理并获得优先审查资格,PDUFA 日期为 2024 年 6 月 26 日。此外,另有 8 款进入临床阶段,包括百利天恒/BMS HER3/EGFR 双抗 BL-B01D1 处于 III 期临床阶段。布局企业还涉及恒瑞、映恩生物、石药集团等。在国内,HER3-DXd 以及 BL-B01D1 进展最快,均处于 III 期阶段。
在 ADC 领域,据 Insight 数据库显示,当前信达共有 6 款产品在国内进入临床阶段,此外,另有一款 B7-H3/EGFR 双抗 ADC 新药 IBI3001,刚于本月初在澳大利亚开展 I/II 期临床试验(登记号:NCT06349408),但在国内暂处于临床前阶段。
从靶点来看,当前,据 Insight 数据库显示,全球进入临床阶段的 ADC 新药共有 387 款,TOP5 热门靶点分别为 HER2、TROP2、EGFR、CLDN-18.2 以及 B7-H3。这些热门靶点信达均有布局,此外,还差异化布局了 HER3 以及 CEACAM5。
其中,信达布局的 IBI343 是全球首款登记启动 III 期临床的 CLDN-18.2 ADC,上个季度登记启动了一项 III 期临床试验,针对 Claudin 18.2阳性、HER2 阴性胃或胃食管交界处腺癌(登记号:NCT06238843/CTR20240639)。此后,同类产品,康诺亚/阿斯利康 CMG901 以及礼新医药 TPX-4589 先后进入 III 期。
信达还在探索 IO+ADC 的疗效,上个月启动了 IBI343 联合信迪利单抗二线治疗胃及胃食管交界处癌的 II 期临床试验(登记号:NCT06321913),且已完成首例受试者的入组工作,预计明年 12 月完成主要指标。此外,信达在年报中表示,将探索 IBI343 联合其自研产品信迪利单抗在治疗 1L GC 和雷莫西尤单抗在治疗 2L GC 的 PoC 研究。
针对该靶点,信达分别对应布局了 5 种成分类别的新药管线,进入临床阶段的,除 ADC 外,还有 CAR-T、双抗以及单抗。另有 ISAC 药物处于临床前阶段。
2022 年 11 月,信达在 ClinicalTrials.gov 上登记启动了 HER2 ADC(IBI354)治疗实体瘤受试者的 I/II 期研究(登记号:NCT05636215),去年 7 月也启动了国内部分(登记号:CTR20232339)。该研究计划全球入组 739 名受试者,当前已完成全球首例受试者的入组工作,预计今年 10 月完成主要指标。
去年 6 月,在澳大利亚启动了 TROP2 ADC(IBI130) I/II 期试验(登记号:NCT05923008),同年 11 月完成首例受试者的入组工作,并预计于今年 11 月完成主要指标。在国内,刚于上个月获批临床。
今年,据信达年报,将重点推进一系列具有全球创新潜力的 ADC 项目进入 IND 阶段以及 I 期临床研究,包括 EGFR/B7-H3 ADC(IBI3001),B7-H3 ADC(IBI129)以及今日国内获批临床的 HER3 ADC(IBI133)等。
B7-H3 ADC(IBI129)在国内的临床试验申请刚于上个月获默示许可(受理号:CXSL2400006)。从全球来看,去年 8 月已经启动了一项 I/II 期临床试验,试验地区为奥地利(登记号:NCT05991349),其中,I 期临床计划入组 22-180 例患者,II 期临床部分计划入组约 182 例患者;并预计于 2024 年 11 月初步完成。
当前全球进展最快的 B7-H3 ADC 是第一三共 Ifinatamab deruxtecan,今年 1 月登记启动了 III 期临床试验;国产企业还有翰森制药、映恩生物等布局。
四川省医药保化品质量管理协会关于2026
各会员单位: 当前,制药行业正..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..