国内创新药IND汇总
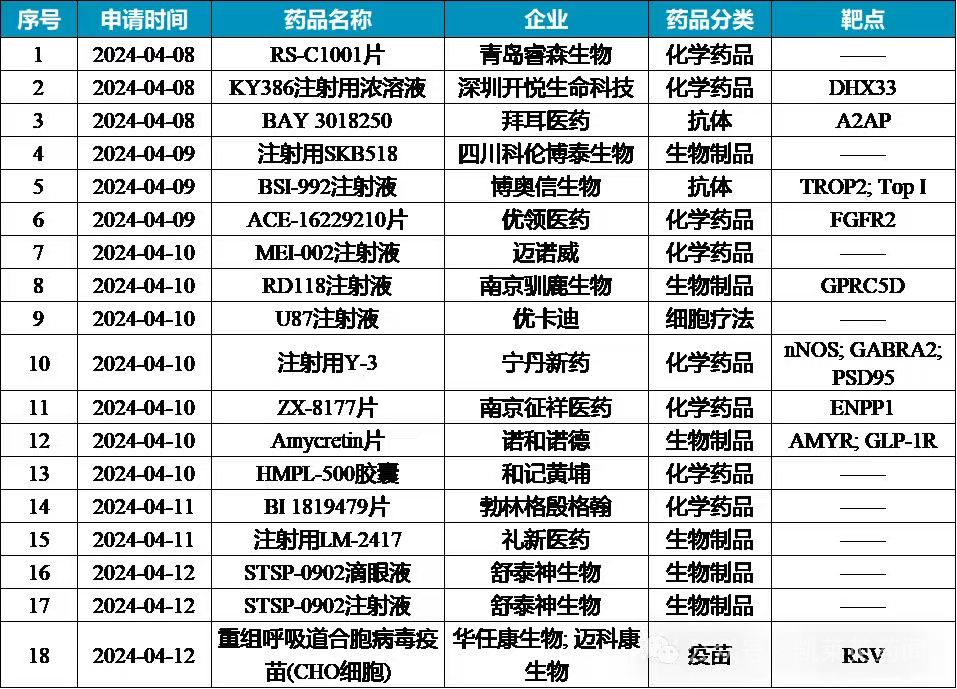
1、博奥信生物:BSI-992注射液
作用机制:靶向TROP2 ADC
适应症:肿瘤
4月9日,博奥信生物的BSI-992注射液的临床试验申请(IND)获CDE受理。BSI-992(OBI-992)是以TROP2为靶点所设计的ADC,以连接子(linker)将抗体和强效的TOP1(topoisomerase I)抑制剂相结合,这个独特的连接子具有高度亲水性,必须由癌细胞内的酶裂解,从而释放药物。BSI-992在血液中维持稳定,一旦与癌细胞表面的TROP2结合内吞,就会在癌细胞内释放小分子药物,毒杀癌细胞。多种动物模型已经充分显示,OBI-992(BSI-992)具有高效的抗肿瘤活性,优异的药代动力学表现,和良好的安全性。
2021年12月,博奥信生物将BSI-992授权给OBI Pharma,OBI负责ADC构建、研发,并拥有中国大陆、香港、澳门以外的商业化权利。美国FDA已于2024年1月批准OBI-992的IND申请,并将于今年第二季展开1/2临床试验以评估安全性与疗效。
2、优领医药:ACE-16229210片
作用机制:FGFR2抑制剂
适应症:肿瘤
4月9日,优领医药的ACE-16229210片的IND获CDE受理。ACE-16229210是新一代的高选择性FGFR2抑制剂,FGFR2 是一个经过临床验证的靶标,在许多实体瘤中经常发生改变。FGFR2基因扩增发生在4-10%的胃癌中;FGFR2 突变或融合发生在大约 10% 的子宫内膜癌和 15% 的肝内胆管癌中。在临床前的毒理实验中,ACE-16229210表现出极大的安全窗口;除了针对FGFR2重排和扩增异常具有高活性之外,它还保持了针对门控突变(V564F/L/I)和分子制动突变(N549K/D/H)的高抑制活性以克服此类突变带来的耐药,从而扩大了适用人群。此外,在多种肿瘤动物模型(胆管癌,乳腺癌,胃癌等)中展现了强大的单药及联合用药(Irinotecan/Fulvestrant)活性,结合其出色的安全性,有望被开发为针对FGFR2 驱动的癌症的更优的治疗选择。
3、驯鹿生物:RD118注射液
作用机制:靶向GPRC5D CAR-T
适应症:多发性骨髓瘤或淋巴瘤
4月10日,驯鹿生物的RD118注射液的IND获CDE受理。RD118是一款靶向GPRC5D靶点的CAR-T疗法。GPRC5D在正常人体组织中表达较低,但在多发性骨髓瘤浆细胞表面特异性过表达,是继BCMA之后第二个治疗多发性骨髓瘤治疗的潜在靶点。
4、优卡迪:U87注射液
作用机制:——
适应症:肿瘤
4月10日,优卡迪的U87注射液的IND获CDE受理。U87是一种CAR-T细胞疗法,通过筛选大量sCFv,找到了具有高亲和力和特异性的候选分子。在前期临床试验中,治疗组的患者展现出比对照组更好的疗效和生存期延长,显示了U87注射液的巨大潜力。
5、宁丹新药:注射用Y-3
作用机制:非肽类PSD95-nNOS解偶联剂
适应症:卒中
4月10日,宁丹新药的注射用Y-3的IND获CDE受理。Y-3的作用机制为解离PSD-95和nNOS偶联和激动α2-GABAA受体,药效明确,安全性良好,药代性质稳定,能够透过血脑屏障,无被纤溶酶降解的风险,能够克服Nerinetide临床缺陷便于与溶栓药物联用,未来临床治疗限制小,有可能让更多患者获益;同时由于Y-3具有快速抗焦虑和抗抑郁的作用,可兼顾急性脑卒中保护和卒中后情感障碍改善,更加有利于患者的预后。
临床前药效研究表明,Y-3对大鼠急性脑缺血损伤具有显著的保护作用,量效关系明确。Y-3用药3天即能显著改善脑缺血动物远期感觉运动功能和学习记忆能力,并减小脑损伤范围。Y-3单次用药可快速产生显著抗焦虑和抗抑郁的效果。同时,该产品安全性良好,动物最大无毒反应剂量与药效剂量暴露量相差140倍。
2023年8月,宁丹新药与康哲药业全资附属公司就Y-3注射液签约,康哲药业获得Y-3注射液在中国大陆、香港特别行政区、澳门特别行政区的独家推广权。
6、诺和诺德:Amycretin片
作用机制:AMYR和GLP-1R共激动剂
适应症:减重
4月10日,诺和诺德的Amycretin片的IND获CDE受理。Amycretin是诺和诺德开发的一款口服GLP-1受体和胰淀素受体的长效共激动剂,为新一代减重疗法,正在开发皮下注射(每周一次)和口服(每天一次)两种剂型,目前拟开发适应症为肥胖。
小型1期试验显示,患者在接受amycretin治疗12周后,其体重下降幅度达13.1%,而安慰剂组患者的体重下降幅度仅为1.1%。此外,药物展现出良好的药代动力学特性,与目前所开发的GLP-1类疗法具有相似的安全性、耐受性以及不良反应。
7、迈科康生物:重组呼吸道合胞病毒疫苗(CHO细胞)
作用机制:——
适应症:RSV感染
4月12日,迈科康生物的重组呼吸道合胞病毒疫苗(CHO细胞) 的IND获CDE受理。迈科康生物的重组呼吸道合胞病毒疫苗(CHO细胞)包含重组呼吸道合胞病毒融合前F蛋白(Pre-F)三聚体抗原和迈科康生物自主研发的佐剂系统,可诱导机体产生高水平的体液免疫应答及细胞免疫应答,在动物攻毒模型中展现出良好的保护效果及安全性。该疫苗是首款获CDE正式受理的采用重组蛋白技术路线的国产RSV疫苗。迈科康生物针对传染性及肿瘤领域布局了多样化的产品研发管线,包括多个针对重大传染病的预防性疫苗,以及HPV感染、癌症等领域的治疗性疫苗;截止目前,已有2款产品进入临床试验II期阶段。
国内创新药NDA汇总
1、长春高新/金赛:注射用金纳单抗
作用机制:IL-1β单抗
适应症:炎症疾病
4月11日,长春高新子公司金赛药业的注射用金纳单抗的上市申请获CDE受理。金纳单抗是通过基因工程技术等进行生产的抗白介素-1β(IL-1β)抗体药物。IL-1β以快速和特异性地阻断IL-1β与其受体的结合,从而阻断炎症发生。目前,金纳单抗正针对急性痛风性关节炎、全身型幼年特发性关节炎及间质性肺病等适应症展开研究。针对急性痛风性关节炎的 III 期临床数据显示,该药物能够有效缓解患者疼痛,并可显著降低复发风险。
2、Recordati:注射用双羟萘酸帕瑞肽微球
作用机制:生长抑素类似物
适应症:肢端肥大症
4月11日,Recordati的注射用双羟萘酸帕瑞肽微球的上市申请获CDE受理,拟用于治疗无法手术或手术后未治愈和通过另一种生长抑素类似物治疗控制不佳的成人肢端肥大症患者。帕瑞肽属于为第二代生长抑素类似物(SRL),是一款长效帕瑞肽产品,通过将生长抑素受体(SST)的4个合成氨基酸和两个必需氨基酸掺入新型环六肽结构中而产生的;与第一代SRL相比,长效帕瑞肽增强了生长抑素受体(SSTR)的结合谱,即对SSTR1、2、3和SSTR5亚型具有高亲和力,尤其对SSTR5的亲和力最高,具有更好的临床和生化控制率,且安全性良好。除此以外,该药物采用了微球制剂,不仅实现了长效缓释,也使其具有了良好的安全性。
该药物于2014年相继获EMA和FDA 批准治疗成人肢端肥大症患者。肢端肥大症是一种起病隐匿的慢性进展性内分泌代谢性疾病,患者的临床表现多为生长激素(GH)、胰岛素样生长因子-1(IGF-1)长期过度分泌所致,并伴有心血管并发症、糖脂代谢并发症、呼吸系统并发症、骨和骨关节系统并发症、神经系统并发症和肿瘤相关并发症等。临床上约95%的患者是由分泌GH的垂体瘤引起的,少数情况下是由垂体增生、GH或促生长激素释放激素(GHRH)的异位分泌引起;SRL是治疗肢端肥大症最有效的药物,其能够使得多数患者达到生化和临床症状的控制,控制肿瘤的生长及减小肿瘤的体积,改善与肢端肥大症相关的心脏、呼吸系统的并发症。
国内创新药上市获批
1、智核生物:人促甲状腺素注射液
作用机制:——
适应症:分化型甲状腺癌
4月11日,智核生物的人促甲状腺素(研发代号为SNA001/KN040)注射液的上市申请获NMPA批准,用于无远处转移分化型甲状腺癌患者在甲状腺全切或近全切术后碘[131I]清除残余甲状腺组织的治疗。SNA001为国内首个上市的重组人促甲状腺激素(rhTSH),是一种与人体内垂体分泌的促甲状腺激素(TSH)为同类糖蛋白,可在首次注射48小时内100%快速提升患者体内促甲状腺激素水平,促进碘摄取和有机化,便于分化型甲状腺癌患者快速接受碘治疗;此外,rhTSH能够刺激体内残留的甲状腺组织或转移灶分泌甲状腺球蛋白,便于诊断及监测疾病进展。
2018年早期临床试验研究显示,该药物不良反应轻微,安全耐受性良好。2019年12月起,智核生物的人促甲状腺素注射液在全国19家研究中心开展III期临床试验,累计纳入受试者307例,结果显示,其疗效非劣效于目前临床实践中常用且唯一的停服甲状腺素法,SNA001组体内促甲状腺激素水平3天内即达标,明显快于甲状腺激素撤退(THW)组;且安全耐受性良好,有效降低不良反应发生率,具有明确的临床需求和价值。
据悉,重组人促甲状腺激素最早于1998年在美国上市,由健赞Genzyme公司生产,目前已在包括中国台湾和香港的60多个国家和地区销售,但未进入大陆市场。此次智核生物人促甲状腺素注射液的上市将填补中国大陆该领域用药空白。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..