近日,BridgeBio Pharma公司宣布已向美国FDA提交了acoramidis用于治疗伴有心肌病的转甲状腺素蛋白介导的淀粉样变性(ATTR-CM)患者的新药申请(NDA)。该申请是基于关键性试验ATTRibute-CM的积极结果提出的,ATTRibute-CM是BridgeBio公司的一项3期研究,旨在评估acoramidis的疗效和安全性。
BridgeBio在今年7月宣布ATTRibute-CM试验获得了积极的顶线结果。该究第30个月的临床结果包括:
主要终点获得具有高度统计学显著性的改善(分层分析优先顺序为:全因死亡率,然后为心血管疾病相关住院频率,然后为N末端脑钠肽前体自基线的变化,然后为6分钟步行距离自基线的变化),Win比率(Win ratio)为1.8(p<0.0001)。与既往转甲状腺素蛋白(TTR)稳定剂试验观察到的结果不同的是,在30个月时,在所有预定病患亚组中观察到了降低心血管相关住院风险的一致性。
治疗组和安慰剂组在全因死亡和心血管相关住院的首次发生所需时间曲线在第3个月开始分离,并持续到第30个月,风险比为0.645(p=0.0008)。
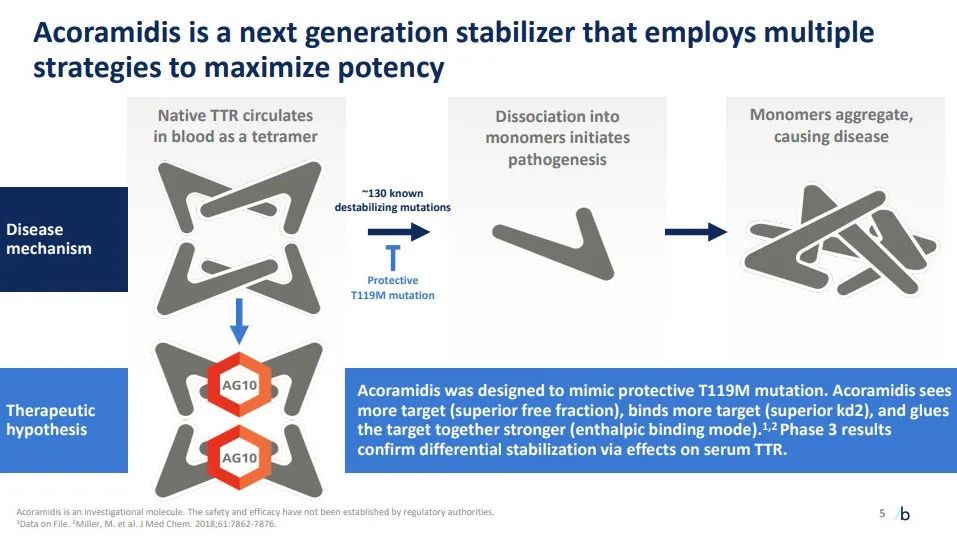
▲Acoramidis作用机制
值得注意的是,ATTRibute-CM的主动治疗组在30个月内的整体生存率为81%,这与美国数据库中年龄相匹配的一般人口的生存率(85%)相似。同时,acoramidis组的年化心血管相关住院率为0.29,与美国数据库报告的一般医疗保险人口的0.26相似。ATTRibute-CM的研究结果还显示,接受acoramidis治疗的患者在全因死亡率和心血管相关住院的复合终点方面可迅速获得临床获益。此外,acoramidis的耐受性良好,未发现潜在的安全信号。
Acoramidis是一款新一代、口服给药的高效TTR小分子稳定剂。它旨在模拟具有保护作用的TTR T119M突变的功能,维持TTR蛋白的正常四聚体构象,防止具有毒性的淀粉样蛋白的产生。
四川省医药保化品质量管理协会关于2026
各会员单位: 当前,制药行业正..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..