细胞和基因疗法(Cell and Gene Therapy, CGT)是继小分子、大分子靶向疗法之后的新一代精准疗法。
11月16日,CGT疗法迎来突破进展,Vertex Pharmaceuticals和CRISPR Therapeutics联合开发的全球首款CRISPR基因编辑疗法Casgevy在英国有条件获批上市,用于治疗镰状细胞病和输血依赖性β-地中海贫血。
放眼国内,据不完全统计,11月份共有14款CGT疗法IND获批,涉及万邦医药、星汉德生物、基因启明、可瑞生物、方拓生物、鼎新基因、百暨基因、上海医药等13家公司。
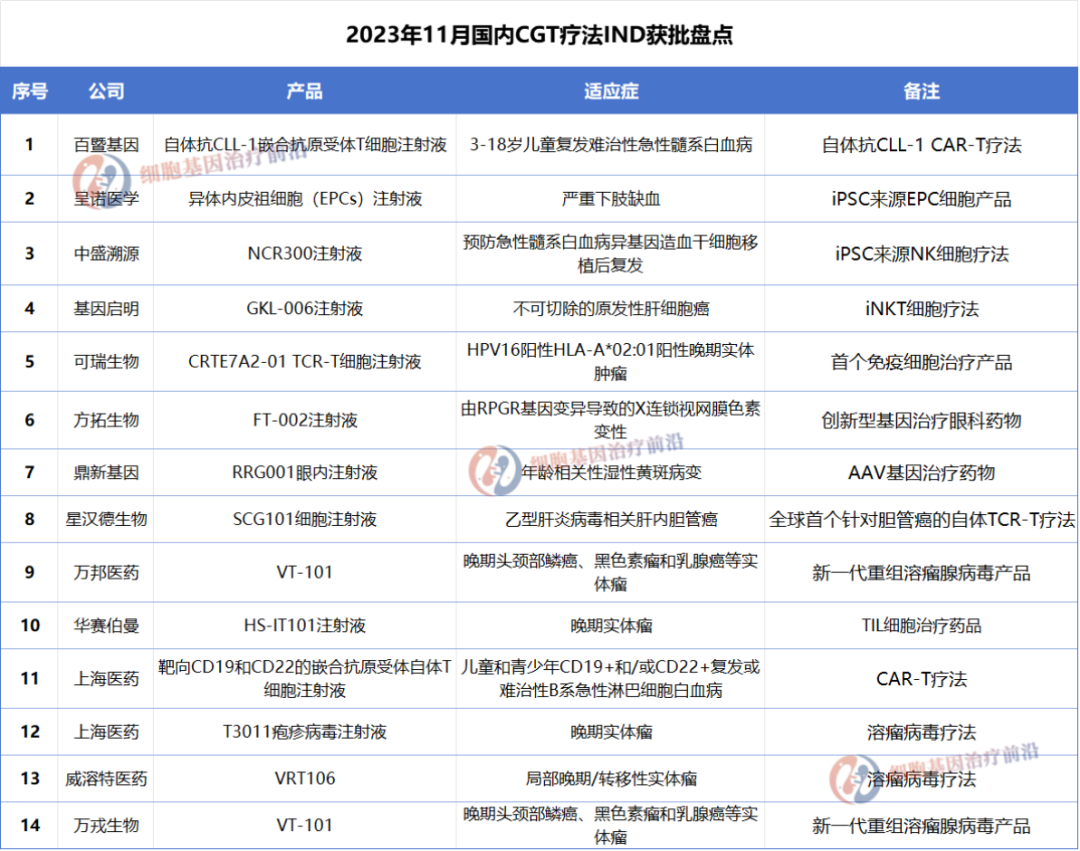
基因启明
11月21日,基因启明研发的GKL-006注射液获得临床试验默示许可,拟用于治疗不可切除的原发性肝细胞癌。GKL-006注射液是一款iNKT细胞疗法。
可瑞生物
11月21日,可瑞生物首个免疫细胞治疗产品CRTE7A2-01 TCR-T细胞注射液获得临床试验批准通知书,这标志着可瑞生物正式迈向注册临床试验的开展阶段。
方拓生物
11月6日,方拓生物自主研发的创新型基因治疗药物FT-002注射液获CDE临床试验许可,拟治疗由RPGR基因变异导致的 X连锁视网膜色素变性(XLRP)患者。
目前全球尚未有一款有效治疗XLRP的药物上市,FT-002注射液是中国XLRP治疗领域首个获得CDE临床试验许可及开展人体试验的基因治疗药物。
星汉德生物
近日,星汉德生物SCG101细胞注射液获得中国国家药监局临床试验默示许可,用于治疗乙型肝炎病毒相关肝内胆管癌。
SCG101注射液是一款全球首创(First in class)的自体TCR-T细胞治疗产品,为全球首个针对胆管癌的细胞疗法。
万邦医药
值得注意的是,复星医药控股子公司万邦医药控股子公司自主研发的 VT-101注射液已分别获国家药品监督管理局和美国 FDA关于同意该新药用于治疗晚期头颈部鳞癌、黑色素瘤和乳腺癌等实体瘤的临床试验批准。
该药是一款具有三重肿瘤靶向调控机制、三个病毒结构基因改造、三种血清型腺病毒嵌合、三类抗癌免疫基因装载的新一代重组溶瘤腺病毒产品。截至 2023 年 10 月,复星医药集团现阶段针对该新药的累计研发投入约 5,450 万元。
除此之外,11月份还有10款CGT疗法IND已获受理,涉及华夏英泰、先博生物、中因科技、达博生物、舶望制药、金唯科生物、易慕峰、茵冠生物10家公司。
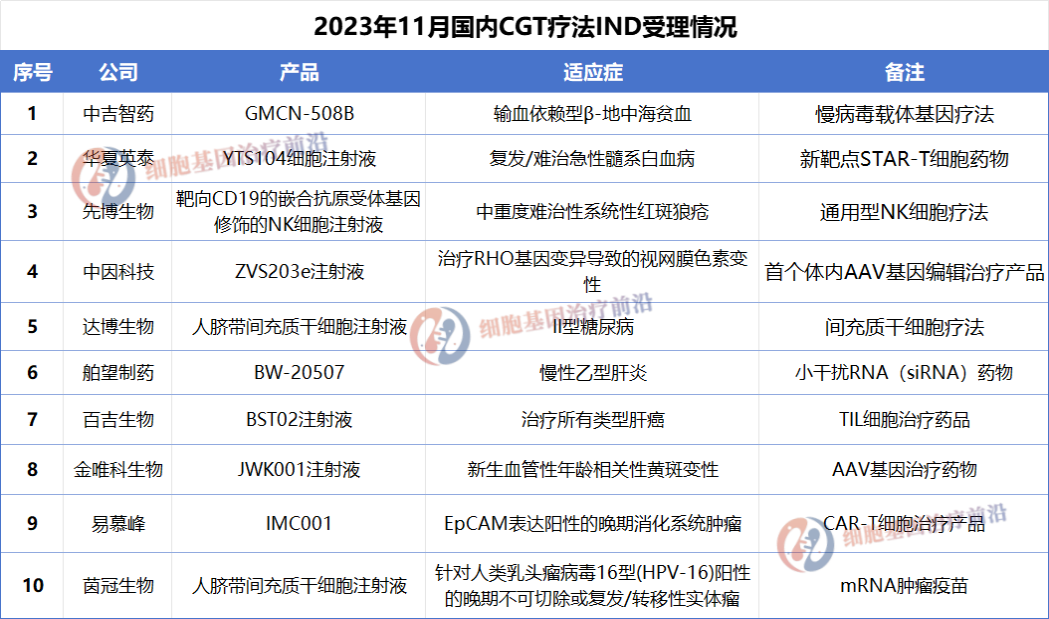
其中,华夏英泰的“YTS104细胞注射液”,作为华夏英泰探索血液瘤新靶点的STAR-T细胞药物,为治疗急性髓系白血病等适应症带来了崭新的希望。而中因科技的基因编辑治疗药物ZVS203e注射液是国内受理的首个体内AAV基因编辑治疗产品,用于治疗RHO基因变异导致的视网膜色素变性。
关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..