默沙东(MSD)公司今日宣布,重磅PD-1抑制剂Keytruda,在治疗可切除的Ⅱ期,ⅢA期或ⅢB期非小细胞肺癌(NSCLC)患者的关键性3期临床试验KEYNOTE-671中达到总生存期(OS)的主要终点。Keytruda与化疗联用作为术前新辅助治疗,并在手术后单药作为辅助治疗,与安慰剂与化疗联用作为新辅助治疗,加术后安慰剂辅助治疗相比,为OS带来统计显著并具有临床意义的改善。新闻稿指出,这是在这类患者中“首个”显示统计显著OS获益的3期临床试验。
默沙东此前已经基于无事件生存期(EFS)数据向美国FDA递交了补充生物制品许可申请(sBLA),预计在10月16日前获得审评结果。
肺癌是最常见的癌症类型之一,也是癌症死亡的主要原因。仅在2020年,全球肺癌确诊人数超过220万人,并造成超过180万人死亡。肺癌可大致分为NSCLC和小细胞肺癌(SCLC)两大类,其中NSCLC是最高发的肺癌类型,约占肺癌病例81%。约44% NSCLC患者在确诊时已是晚期。
Keytruda是一种人源化的抗PD-1单克隆抗体,可以阻断PD-1与其配体PD-L1、PD-L2的结合,进而激活T淋巴细胞。此作用可能增强体内免疫系统侦测与抵抗肿瘤细胞的能力。2014年9月,Keytruda首次获美国FDA批准治疗晚期黑色素瘤,并在后续获批作为一线疗法治疗转移性NSCLC患者。在中国,Keytruda也已获批多项适应证,涵盖黑色素瘤、NSCLC、头颈部鳞状细胞癌、结直肠癌、食管癌与肝细胞癌等。
此前在KEYNOTE-671试验的第一次期中分析中,基于Keytruda的围手术治疗方案与对照组相比,显著提高了患者的EFS,减少疾病复发,进展或死亡的风险42%(HR=0.58,[95% CI,0.46-0.72],p<0.00001)。接受基于Keytruda治疗方案的患者,中位EFS尚未达到(95% CI,34.1-NR),接受单独化疗的患者的EFS为17个月(95% CI,14.3-22)。
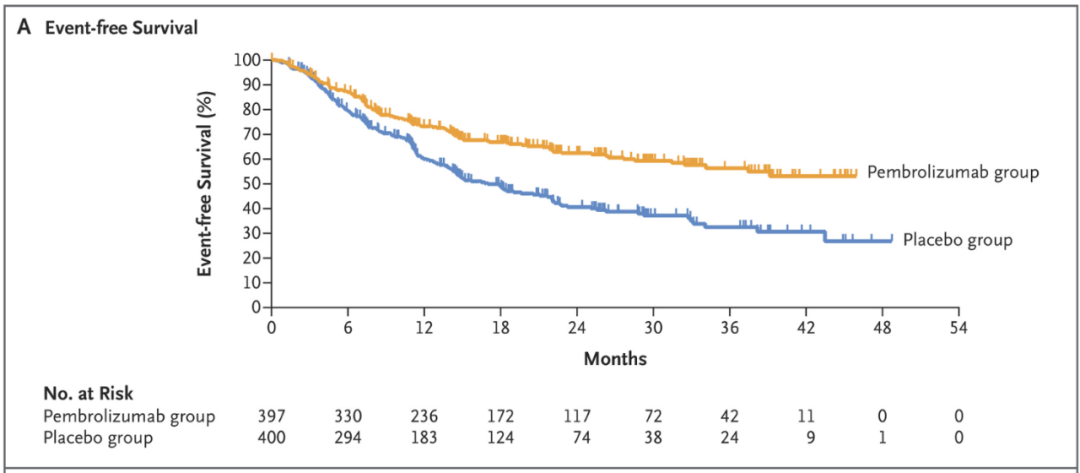
▲KEYNOTE-671试验的无事件生存期结果(图片来源:参考资料[2])
参考资料:
[1] Merck Announces Pivotal KEYNOTE-671 Trial Meets Dual Primary Endpoint of Overall Survival (OS) in Resectable Stage II, IIIA or IIIB Non-Small Cell Lung Cancer (NSCLC). Retrieved October 10, 2023, from https://www.merck.com/news/merck-announces-pivotal-keynote-671-trial-meets-dual-primary-endpoint-of-overall-survival-os-in-resectable-stage-ii-iiia-or-iiib-non-small-cell-lung-cancer-nsclc/
[2] Wakelee et al., (2023). Perioperative Pembrolizumab for Early-Stage Non–Small-Cell Lung Cancer. NEJM, DOI: 10.1056/NEJMoa2302983
四川省医药保化品质量管理协会关于2026
各会员单位: 当前,制药行业正..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..