今年8月4日,美国食品药品监督管理局(FDA)批准Sage Therapeutics/渤健公司合作开发的Zurzuvae(zuranolone胶囊),成为该机构批准的首款产后抑郁症(PPD)口服治疗药物。
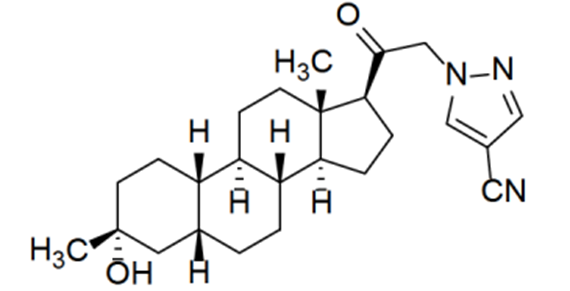
▲图1 zuranolone结构式
尽管2019年FDA批准了史上第一款专门用于治疗产后抑郁症的药物Zulresso(brexanolone注射液),亦由Sage Therapeutics开发。不过该药须通过60小时(2.5天)的连续静脉输液,需要多次调整剂量,而且治疗费用昂贵(每瓶售价7854.35美元),市场推广遇到巨大困难。
Zurzuvae每天一次口服给药,疗程为14天,可以快速改善PPD女性的抑郁症状。
Zurzuvae的批准,被认为是开创了产后抑郁症治疗新的局面。
笔者通过检索,Zurzuvae中国专利布局如下:
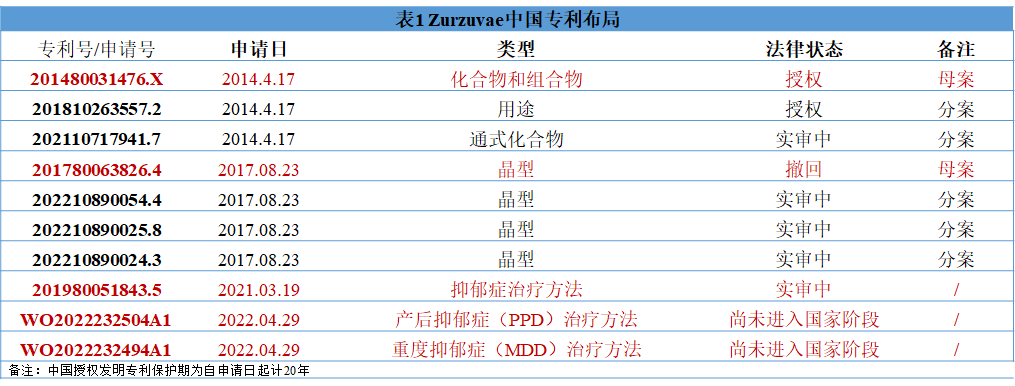
化合物和用途专利
萨奇治疗股份有限公司(Sage Therapeutics)于2014年4月17日提交国际申请(公布号为WO2014169833A1),进入中国后权利要求经过修改,2018年4月27日首先获得授权专利201480031476.X保护了zuranolone化合物结构和其组合物。
萨奇治疗股份有限公司2018年3月28日基于201480031476.X提交了分案申请,并于2021年7月13日获得授权(专利号为201810263557.2),该分案申请专利保护了zuranolone的医学用途。
萨奇治疗股份有限公司2021年6月28日通过“二次分案”(申请号为202110717941.7)保护了通式化合物,目前处于实审中。
晶型专利
萨奇治疗股份有限公司于2018年3月1日提交了国际申请(公布号为WO2018039378A1),专利(申请号为201780063826.4)进入中国后因超过答复期限视为撤回(发文日为2022年9月2日)。
不过,萨奇治疗股份有限公司于2022年7月27日已基于201780063826.4提交了3件分案申请(202210890054.4、202210890025.8、202210890024.3),目前处于实审中。
其他专利
此外,萨奇治疗股份有限公司还申请了zuranolone治疗方法的专利,其中产后抑郁症(PPD)治疗方法专利尚未进入国家阶段。因治疗方法专利在中国不属于授权客体,答复审查意见时可能会通过修改权利要求以满足授权条件。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..