美国修订《药品法》,明确新药化合物是否新的判定准则
三周前,在美国华盛顿举行的食品药品法协会(FDLI)的年度大会上,FDA药品审评和研究中心(CDER)的资深法规律师Nisha Shah介绍了过去几年中对《药品法》的几项修订。其中之一是如何判断新药可否获得专利过期后5年的专营期。具体讲就是,拜登总统于2021年4月签署了“确保创新法,Ensuring Innovation Act”,将《药品法》涉及专营期内容中的活性成分(active ingredient)的用词换成活性部位(active moiety)。
此事有两点值得注意:一是为何要改变用词,二是修订《药品法》的做法。
先来看为何要改变用词。《药品法》原来的说法是:若新药的活性成分(包含其任何脂和盐的成分),有别于任何已获批药品的活性成分,则获得5年的专营期。这个似乎相当明确的说法,其实有漏洞,而且这个漏洞让FDA输了法律官司。具体情况如下。
2004年11月,FDA批准了挪威Pronova公司源于天然产物的新药Lovaza,其主要成分是omega-3-酸乙酯,是含多种相似脂类成分的鱼油产品。其主要活性部位是下图中的二十碳五烯酸(EPA)。2012年7月,FDA批准了爱尔兰Amarin公司的新药VASCEPA,其活性成分是如下图所示的二十碳五乙酯(IPE),其活性部位就是EPA。
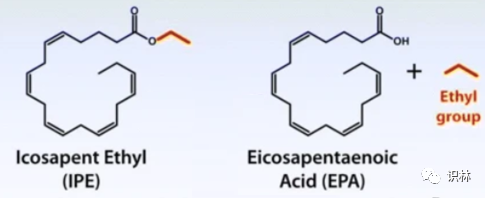
因两个新药的活性部位相同,FDA拒绝给予VASCEPA 5年的专营期。Amarin不服,将FDA告上法庭。2015年3月,联邦法官Randolph Moss判Amarin胜诉。2016年5月,FDA撤回拒绝的决定,给予VASCEPA 5年的专营期。这是自1984年仿制药立法以来,挑战FDA拒绝5年专营权的首次成功。
FDA败诉的原因之一是《药品法》中关于活性成分和活性部位在判定是否给予专营期上说法不明确,之二是FDA在批准Lovaza时,将多种相似脂类成分的总体作为活性成分,而未说活性成分所对应的活性部位就是EPA。修改后的《药品法》明确了专营期判断将基于药品活性部位,从而避免今后再发生上述官司。
再来看这个改变用词的药品法修订是如何做的。2021年2月24日参议院提出“确保创新法案”,3月10日参议院全票通过,4月14日众议院唱票通过(未投票表决,因为明显会以压倒多数通过),4月23日总统签署,法律生效。前后不到2个月。而且,法律的内容很简单,加上各种套话,总共才1000余字,重点说清在《药品法》中将哪些“活性成分”在字眼替换成“活性部位”。当然,前期的准备工作花时间是免不了的。此飞速精准修法,相当罕见,说明该项法律修订,广得人心。
作者:榆木疙瘩
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..