5月9日,蓝鸟生物公布2023年一季报,截至2023年3月31日,公司营收238.1万美元,同比增长22%;其中产品收入同比增长63%,达到230万美元。而研发费用支出为4614.4万美元,同比下降41%。值得注意的是,蓝鸟生物去年同期净亏损1.222亿美元,今年一季度转亏为盈,净利润达2124万美元。
图片
受此影响,蓝鸟生物股价上涨近13%,市值达到4.627亿美元。
蓝鸟生物共有3款基因疗法,其中2款已经进行商业化,另外1款已向美国FDA提交BLA,接下来,就让我们一起看看蓝鸟生物一季度基因疗法的业绩亮点:
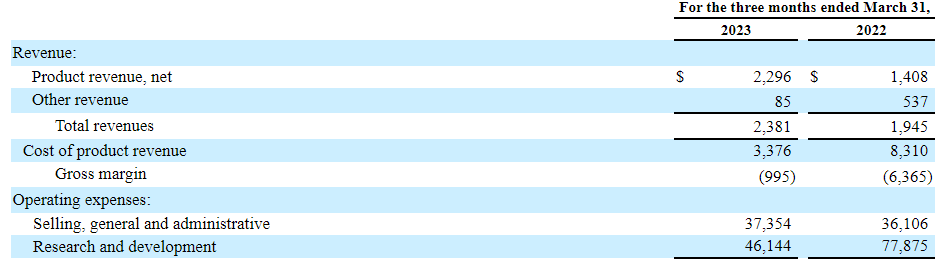
蓝鸟生物研发管线 来源:官网
lovo-cel (lovotibelogene autotemcel) BLA 已提交
lovo-cel作为蓝鸟生物的第三款基因疗法,4 月 24 日,蓝鸟生物宣布向美国食品和药物管理局(FDA) 提交 lovo-cel的生物制剂许可申请(BLA)申请,用于治疗镰状细胞病 (SCD) 患者。该公司已申请优先审查,FDA的审查时间将缩短至六个月,而标准审查时间为 10 个月。
如果获得批准,蓝鸟生物预计lovo-cel将于 2024 年初进行商业化。届时,大约有 20,000 名镰状细胞病患者(美国1/5的 SCD患者)有机会接受该基因治疗。
ZYNTEGLO ® (betibelogene autotemcel) 完成首例商业输注
迄今为止,已有6例患者开始使用ZYNTEGLO(细胞收集)。首个商业化ZYNTEGLO输注已完成,公司预计2023年第二季度将产生收入。付款人对ZYNTEGLO的接受度依然很高,迄今为止,该公司未收到任何拒绝案例;药品的事先授权批准保持不变,大约为两周。如此看来,患者启动率仍然是ZYNTEGLO上市第一年的关键商业指标。
SKYSONA®(elivaldogene autotemcel) 完成首例商业输注
SKYSONA的首次商业输液于2023年3月完成,总共完成了3例患者的细胞收集。自SKYSONA获批以来,蓝鸟生物已启动了3个合格的治疗中心(QTC),为肾上腺脑白质营养不良患者提供SKYSONA治疗。2023年,蓝鸟生物有可能在美国西海岸再增加2个QTC。
截至2023年3月31日,蓝鸟生物现金、现金等价物、有价证券和受限制的现金约为3.64亿美元,随着第三种基因疗法的商业化准备,预计2023年蓝鸟生物的现金支出将在2.7亿~3亿美元。根据目前运营计划,蓝鸟生物的现金跑到足以支撑到2024年底。
参考资料:
蓝鸟生物官网
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..