2021年全球杜氏肌营养不良症(DMD)市场为6.9334亿美元,预计到2028年将达到15.3372亿美元,预测期(2022-2028年)的复合年增长率超过11.87%。
目前,DMD的特点是渐进性的肌肉无力和萎缩,还没有治愈方法,大多数治疗方法只能提供有限的缓解。
根据SkyQuest的估计,DMD患者的数量在过去十年中增加了50%。这可能是由于医疗创新扩大了DMD的治疗范围,再加上公众对DMD患者的认识和宣传不断提高。
根据美国国立卫生研究院(NIH)的数据,美国每年有超过25万名DMD患者,推动了美国DMD的市场。虽然DMD患者仍然面临许多挑战,包括缺乏认识和研究资金,但NIH报告说,在过去几十年里,DMD的治疗方法已经有了明显的改善。目前正在努力寻找治疗DMD患者的新方法,推进对遗传学和治疗方案的研究。
由于DMD仍无法治愈,对开发能够帮助DMD患者活得更长、更健康的新型疗法的兴趣越来越大。
全球DMD市场对这些治疗方法的高度需求,导致了一些创新的新疗法被开发出来,以治疗这种疾病。一些最有前途的治疗方法侧重于修复和用健康的肌肉“替换”有缺陷的肌肉。这些疗法如基因疗法或细胞疗法,由于其有可能恢复患者的力量和活动能力,正变得越来越受欢迎。
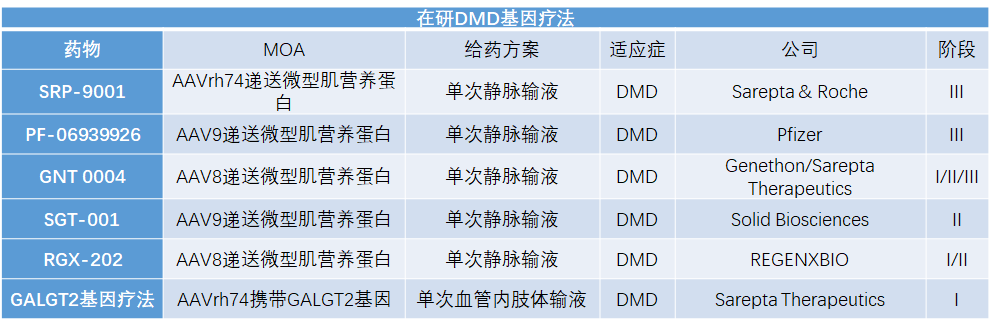
全球DMD市场最近的一项创新是基因疗法,使用病毒将纠正的基因副本输送到体内的细胞。这种方法有可能使一些DMD患者的症状得到长期缓解。然而,基因疗法仍处于早期阶段,关于其安全性和有效性还有许多未解之谜。
值得一提的是,DMD将迎来首款基因疗法。
SRP-9001是Sarepta公司用于治疗DMD的研究性基因疗法。2022年9月29日,Sarepta公司宣布已向美国食品药品管理局(FDA)提交了一份生物制品许可申请(BLA),要求加速批准SRP-9001,以治疗能走动DMD患者。
11月28日,Sarepta 公司宣布,FDA已接受该公司SRP-9001的生物制品许可证申请。SRP-9001已获得FDA的优先审查,监管行动日期为2023年5月29日。
此前的一项安慰剂对照的2期阶段研究未能显示出与安慰剂相比对患者的益处,这一结果使Sarseta寻求批准的计划推迟了一年多。
混合数据结果可能导致FDA召集一个外部专家小组来审查数据。Sarepta预计会召开这样一次会议,在此期间,外部专家可能会设法推迟药物的上市,直到3期阶段试验产生结果。而Sarepta获得一项确定的安慰剂对照3期阶段试验研究数据要延后几个月。不过这项试验可以作为一项“验证性”研究,如果是肯定的,将有助于将加速批准转变为完全批准。
不过,如果在5月29日前获得批准,Sarepta可能会领先其主要竞争对手辉瑞几个月甚至一年多。辉瑞的上市之路因临床试验中的安全问题而推迟。然而,3期阶段试验可能在2023年进行。假设结果是积极的,辉瑞预计将在明年年底前获得批准。
SRP-9001如果获得批准,将是DMD的第一个基因疗法。
另一个不断增长的研究领域是干细胞疗法。干细胞是可以无限期分裂的细胞,可用于修复组织损伤或创造新细胞。早期研究显示,干细胞疗法可能对受DMD影响的肌肉再生有效。然而,需要更多的临床研究来证实这些发现,并确定使用这种治疗的最佳方式。
治疗DMD也面临着许多挑战。
最明显的挑战是DMD是一种进行性疾病,这意味着疾病的严重程度会随着时间的推移慢慢增加。DMD的早期干预措施,如用于治疗其他形式的肌肉萎缩症,通常对治疗DMD患者并不有效。此外,由于DMD是一种遗传性疾病,目前还没有已知的治愈方法,也没有可靠的方法来减缓或阻止疾病的发展。
另一个关键的挑战是开发药物疗法,有效解决DMD的根本原因,而DMD通常是由遗传和环境因素共同造成的;寻找更好的方法来监测和跟踪病人的进展和结果;以及开发更有效的教育和宣传措施,以提高对该疾病的认识。
幸运的是,在全球杜兴氏肌肉萎缩症市场上有几种治疗方法,可以改善DMD患者的生活质量。这些治疗方法可以包括辅助呼吸装置、物理治疗和药物。然而,需要注意的是,这些治疗方法只能提供部分缓解,不一定能阻止疾病的发展。需要进行更多的研究来为DMD患者开发更有效的治疗方法。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..