测和需求计划中可变性的主要领域之一是新产品引入(NPI)。这可能会受到许多因素的影响,例如监管机构的后期查询、产品的需求概况等。还涉及许多相互竞争的因素,例如,计划全球发布时,每个国家/地区的注册流程都不同,何时批准发布的时间框架也不同。
然而,最重要的可变性领域可能是规划入站供应链的需求以支持生产要求。这通常是因为公司不知道它们将生产多少产品。此外,公司的商业和生产部门之间的规划讨论有时可能会脱节,从而导致NPI 的可变性。
与生产生物疗法相关的成本,包括细胞和基因疗法,通常是小分子产品的数百倍。对于生物仿制药,新产品的使用、驱动因素等存在巨大的不确定性。因此,引入新产品时的错误可能会很严重。挑战在于减少可变性,同时为市场生产正确的数量。
各国通常对如何批准产品有不同的标准。例如,有些可以在几个月内处理监管提交;而在其它情况下,可能需要两到三年。因此,公司必须正确规划他们计划在哪里推出新产品,并且必须与他们的商业和营销团队合作,以了解对这些国家现有产品的影响。因此,预测和需求计划对于推出新产品至关重要,尤其是其发布计划以及对何时需要完成、由谁完成等的理解程度。此过程的一部分是研究公司需要收集哪些信息来支持正在生产的新产品。
通常缺乏用于临床或上市供应的产品的基本数据包,并且在开发和业务功能之间没有“一组商定的数字”。这可能会导致几个问题,例如,产能和交货时间限制、供过于求以及变更评估和实施延迟。
在较好的情况下,这些可能会导致需要一定的“灭火”工作,而最坏的情况是,错过临床供应里程碑或延迟NPI 启动。供应商有效应对的能力可能会受到严重限制。
全面而稳健的 NPI 流程有很多好处,包括:
文件的标准化规划/跟踪
早期规划、数据收集和协作
捕捉每个阶段的风险
包括“创新”讨论的业务审查流程
为材料需求生成“生命周期”文件
步进式过程可用作引入材料以支持新原料药生产的指南,并可与详细的公司特定NPI 程序结合使用。我们在本文中描述的过程也是细胞和基因治疗制造商的相关最佳实践。
Part
1
阶段关卡(stage-gate)流程
材料供应过程包含贯穿早期到晚期临床阶段的许多共同要求。每个阶段都固有的是“生命周期材料战略”的持续发展,该战略记录了每个阶段的关键行动、决策和材料需求等信息。因此,在这个基于风险的过程中,要求供应商尽早合作是至关重要的。
为了支持每个阶段关卡的交付,使用以下结构:
输入 - 支持阶段关卡交付的文档/参与功能的集合。
流程 - 需要交付的任务。
输出 - 完成关闭阶段关卡的可交付成果。
阶段关卡流程正式将材料引入和供应流程分为4个不同的阶段,它们是:
建立产品生命周期材料要求
材料评估
供应商选择和资质确认
制造和业务审查
这一过程将帮助公司进行成功规划,并考虑诸如在产品生命周期内提供适当数量的原材料以及将如何与供应基地合作、以确保两者能够以相同的速度增长等问题。
它应该在开发过程和 3 期试验结束时使用。这一点很关键,因为公司通常没有花足够的时间与开发团队一起规划新产品,也没有考虑一旦产品成为商业实体,生产流程将如何运作。
这个过程将支持参与新产品周期的团队,并帮助他们考虑整个过程的管理 -从了解供应链和产品如何进入市场到他们需要进行什么样的对话。
Part
2
阶段关卡 - 建立产品生命周期材料要求
当大量公司资源致力于产品开发时,这个阶段可能会开始,例如,首次人体(FTIH) 研究。它是对支持引入原料药供应的材料的基本数据要求进行整理,并对整个产品开发和商业生命周期的预测进行评估的时间点(见图 1)。
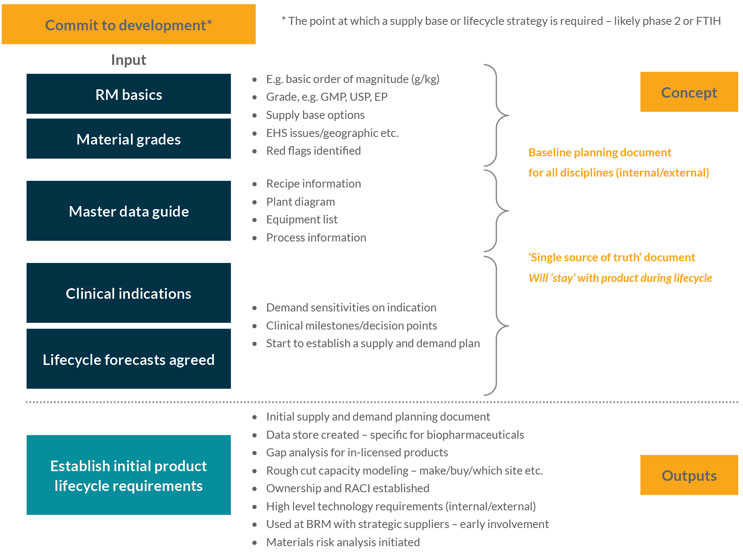
图 1:建立产品生命周期材料要求
Part
3
阶段关卡 – 材料评估
此阶段的重点是准备好从供应商群中收集信息。使用来自产品开发团队的技术数据,该阶段向供应商发起关于材料的正式信息请求(RFI),这些供应商最终可能会支持全部生产量。该阶段试图确保供应链对这些材料具有弹性,并且供应商可以支持产品在其生命周期内的预测或拟议增长(参见图 2)。
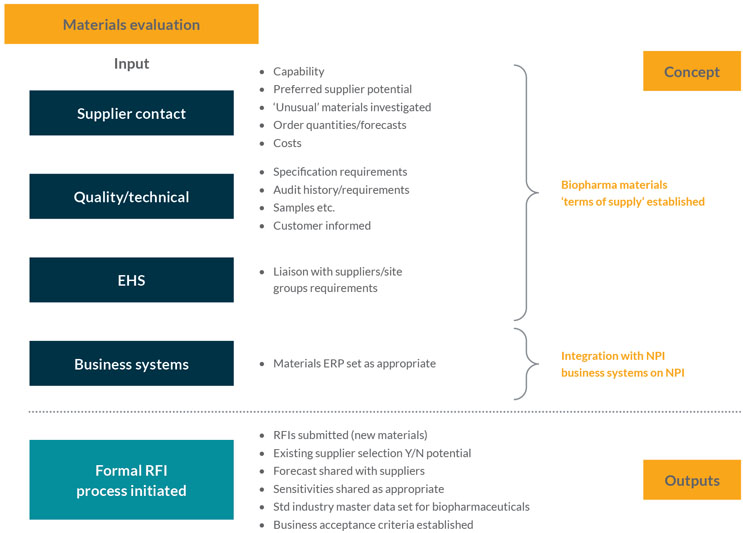
图 2:材料评估
Part
4
阶段关卡– 供应商选择和资质确认
这一阶段的重点是确保与供应商的材料供应协议,是应考虑供应链弹性和稳健性战略的地方。它评估来自供应商的RFI 信息(在第 2 阶段收集),并开始制定供应链弹性战略方法,其中包括关键材料的双重和二级采购等行动。该团队还应与供应商的QA 组织合作,考虑制定审核或资质确认策略,并使用 Rx-360 Joint Audit Program等设施(参见图 3)。
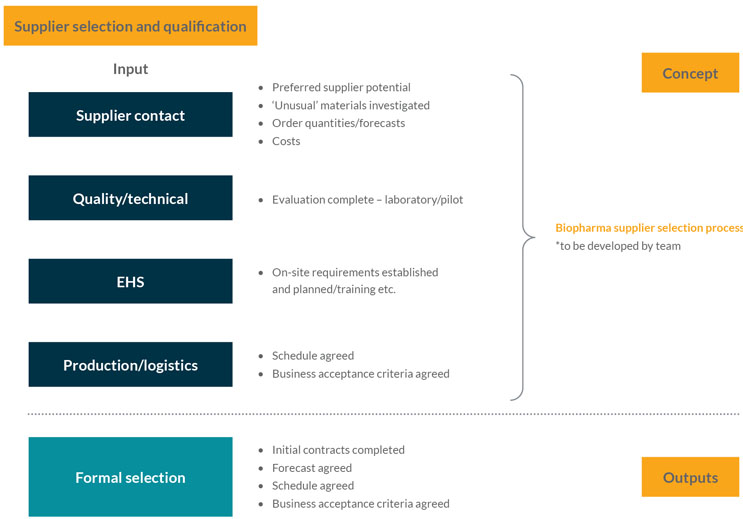
图 3:供应商选择和资质确认
Part
5
阶段关卡 – 制造和业务审查
此阶段是对支持生产过程的原材料供应链的运营绩效审查。它收集相关的绩效指标,例如材料是否按时、完整等。它旨在确保监控和管理任何趋势或未来问题,以便正确设计入站供应链并确保平稳一致的供应(见图 4)。
反馈回路在此过程中至关重要。该阶段评估供应历史并调查任何问题的细节,例如,20批中有2批被延迟。它会询问诸如“延迟的原因是什么?”和“这是我们未来应该关注的事情吗?” 之类的问题。然后应与供应商讨论这些问题。

图 4:制造和业务审查
Part
6
结论
NPI 流程是从供应链中获取有关原材料的所有正确信息的最佳机会之一,以支持新产品在其生命周期内的开发。如果做得正确,它可以避免在产品的不同阶段发生问题时可能需要的追溯工作。因此,在与开发、制造、运营和质量团队合作时,确保NPI 取得成功是一项必不可少的风险缓解措施。
该流程可确保支持原材料使用所需的所有主数据信息都存在且正确无误,并且您可以通过稳健、有弹性的供应链来规划这些材料,该供应链支持为您的生产设施供应材料。
它是支持任何新产品推向市场的关键活动。大流行期间需求的变化很大,因此重要的是要知道您可以根据市场需求快速上下调整。因此,与您的供应商及其供应链共享信息至关重要,以便他们在向单一市场或全球推出新产品时了解您的需求和期望。
本文为以下文献内容简介,详细内容,请参考原文。
原文:BioPhorum, The Process Map To Ensure Biopharma Raw Materials Supply. Bioprocess Online, 2022.
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..