近日(10月6日),Allogene公司宣布,已启动同种异体CAR-T(AlloCAR T™)细胞疗法ALLO-501A用于治疗复发/难治性(r/r)大B细胞淋巴瘤(LBCL)的关键II期ALPHA2临床试验。这也是行业内同种异体CAR-T产品的首个潜在关键性II期试验。

该公司也在启动一项名为EXPAND的临床试验,旨在评估ALLO-647对标准的氟达拉滨/环磷酰胺淋巴耗竭方案的贡献。如果获得积极结果,该公司希望这些研究能够支持ALLO-501A和ALLO-647的监管批准。
ALL-501A是一种经基因工程改造、靶向CD19的AlloCAR-T产品,通过改造,患者可使用健康捐赠者的T细胞,并可减少自身的免疫排斥反应。ALLO-647是Allogene开发的抗CD52单抗,旨在抑制宿主免疫系统并允许AlloCAR-T产品继续扩增,以达到充分的治疗效果。今年6月,美国FDA授予ALL-501A治疗r/r LBCL的再生医学先进疗法认定(RMAT)。
这项单臂II期ALPHA2试验将在r/r LBCL患者中单次输入含1.2亿CAR-T细胞的ALLO-501A。在输注ALLO-501A之前,受试者将接受FCA90淋巴细胞耗竭方案(氟达拉滨+环磷酰胺+ALLO-647)预处理。该试验将招募大约100名患者,这些患者之前至少接受过两种治疗方案,且没有接受过抗CD19治疗。主要终点为客观缓解率(ORR)。
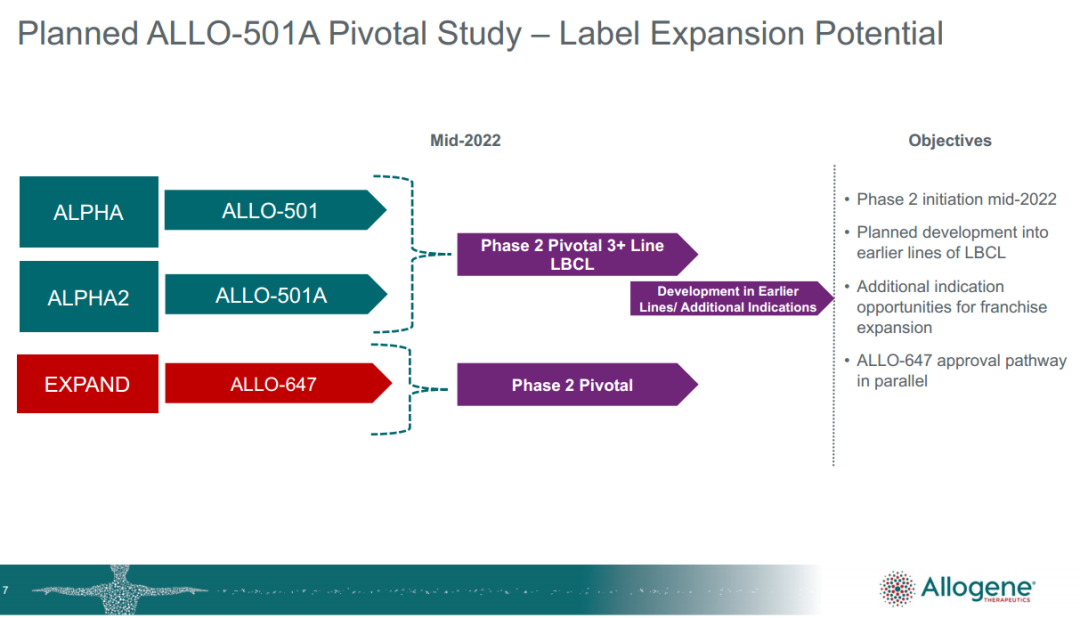
EXPAND试验是ALLO-647潜在的单独注册试验,预期入组约70例 r/r LBCL 患者,旨在证明ALLO-647的安全性及其对淋巴细胞耗竭方案总体有效性的贡献。患者将随机接受与ALPHA2试验相同的单剂1.2亿个细胞剂量ALLO-501A,以及标准淋巴细胞耗竭方案(对照组)或与ALPHA2试验相同的FCA90淋巴细胞耗竭方案(活性药物组)。
“我们自豪地启动了同种异体CAR-T产品的行业首个潜在关键性II期试验。这一里程碑为ALLO-501A和我们更广泛的创新产品管线铺平了道路,有可能大大增加患者获得细胞治疗的机会。”Allogene的总裁兼首席执行官兼联合创始人David Chang医学博士说。“这是多年辛勤工作和坚持不懈的结果,是我们敬业的工作人员、研究者、临床试验中心协调员、监管机构以及参与我们研究的患者合作共同完成的。”
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..