近年来,国内制药企业在实施创新药走出去战略的同时,也在不断加大项目的License-in(许可引进),以快速补充内部研发管线,不过,License-in项目同样面临着高风险!
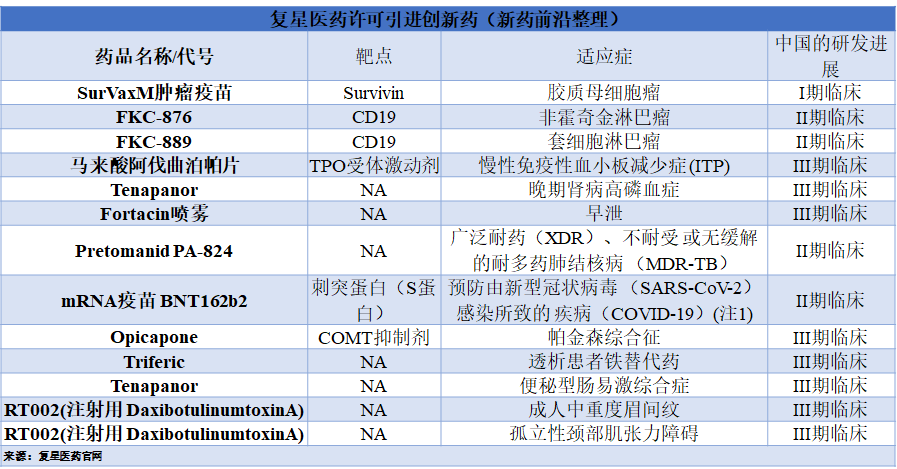
近日,复星医药官网更新了其研发管线,根据新药前沿微信公众号跟踪的数据显示,与公司官网2021年6月30日公开的信息相比,复星医药研发管线中许可引进创新药有多项重大变动(其中涉及2款新药从更新后研发管线踢除,1款新药上市申请遭拒)。
Balixafortide是Polyphor(基于由苏黎世大学授权的专利)研发的一款强效、 高选择性 CXCR4 拮抗剂。
2020年8月,复星医药控股子公司Fosun Pharma AG与Polyphor签署许可协议,Polyphor授权Fosun Pharma AG在区域内及领域内使用其专利、专有技术及改进独家临床开发及商业化Balixafortide以及相关产品/组合。根据协议,Fosun Pharma AG向Polyphor支付1500万美元的首付款和最高1900万美元的临床开发注册里程碑付款,在Balixafortide启动商业化销售后,Fosun Pharma AG将根据其年度净销售额达成情况向Polyphor支付至多1.48亿美元的销售里程碑款项,以及12%-16%不等的销售提成。
2021年6月10日,上海复星医药控股子公司上海复星医药产业发展有限公司收到国家药品监督管理局关于同意该集团获许可的Balixafortide用于与艾立布林联合治疗HER2阴性、局部复发或转移性乳腺癌开展临床试验的批准。复星医药产业拟于条件具备后于中国境内开展该新药的临床试验。截至2021年5月,复星医药现阶段针对该新药累计研发投入按2021年5月31日中国人民银行公布的汇率中间价折合人民币约9646万元。
不幸的是,2021年6月28日,PolyphorAG宣布Balixafortide与艾日布林联合治疗HER2阴性、局部复发或转移性乳腺癌的全球Ⅲ期临床失败。
2017年9月6日,复星医药公告称,控股子公司上海复星医药产业发展有限公司获得美国Palatin Technologies公司许可,获得其肽类药物Bremelanotide(包括原料、药物制剂和药物递送装置)在中国(包括大陆、台湾、香港及澳门特别行政区)的独家商业化和非独家开发、制造权利,以及为了区域内的开发和商业化之目的,在区域外非独家制造产品的权利。
根据协议,复星将向Palatin支付500万美元首付款,750万美元国内注册里程金(CFDA批准上市后支付),以及基于产品未来净销售额的里程金9250万美元和约定比例的销售提成。交易总额合计1.05亿美元。
Bremelanotide是一款黑素皮质素受体-4(MC4r)激动剂,通过激活大脑中的内源性途径来调节性欲和性反应,帮助伴有低活跃性性欲障碍况的绝经前女性保持正常性欲。
2019年4月,Bremelanotide注射液用于治疗机能减退女性性欲障碍(HSDD)获国家药品监督管理局临床试验注册审评受理。
2019年6月,复星医药合作伙伴Palatin Technologies的Bremelanotide在美国获得批准上市,商品名为Vyleesi。值得一提的是,在之前的一项研究中注意到动态血压的短暂升高后,FDA希望看到Vyleesi每天给药对血压的影响,这一要求将其决定日期推迟了三个月。尽管获得批准,FDA限制该药物在心血管疾病高风险人群中的使用,并要求患者每月用量不超过八剂。
不过Balixafortide和Bremelanotide注射液2个项目在国内都处于临床试验早期阶段。
奥匹卡朋胶囊上市申请遭拒
奥匹卡朋胶囊(opicapone)是一种长效、第三代COMT抑制剂。由葡萄牙Bial-Portela(Bial-Portela & Ca, S.A.)公司开发。
复星医药子公司江苏万邦生化医药集团有限责任公司在2018年1月9日与Bial达成协议,引进Ongentys的中国大陆开发权益(不包括港澳台),交易包括250万美元首付款和1250万美元里程金。
奥匹卡朋胶囊最早于2016年6月首次获欧盟批准,作为左旋多巴/多巴脱羧酶抑制剂(DDCI,如卡比多巴)的辅助疗法,以治疗出现剂末现象不能稳定控制运动症状帕金森病患者,商品名为Ongentys 。奥匹卡朋分别于2020年4月、2020年6月在美国、日本获批上市,在美国获批用于辅助左旋多巴/卡比多巴治疗出现“开‐关”现象帕金森病患者。
2021年3月10日,奥匹卡朋胶囊的进口上市注册申请获CDE受理(去年6月公司官网显示状态为“上市申请”)。NMPA于2022年03月21日发布药品通知件待领取信息,奥匹卡朋胶囊遭遇拒绝批准。不过,复星医药对该项目更新后的状态为“III期临床”。
另外,复星医药许可引进创新药新增2项研究:FKC-876(阿基仑赛注射液)用于非霍奇金淋巴瘤(II期临床)和用于套细胞淋巴瘤(II期临床),从而使公司许可引进创新药总的研究项目与去年6月持平(13项)。
复星医药许可引进创新药其他项目变化不大(部分项目略有推进)。
关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..