免疫肿瘤学(I-O)领域如今已进入发展快速轨道,目前的药物开发管线中有数千种潜在的I-O疗法和组合,其中许多项目已进入到临床试验并正在对其进行最终的疗效和安全性评估。
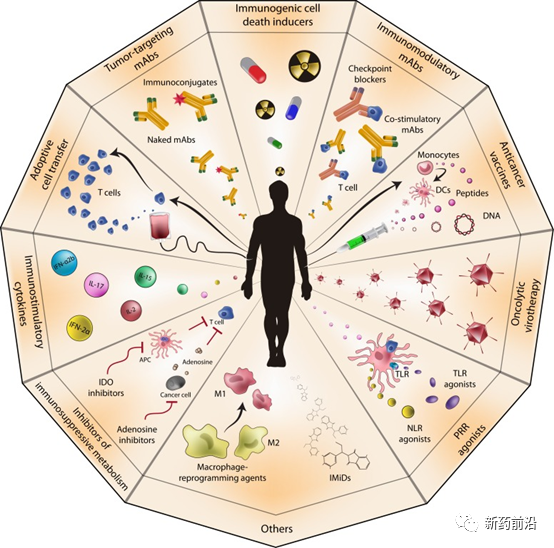
▲图1 抗癌免疫疗法[1]
纳入样本量更小
在过去的几十年中,系统性抗癌疗法发生了重大转变:细胞毒性化学疗法靶向于分裂细胞的化学物质;随后出现的靶向药物优先作用于表现出特定分子异常的癌细胞,例如用于慢性粒细胞白血病的伊马替尼和用于HER2阳性乳腺癌的曲妥珠单抗;近年兴起的免疫治疗药物可作用于癌细胞的各个方面及其与肿瘤微环境和免疫系统,可大致分为直接作用于癌细胞的药物(“被动”I-O)和刺激免疫细胞发挥抗肿瘤作用的药物(“主动”I-O)。
I-O药物包括抗肿瘤抗体、过继细胞、免疫刺激细胞因子、共抑制拮抗剂或免疫检查点抑制剂(ICI)、共刺激激动剂、免疫细胞死亡诱导剂和治疗性癌症疫苗。
随着新一代测序等高通量方法的广泛应用和成本降低,各种癌症的基因组特征得到了更好的定义。结果,癌症患者被分割成更小的亚群,生物标志物阳性人群现在被招募到基于其肿瘤特定分子特征的I-O临床试验中。
这导致I-O试验招募了更多分子同质但样本量更小的患者群体。最近的一项研究发现,每项肿瘤学试验的平均患者人数从2014年的429人已经显著减少到2019年的129人。
研究时间更短
在过去的几十年中,新抗癌药物临床开发所需的总时间也显著减少。
对于细胞毒性药物,药物开发过程通常包括一系列试验:Ⅰ期确定剂量和安全性,Ⅱ期确定剂量、记录不良反应并确定疗效,Ⅲ期确定疗效并对新疗法与现行标准进行对照研究;在成功获得Ⅲ期临床试验数据结果后即可获得监管机构批准。
在靶向治疗时代,有希望的Ⅱ期结果有时足以获得加速批准,条件是未来将需要进行紧随其后的验证性Ⅲ期研究。
在当前的免疫治疗时代,开发通常从小型Ⅰ期研究开始,在同一研究中逐步增加不同的扩展队列,有时包括随机分组。一项这样的“无缝”试验足以获得监管机构的加速批准,正如默沙东的帕博利珠单抗(Pembrolizumab) 首次人体(FIH)试验KEYNOTE-001所证明的那样,该试验招募了1260名患者,并导致该ICI获批用于黑色素瘤和非小细胞肺癌(NSCLC)适应症。
此外,这种模式转变将开发时间从大约10年缩短到<5年,细胞毒性、靶向非精准药物和精准药物开发时间中位数分别为112.7、87.1和64.6个月。
试验设计更高效
“主方案”的使用允许将一种治疗方法应用于多种疾病(“篮子”研究),或将多种治疗方法应用于一种疾病(“伞形”研究)。基于正在进行中试验积累数据分析的研究计划,开发允许修改设计和统计数据的适应性试验,将使药物在开发过程具有更大的灵活性和效率。
I-O疗法被注意到的一个有趣现象是Kaplan-Meier生存曲线(I-O与标准化疗)倾向于较晚分离,但随后会导致持续分离(有时会被描述为“曲线尾部抬升”),这意味着在一定比例的患者中观察到了持久的益处。从统计学的角度来看,这对方法学提出了挑战,因此除了无进展生存期之外,其他较新的方法,如里程碑生存期、里程碑分析和限制平均生存时间也是在I-O领域被调查研究。
与此同时,I-O试验的医学监测出现了新的挑战,因为许多免疫疗法会导致晚期、严重或不寻常的毒性,这些毒性最初可能会超出方案规定的剂量限制毒性期。此外,放射学的非典型模式在少数接受I-O药物治疗的患者中可能观察到反应,例如假性进展或超进展;因此,在I-O领域,评估肿瘤反应的标准已被修改,例如免疫疗法的应答标准(iRECIST)和实体瘤免疫相关疗效评价标准(irRECIST)。
随着I-O药物的持续增加,肿瘤学领域发生了向精准医学的重大转变,利用个体基因、蛋白质和其他癌症特征的信息来诊断或治疗特定疾病。这些快速的进步和新的前沿需要加速对临床前模型和分析的研究,并在适当的时候转化为后期临床试验;特别是随着更多生物标志物和药物靶点的确定,以支持这一新兴的治疗领域并巩固早期研究对未来疗法的价值。
延伸阅读:主方案的益处
主方案为药物开发提供了一种强大的新方法,可在高度监管的临床试验领域实现灵活性和创造性。主方案可用于整合生物标志物开发、基因亚型和具有不同作用机制的疗法。主方案试验提供了一个机会,可以有效地加快许多治疗领域的创新治疗的开发和上市。其相关益处如下:
节省时间:能够快速有效地检验假设并评估和比较药物组合(特别是在复杂疾病中)。主方案还允许公司通过增加现有的基础设施和队列来更快地激活新的研究和子研究。
节省成本:主方案有可能通过与合作伙伴分摊成本来节省成本。研究者可以通过利用共享基础设施和减少冗余来降低几个试验领域的成本,包括启动和站点招募、站点监控、管理和对照组。
分享真实世界证据:主方案通常汇集了复杂和难以治疗疾病领域的领先研究和临床专家,例如:某些难以治疗的癌症、阿尔茨海默病。这将允许利益相关者之间共享最新的科学和现实世界证据。
患者受益:主方案为患者提供由其基因亚型和生物标志物构成驱动的个性化治疗。安慰剂暴露也从通常的1:1比例降低到1:5甚至1:10。此外,主方案允许为无反应的患者提供一种以上的治疗,从而为那些以前无法治疗或危及生命的疾病的患者提供更多的机会。
对研究人员的益处:主方案允许研究人员与其他研究人员合作。研究者通过合作可以帮助对方收集观察数据、创建历史队列并快速检验临床假设。
对倡导团体的益处:主方案可以使患者倡导团体加速将临床前研究转化为其所代表的患者团体的新疗法。
参考文献:
[1] Galluzzi, L., Vacchelli, E., Bravo-San Pedro, J. M., Buqué, A., Senovilla, L., Baracco, E. E., Bloy, N., Castoldi, F., Abastado, J. P., Agostinis, P., Apte, R. N., Aranda, F., Ayyoub, M., Beckhove, P., Blay, J. Y., Bracci, L., Caignard, A., Castelli, C., Cavallo, F., Celis, E., … Kroemer, G. (2014). Classification of current anticancer immunotherapies. Oncotarget, 5(24), 12472–12508. doi.org/10.18632/oncotarget.2998
[2] Bogin V. Master protocols: New directions in drug discovery. Contemp Clin Trials Commun. 2020;18:100568. Published 2020 Apr 25. doi:10.1016/j.conctc.2020.100568
[3] Franklin MR, Platero S, Saini KS, Curigliano G, Anderson S. Immuno-oncology trends: preclinical models, biomarkers, and clinical development. J Immunother Cancer. 2022;10(1):e003231. doi:10.1136/jitc-2021-003231
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..