前言
目前肿瘤的免疫治疗主要集中在T淋巴细胞介导的适应性细胞免疫。B细胞在肿瘤免疫治疗中很大程度上被忽视。B细胞通常被认为主要参与病毒和细菌感染的体液免疫反应,在肿瘤免疫中的作用一直备受争议。但最近越来越多的临床前和临床研究证据表明,B细胞也可以通过体液和细胞免疫反应诱导强大的抗癌免疫。
然而,B细胞在癌症免疫治疗中发挥作用的机制还不是很明确,根据现有的结果,本文主要从肿瘤特异性抗体产生、抗原递呈、B细胞细胞因子释放和肿瘤内三级淋巴结构等方面讨论了B细胞的抗肿瘤免疫,并对B细胞的抗肿瘤机制进行简要的总结。此外还讨论了利用纳米材料激活和调节B细胞的策略。为肿瘤治疗提供了一个独特的视角,有望实现免疫治疗的下一步突破。
作者 | Discovery
B细胞的抗癌功能
近年来,对15种不同类型的肿瘤(如黑色素瘤、乳腺癌、非小细胞肺癌等)进行分析总结,发现肿瘤组织中B细胞的浸润与阳性预后相关。最近在软组织肉瘤(STS)中也发现在肿瘤中高密度的B细胞与延长总生存期显著相关,那么B细胞在肿瘤组织中是如何发挥作用的呢?下面将进行揭晓:
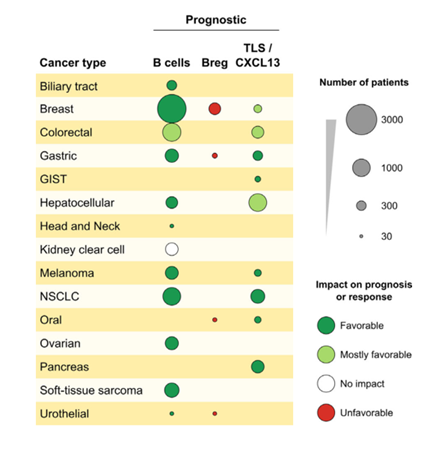
图1:B细胞浸润对肿瘤预后影响
Journal of Experimental Medicine, 2020.
1.1
癌症特异性抗体产生
B细胞在肿瘤相关抗原刺激后分化产生抗体,介导针对肿瘤抗原的体液免疫反应。从临床癌症患者的血清学分析显示,癌症患者体内可以产生P53、Survivin、Cyclin B1和HER2等肿瘤抗原的抗体。通常抗体的产生与各种癌症的阳性预后有关,并部分抗体已作为肿瘤诊断的标志物。肿瘤抗体除与肿瘤组织表面抗原结合,还可以通过抗体依赖的细胞介导的细胞毒作用(ADCC)、抗体依赖的细胞介导的吞噬作用(ADCP)和补体依赖的细胞毒作用(CDC)来清除癌细胞。研究显示,从接种HER2多肽疫苗的患者中分离HER2抗体,可以抑制表达HER2癌细胞的HER2激酶活性及其下游信号转导。
1.2
B细胞抗原递呈
B细胞是一类重要的专职抗原提呈细胞(antigen-presenting cells ,APC),但在肿瘤免疫治疗中,这一点经常被忽视。与树突状细胞和巨噬细胞主要通过吞噬方式递呈抗原不同,B细胞的抗原提呈主要通过BCR与抗原高亲和力结合,因此能够有效的识别低水平的抗原,提高抗原递呈效率。抗原与特定BCR结合后,抗原内化过程启动,并通过MHCⅡ类分子展示在B细胞表面,激活同源的CD4+辅助T细胞,产生抗体。B细胞不仅在激活CD4+ T细胞起重要作用,最近被证明B细胞也可以通过MHCI途径激活原始CD8+ T细胞。这一发现对于肿瘤治疗是一个新的突破。
1.3
B细胞细胞因子表达
B细胞可以分泌多种细胞因子,与抗肿瘤免疫相关的细胞因子主要包括TNF-α、IL-2/4/6/17、IFN-γ等,这些细胞因子能够在局部肿瘤微环境中调节免疫系统的各种成分,并调节全身免疫系统清除肿瘤细胞。最近发现肿瘤微环境中趋化因子CXCL13的存在对肿瘤预后有很好的效果,在结直肠癌(CRC)中,发现肿瘤微环境中缺乏CXCL13时,B细胞数量较少,肿瘤预后较差。但高水平的IL-6会导致严重的细胞因子释放综合征。因此,在微调B细胞抗肿瘤细胞因子上调过程中,也应避免B细胞细胞因子的过度表达,以防止副作用发生。
1.4
B细胞与三级淋巴结
综合分析不同人类肿瘤的微环境,发现B细胞与肿瘤微环境中三级淋巴结构的形成和功能的发挥有一定的联系。三级淋巴结是一种异位淋巴器官,在慢性抗原刺激的条件下在炎症组织中形成。成熟的三级淋巴结包含T细胞区和B细胞区,在T细胞区树突状细胞(DC)向T细胞递呈抗原,形成细胞免疫。在三级淋巴结中的B细胞可以从滤泡树突细胞(FDCs)获得递呈抗原,产生针对相应抗原的抗体。因此三级淋巴结可以在肿瘤部分发生特异性的免疫反应。2008年报道,在非小细胞肺癌(NSCLCP)中存在三级淋巴结,并发现其密度与肿瘤预后相关, B细胞在这一过程发挥重要作用。据研究发现, B细胞分泌的淋巴毒素α1β2可诱导三级淋巴结构的形成,并且B细胞在维持三级淋巴结构和功能方面也发挥重要作用。
B细胞与癌症:作用机制
B细胞的功能是多样的。尽管其在肿瘤中真正作用机制仍需探究,但下图简要的说明了B细胞参与肿瘤免疫的潜在机制。
在三级淋巴结的生发中心中,B细胞从FDC获取肿瘤表面抗原,并在滤泡T细胞(Tfh)帮助下被激活,增殖分化为记忆细胞和浆细胞,浆细胞产生抗体对抗肿瘤,B细胞也可以向CD8+T细胞递呈抗原促进其活化,并也可以通过ADCC和ADCP杀死或吞噬肿瘤细胞。记忆B细胞和抗体在血液中循环,帮助控制潜在的癌细胞。此外,免疫复合体与巨噬细胞的结合会导致巨噬细胞的激活和产生促炎介质,从而发挥促肿瘤活性。但与肿瘤细胞结合的抗体一部分可以激活补体,激活的补体会助长炎症并激活内皮细胞,而促进肿瘤的生长和扩散,调节性B细胞也可以产生IL-10来抑制免疫反应。因此,B细胞在肿瘤治疗中可能是一把双刃剑,在后续的研究中应扬长避短,更好的发挥B细胞在肿瘤治疗中作用。
调节性B细胞
和调节性T细胞(Regulatory cells,Treg)相似,B细胞也可以表现出调节性表型来抑制免疫反应。B细胞的调节功能主要表现在两方面,一是通过表达调节性细胞因子来实现。B细胞的调节性细胞因子以IL-10和转化生长因子β(TGF-β)为代表。在小鼠前列腺癌模型中,B细胞表达的IL-10与IgA和PD-L1一起能够抵消奥沙利铂化疗的免疫原性。除IL-10外,转化生长因子β也可以通过抑制CD8+T细胞、树突状细胞和自然杀伤细胞来抑制肿瘤免疫,并诱导调节性T细胞帮助肿瘤逃逸。二是B细胞表面表达抑制性受体。B细胞可以表达包括PD-1及其配体PD-L1/L2在内的免疫检查点分子,在体液免疫和细胞免疫中具有多种不同的调节功能。最近在肝癌中发现,高表达PD-1的B细胞在遇到PD-L1细胞时,通过释放IL-10来诱导T细胞抑制,加入检查点阻断抗体阻断B细胞上的PD-1可以促进癌症的免疫治疗。
纳米材料在B细胞激活中的应用
目前,纳米材料形式的疫苗佐剂在实验中已被证实其有助于B细胞激活。纳米疫苗激活B细胞的独特优势在于纳米颗粒表面可以同时展示多个抗原用于BCR识别,与单个抗原相比有更强的B细胞激活作用。基于这一优势,纳米材料佐剂已经应用于艾滋病疫苗和新冠肺炎疫苗。同样,纳米材料也可以载抗肿瘤药物或以肿瘤疫苗的形式递送到病灶部分达到肿瘤治疗效果。
总结
随着研究的不断深入,B细胞在肿瘤免疫治疗中的作用不断突显,因此利用B细胞的免疫治疗策略可能是继T细胞为主要免疫治疗策略后的一个新的突破。B细胞在肿瘤治疗中的作用可能是通过产生肿瘤特异性抗体或通过ADCC、ADCP和CDC作用消灭癌细胞。此外B细胞被抗原激活后,可以激活CD4+和CD8+T细胞,起到肿瘤杀伤的作用。但B细胞用于肿瘤免疫治疗也存在几个挑战,激活B细胞的同时调节性B细胞的比例也会上升,此外,过度的B细胞激活可能引起炎症风暴。但随着纳米材料在药物控释方面的研究,通过控制B细胞刺激物的释放,这一问题可能得到很好的解决。因此,基于纳米材料的B细胞肿瘤治疗有望成为肿瘤治疗领域的下一次突破。
参考文献:
[1]Fridman W H, Petitprez F, Meylan M, et al. B cells and cancer: To B or not to B?[J]. Journal of Experimental Medicine, 2020.
[2]Shi Y. PLAN B for immunotherapy: Promoting and leveraging anti-tumor B cell immunity[J]. Journal of Controlled Release, 2021.
[3]Michaud D, Steward C R, Mirlekar B, et al. Regulatory B cells in cancer[J]. Immunological Reviews, 2020.
* 推文用于传递知识,如有版权等疑问,请于本文刊发30日内联系BiG生物创新社。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..