近日,国家药品监督管理局医疗器械技术审评中心(CMDE)创新医疗器械特别审查申请审查结果公示(2022年第2号)显示,位于张江科学城的上海星湾生物技术有限公司(以下简称“星湾生物”)自主研发生产的抗-CD19-嵌合抗原受体T细胞检测试剂盒(流式细胞仪法-PE)已通过创新医疗器械特别审查申请。
这也是迄今全国首个进入创新“绿色通道”的CAR-T细胞治疗临床检测产品,从申请受理到公示仅用时35个工作日。
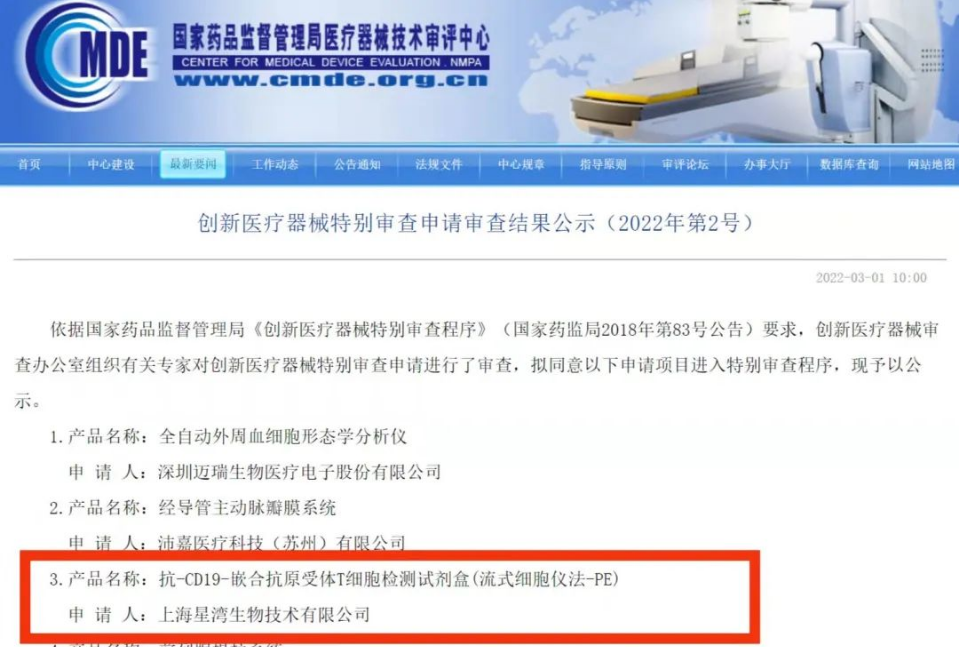
星湾生物成立于2018年7月,聚焦细胞治疗精准检测,为CAR-T药企和临床机构提供药代、ADA/Nab、单细胞测序、质谱流式等检测产品,以及研发、质控、临床检测整体解决方案。
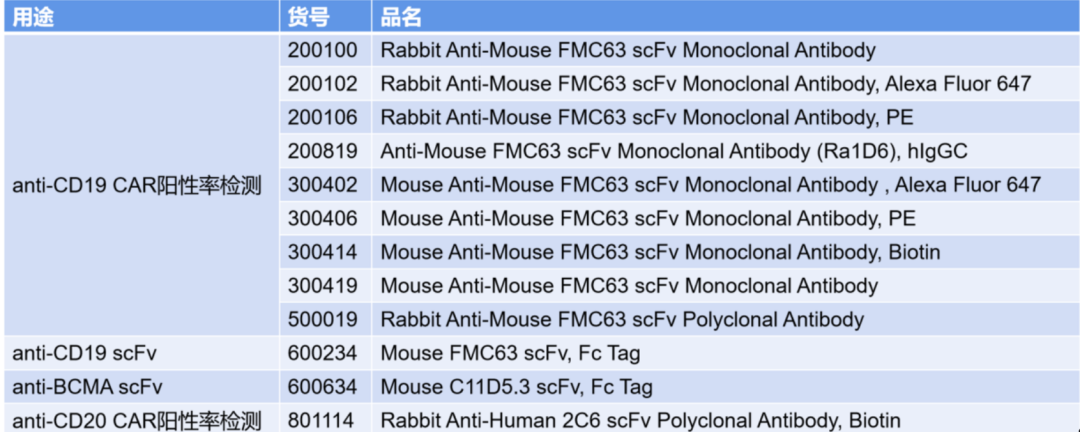
图片来源:星湾生物官网
对于CAR-T细胞治疗,患者体内CAR-T细胞的检测非常重要。CAR-T治疗主要是通过基因工程技术体外改造肿瘤患者的T淋巴细胞,在体外大量培养后生成肿瘤特异性CAR-T细胞,再将其回输入患者体内用以攻击癌细胞,进而达到治疗疾病的目标。然而,CAR-T治疗并不仅仅止于细胞回输。CAR-T是“活”的药物,其疗效,急、慢性毒副作用,复发风险等等,都与CAR-T在体内的变化密切相关。2021年由中国研究型医院学会生物治疗学专委会的专家组织发表了《CAR T细胞治疗NHL毒副作用临床管理专家共识》,指出急性CRS、慢性CRS、CAR-T细胞异常增殖、噬血细胞性淋巴组织细胞增生症/巨噬细胞活化综合征(HLH/MAS)等临床急性毒副作用的诊断都需要检测患者体内CAR-T增殖情况。
因此CAR-T细胞回输后,患者体内CAR-T的检测必不可少,而星湾生物自主研发并申报的抗-CD19 CAR-T流式检测产品灵敏度可达十万分之一,据悉其相比诺华临床检测水平(千分之一)有显著提升,目前国内已获批2款CAR-T产品,并有众多CAR-T产品正在研发中,星湾生物的CAR-T伴随检测产品未来或将为这些药物的临床精准检测带来助力。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..