1 月 18 日,默沙东宣布在 2022 年美国临床肿瘤学会胃肠癌(ASCO GI)研讨会上公布 Keytruda 单药二线治疗索拉非尼治疗后进展的肝细胞癌的 3 期临床 KEYNOTE-394 研究的最终结果(摘要 #352788)。在新闻稿中默沙东指出,这是全球首个 PD-1/L1 抑制剂单药二线治疗肝癌的 3 期临床。2022 ASCO GI 全部摘要已经在官网公布,在 Insight 数据库回复「2022ASCO GI」即可获取
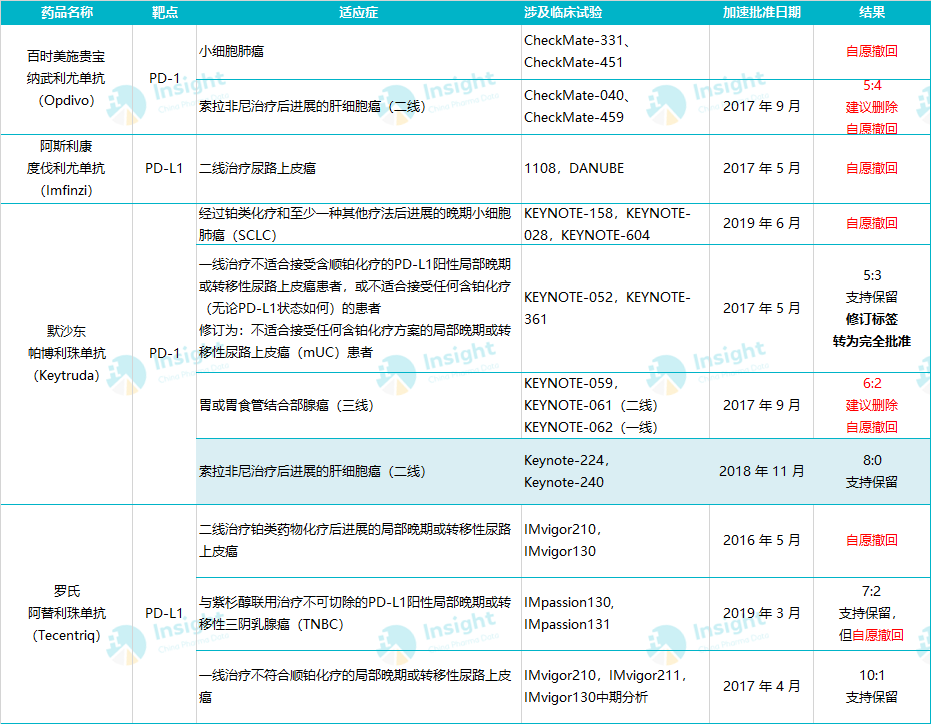
值得一提的是,二线肝癌 3 期临床的阳性结果对 K 药这一适应症能否保住有重要意义。美国 FDA 在 2021 年集中讨论了加速批准却未能在验证性临床中证实疗效的 6 个 PD-1/L1 单抗适应症的去留问题,其中就包括 K 药和 O 药二线治疗肝癌的适应症。O 药的二线肝癌适应症被撤销,而 K 药则暂时保留,等待下一项 3 期临床数据的证明。
2021 年 9 月,默沙东宣布 3 期 KEYNOTE-394 研究达到主要终点,显著延长了亚洲患者 OS。今日该公司公布了相应数据,并表示正基于 KEYNOTE-394 的结果与全球监管机构进行讨论,在美国将其作为一项潜在的验证性研究进行评估。
KEYNOTE-394(NCT03062358)是一项随机、双盲 3 期试验,评估 KEYTRUDA + 最佳支持治疗(BSC)与安慰剂 + BSC 在先前接受过索拉非尼或奥沙利铂化疗的亚洲晚期 HCC 患者中的疗效。主要终点是 OS,其他终点包括 PFS、ORR 和 DOR。该研究在中国和韩国招募了 453 名患者,由秦叔逵教授牵头开展。
结果显示,帕博利珠单抗治疗组在主要终点 OS 方面表现出具有统计学显著性和临床意义的改善,与安慰剂相比,既往接受过治疗的晚期 HCC 患者死亡风险降低了 21%(HR=0.79 [95% CI,0.63-0.99];p=0.0180)。接受帕博利珠单抗治疗的患者中位 OS 为 14.6 个月(95% CI,12.6-18.0),而接受安慰剂治疗的患者为 13.0 个月(95% CI,10.5-15.1)。帕博利珠单抗组患者两年内存活率为 34.3%,而安慰剂组则为 24.9%。
其他疗效终点结果显示,与安慰剂相比,帕博利珠单抗组将疾病进展或死亡的风险降低了 26%(HR = 0.74 [95% CI,0.60-0.92];p = 0.0032),中位 PFS 为 2.6 个月(95% CI,1.5-2.8),而安慰剂组为 2.3 个月(95% CI,1.4-2.8)。ORR 为 12.7%(95% CI,9.1-17.0)vs. 1.3%(95% CI,0.2 -4.6),中位 DOR 为 23.9 个月(2.8 至 32.0+)vs. 5.6 个月(3.0+ 到 5.6)。
不过,这项临床试验的结果也仍存有一些隐忧。一方面,仅降低死亡风险 21%、延长中位 OS 1.6 个月、延长中位 PFS 0.3 个月,获益有限,尽管作为单药在经济性上将带来优势;另一方面,这项试验纳入人群为亚洲患者,以中国患者为主,也给 FDA 是否能接受其作为验证性临床将加速批准转为正式批准带来了疑问,因为 FDA 可能会考虑疾病差异、人群差异、标准治疗差异等因素。
肝癌是全球癌症相关死亡的主要原因之一。根据 WHO 2020 年度报告,全球范围内肝癌发病率居于第 6 位,死亡率却居于第 3,2020 年全球约 83 万患者死于该病,这意味着该领域治疗仍有极大的未满足需求。约 75% 至 90% 的原发性肝癌病例是肝细胞癌(HCC),风险因素主要是乙肝、丙肝、饮酒和代谢综合征。
默沙东临床研发副总裁 Scot Ebbinghaus 博士表示,晚期肝细胞癌患者仍然存在高度未满足的医疗需求,急需能够带来 OS 获益的新疗法。默沙东将通过广泛的肝细胞癌全球项目开发来为患者提供帮助。
目前,默沙东有 7 项肝细胞癌全球临床,包括 KEYNOTE-394 在内总计将纳入约 3000 名患者,正在各线数环境、单药或各种联合疗法之中评估其疗效。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..