2021年11月22日,CRISPR Therapeutics公司宣布美国FDA已授予CTX110再生医学先进疗法认定(RMAT)。CTX110是一款利用CRISPR基因编辑技术改造的同种异体CAR-T细胞疗法,用于治疗CD19阳性的B细胞恶性肿瘤患者。
CTX110将靶向CD19抗原的嵌合抗原受体(CAR)定位敲入细胞的天然T细胞受体(TCR)位点,在引入CAR的同时防止内源性TCR的表达,从而防止移植物抗宿主病(GvHD)的产生。同时它还利用基因编辑敲除了1型主要组织相容性复合体的表达,降低患者的免疫系统对输入的细胞疗法的攻击。

▲CTX110简介(图片来源:CRISPR Therapeutics公司官网)
目前正在进行的多中心、开放标签1期临床试验旨在评估多个剂量水平的CTX110,治疗复发/难治性B细胞恶性肿瘤的安全性和有效性。之前获得的积极数据表明,在接受剂量超过10^8个细胞的CTX110治疗的大B细胞淋巴瘤患者中,基于意向治疗分析的总缓解率为58%,完全缓解率为38%。在接受治疗6个月后,完全缓解率为21%,最长的缓解持续时间超过18个月,显示了CTX110带来持续缓解的潜力。在安全性方面,CTX110表现出差异化的积极安全性特征。各个不同剂量的详细缓解信息如下图所示:
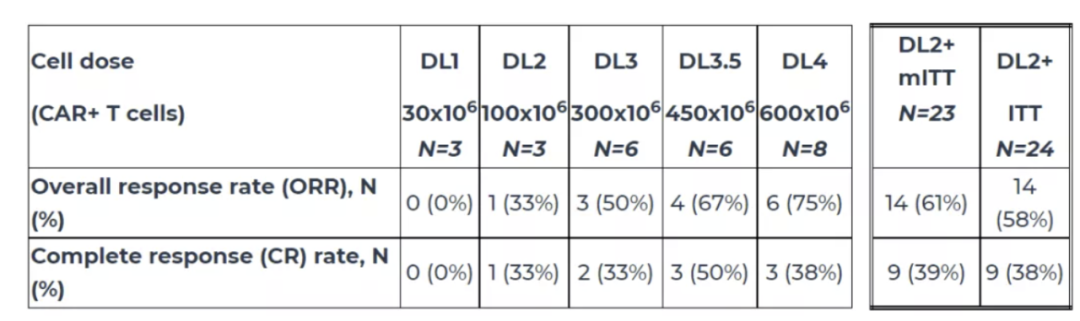
▲CTX110的1期临床试验疗效数据(图片来源:参考资料[2])
“FDA授予RMAT是基于令人鼓舞的临床数据,这是一个重要的里程碑,意味着CTX110在治疗血液系统恶性肿瘤方面的变革性潜力。”CRISPR Therapeutics首席执行官Samarth Kulkarni博士表示, “我们期待与FDA密切合作,致力于将这种重要的新治疗方式带给患者。”
公众号
参考资料:
[1] CRISPR Therapeutics Announces FDA Regenerative Medicine Advanced Therapy (RMAT) Designation Granted to CTX110™ for the Treatment of Relapsed or Refractory CD19+ B-cell malignancies. Retrieved November 22, 2021, from https://crisprtx.gcs-web.com/news-releases/news-release-details/crispr-therapeutics-announces-fda-regenerative-medicine-advanced
[2] CRISPR Therapeutics Reports Positive Results from its Phase 1 CARBON Trial of CTX110™ in Relapsed or Refractory CD19+ B-cell malignancies. Retrieved October 12, 2021, from https://www.globenewswire.com/news-release/2021/10/12/2312955/0/en/CRISPR-Therapeutics-Reports-Positive-Results-from-its-Phase-1-CARBON-Trial-of-CTX110-in-Relapsed-or-Refractory-CD19-B-cell-malignancies.html
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..