“交易有风险,出手需谨慎!”
就在9月8日收购Kadmon仅一天后,赛诺菲就完美诠释了生物制药行业交易收购风险这一箴言。
9月9日,赛诺菲发布公告,该公司开发的口服鲁顿酪氨酸激酶(BTK)抑制剂rilzabrutinib在其主要适应症天疱疮(一种罕见的自身免疫性皮肤病)的3期研究中失败。

rilzabrutinib是赛诺菲一年前以36.8亿美元收购Principia囊获BTK抑制剂产品组合中的晚期项目之一。
评估rilzabrutinib治疗天疱疮的3期PEGASUS试验未达到其主要或关键次要终点。这项3期研究是第一个BTK抑制剂在天疱疮中的安慰剂对照试验。
赛诺菲对Principia的收购看起来很冒险,此次研究失败引发了业界对rilzabrutinib是否会在赛诺菲正在关注的其他各种适应症中发挥作用的怀疑。
rilzabrutinib目前正在进行一项治疗免疫性血小板减少症(ITP)(一种罕见的血液疾病)的3期试验,以及一项治疗自身免疫性疾病IgG4相关疾病的2期研究。公司还计划于2021年开始针对其他免疫疾病(包括哮喘、特应性皮炎、慢性自发性荨麻疹和温热自身免疫性溶血性贫血)进行2期研究。
现在对免疫性血小板减少症似乎也不应抱有太高的希望,最近的失败对于赛诺菲评估rilzabrutinib的其他用途的计划来说也不是好兆头。
rilzabrutinib的挫折对于其他BTK抑制剂治疗自身免疫性疾病的开发者来说也可能是个坏消息,他们依赖于B细胞在此类疾病中起主要作用机制。
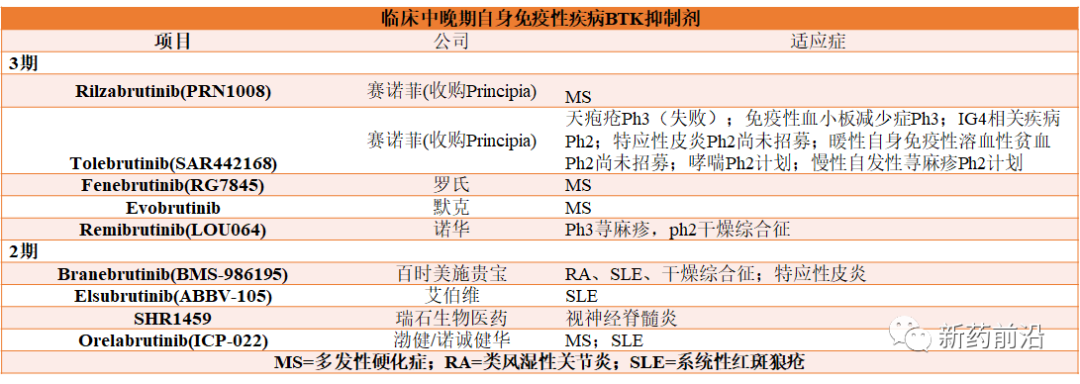
多发性硬化症是一个重点领域,渤健最近从诺诚健华获得了orelabrutinib(奥布替尼)授权,也进入到1期研究中。
多款多发性硬化症BTK候选药物已经充分利用了其跨越血脑屏障的能力。但更直接的问题是,rilzabrutinib的失败强调了这种机制是否对完全阻止自身免疫性疾病有效。
然而,赛诺菲收购Principia的主要焦点是多发性硬化症候选药物tolebrutinib,该药物仍在3期研究中。
赛诺菲对tolebrutinib的信心是否合理还需要一段时间才能显现出来,四项关键多发性硬化症研究中的第一项将于2023年公布数据。
不过,tolebrutinib的中期数据并不明确,存在关于替代终点的使用、复杂的试验设计和较小患者数量的问题。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..