默沙东(Merck & Co)近日宣布,美国食品和药物管理局(FDA)已受理缺氧诱导因子-2α(HIF-2α)抑制剂belzutifan(MK-6482)的新药申请(NDA)并授予了优先审查,该药是默沙东肿瘤学管线中的一款新型候选药物,用于治疗无需立即手术的、与希佩尔·林道综合征(Von Hippel-Lindau disease,VHL综合征,VHL病)相关的透明细胞肾细胞癌(ccRCC)患者。
FDA已指定该NDA的《处方药用户收费法》(PDUFA)目标日期为2021年9月15日。之前,
FDA已授予belzutifan突破性药物资格(BTD)和孤儿药资格(ODD)。值得一提的是,导致发现HIF-2α的VHL生物学研究于2019年获得诺贝尔生理学或医学奖。
此次NDA,基于评估belzutifan治疗VHL相关ccRCC患者的II期Study-004研究(NCT03401788)的数据。该研究结果显示,在VHL相关ccRCC患者中,belzutifan治疗表现出持久缓解,确认的客观缓解率(ORR)为36.1%(n=22/61;95%CI:24.2-49.4)。
VHL综合征是一种罕见的影响多器官的
遗传性疾病,会使患者面临多种癌症的风险,包括肾细胞癌。癌症仍然是VHL综合征患者的主要死亡原因之一,目前还没有批准的系统性治疗方案,因此对新的治疗方案存在着迫切需求。来自上述II期试验的结果提供了belzutifan潜在益处的证据,并支持进一步研究这种HIF-2α抑制剂如何对这些患者发挥有意义的作用。
默沙东研究实验室临床研究副总裁Scot Ebbinghaus博士表示:“VHL病是一种罕见的
遗传病,目前尚无系统的治疗方案,并且与多个器官发生癌症的高风险相关。事实上,高达70%的VHL患者在其一生中会发展成肾细胞癌。这一优先审查证实了我们在通过创新的新治疗方法扩大和多样化默沙东
肿瘤治疗管线方面取得的重要进展。我们期待着与
FDA密切合作,为有需要的患者提供belzutifan。”
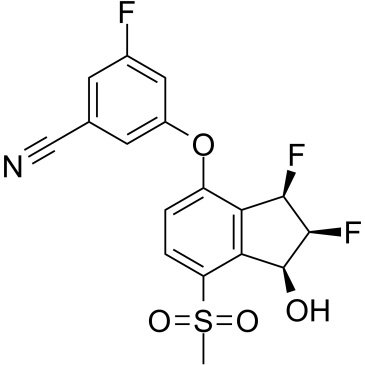
belzutifan(MK-6482)化学结构式(图片来源:medchemexpress.com)
VHL综合征是一种罕见的
遗传病,每36000人中就有一人患上这种病(全世界20万例,仅美国就有1万例)。VHL综合征患者有患良性血管
肿瘤以及包括RCC在内的多种癌症的风险。高达70%的VHL综合征患者发生RCC,这是VHL综合征患者死亡的主要原因。
肾细胞癌(RCC)是目前最常见的肾癌类型,10例肾癌中约有9例为RCC,10例RCC中约有7例为透明细胞癌(ccRCC)。据估计,到2020年,全球约有43.13万例肾癌确诊,约17.94万人死于该病。据估计,仅在美国,2021年就将有近7.61万例新的肾癌确诊病例、近1.38万人死于该病。
VHL基因是一种重要的肿瘤抑制基因,其突变最早是在VHL综合征患者中发现的。VHL蛋白是一种肿瘤抑制蛋白,其失活可异常激活肿瘤患者体内的缺氧诱导因子-2α(HIF-2α)蛋白。这种VHL抑癌蛋白的失活在90%以上的ccRCC肿瘤中被观察到,导致缺氧诱导因子(HIF)蛋白在癌细胞内积聚并激活,错误地发出缺氧的信号,这会激活血管形成,刺激良性和恶性
肿瘤的生长。
belzutifan(MK-6428)是一种新型、强效、选择性、口服HIF-2α抑制剂,靶向抑制HIF-2α,阻断细胞生长、增殖以及阻止异常血管形成。belzutifan由Petolon Therapeutics公司研制,默沙东在2019年5月以10.5亿美元首付款、11.5亿美元里程碑款项将Petolon Therapeutics收购。
目前,belzutifan正在多个临床研究中进行评估。除了治疗VHL相关ccRCC的II期试验(NCT03401788)之外,belzutifan临床开发计划还包括治疗晚期RCC的III期试验(MK-6482-005;NCT04195750)、治疗晚期实体瘤包括晚期肾癌的I/II期剂量递增和剂量扩展试验(NCT02974738)。(生物谷Bioon.com)
原文出处:Merck Receives Priority Review From
FDA for New Drug
application for HIF-2α Inhibitor Belzutifan (MK-6482) - FirstWord Pharma