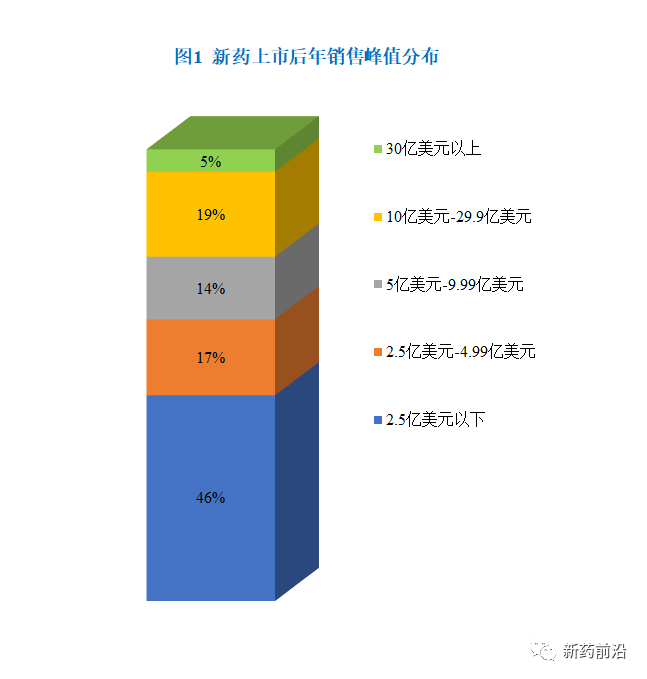
在截止2019年的过去15年中,美国上市新药的销售额平均峰值约为8亿美元,只有五分之一的新药在美国的销售峰值达到10亿美元,而超过一半的新药甚至没有达到2.5亿美元。
随着药物开发投入的持续增加【新药开发成本解析(附案例)】,开发新的“重磅炸弹”级别新药的可能性似乎变得越来越容易【2021年畅销药TOP 10:修美乐称“王”,“K”药逼近】。因此,大多数生物制药公司越来越关注于如何有效开发具有高商业潜力的候选产品【2021年这些“重磅炸弹”级药物将上市】。
但是,药品监管机构的批准并不保证其上市后的商业成功,这仅仅是新的开始。为了尽可能实现上市产品真正的价值,生物制药公司必须完美执行新产品上市后的商业化过程至关重要。
历史经验表明,由于诸如市场准入受限,对市场需求了解不足或对竞争威胁的误判等多种因素,许多公司在新药上市后的商业化过程中遭遇失败。
半数新药上市后销售额不如预期
01
在美国,纳斯达克生物技术指数在过去15年中上涨了600%以上,反映出投资者对大量新药的热情,业内分析师认为这些新药有可能成为“重磅炸弹”级别,但实际可能是潜在的“雷区”。
但是,到底有多少新药在上市后的市场表现能够符合业内分析师的高期望呢?
投资者或生物制药公司在新药上市前预期与其上市后的表现或许存在着不小的差距。
根据全球领先的战略咨询公司L.E.K.(艾意凯)的最新报告,在2004年至2016年获得FDA批准的450种新分子实体,约有一半药物上市后的销售额低于分析师的预期,且销售额低于预期值超过了20%。
实际上,在截止2019年的过去15年中,美国上市产品的销售额平均峰值约为8亿美元,只有五分之一的新药在美国的销售峰值达到10亿美元,而一半的新药甚至没有达到2.5亿美元。
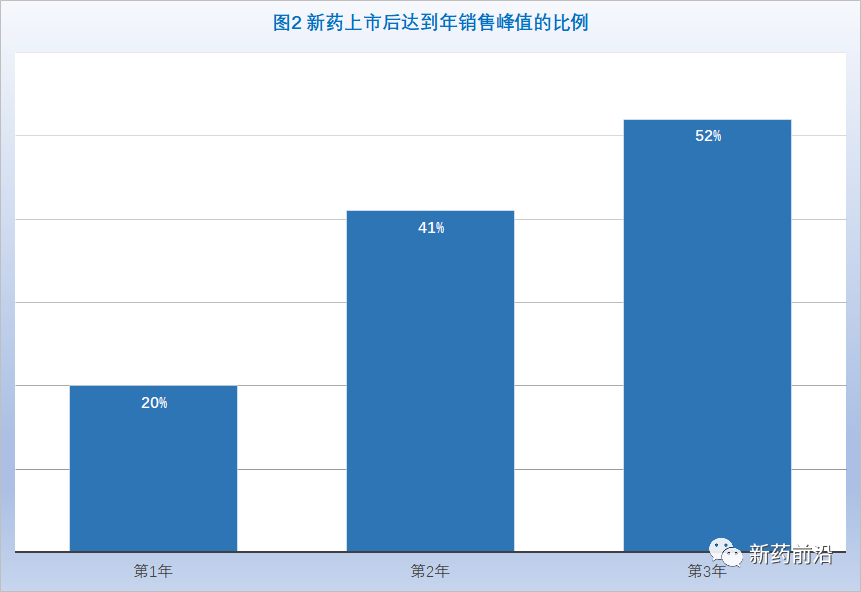
在大多数疾病领域竞争不断加剧的情况下,新上市产品的商业化异常艰难。平均而言,新药在上市后第三年才达到其销售额峰值的50%。肿瘤学等领域的增长速度更快些,到第二年年底达到销售额峰值的50%。
诚然,分析师预测的准确性很可能存在“偏差”。大多数市场观察家都认为,分析师预测的准确性参差不齐,因为对仍处于临床开发阶段的产品进行预测具有很强的不确定性。
在新药上市后的最初几年尤其如此,要满足不现实的业内分析师期望可能会充满挑战。过去15年药物市场的分析显示,新药在美国上市后第一年的销售额低于2.5亿美元的产品占90%以上,第二年销售额低于2.5亿美元的仍旧达到70%以上。
传染病,免疫学和心血管领域表现最差
02
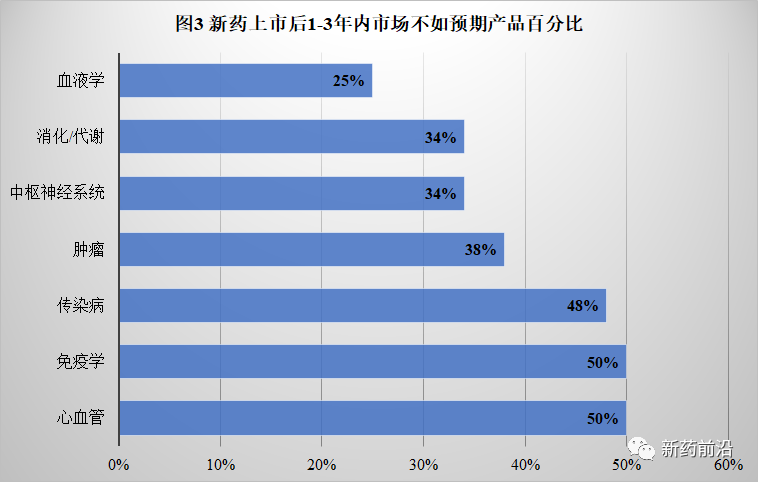
就治疗领域而言,传染病,免疫学和心血管疾病等领域则表现更差。一半的心血管新药物和免疫学新药在上市后的三年内都达不到预期,大约48%传染病新药也未能达到目标。
毋庸置疑,近年来,心血管领域的新药在高端市场上异彩纷呈,但最终市场表现却令人失望。以降胆固醇药物PCSK9抑制剂——赛诺菲/再生元的Praluent(alirocumab,阿利西尤单抗)和安进的Repatha(evolocumab,依洛尤单抗)为例,在2015年上市时都被认为是“重磅炸弹”级别(10亿美元),但至今都没有达到。当然,该类药物受到了包括大规模降价在内的多种因素困扰【PCSK9抑制剂再增新员:三强鼎力之势将定】。
癌症领域的新药上市后的市场表现要好于前述3个治疗领域的药物,只有38%未能达到市场预期。当然该领域的创新对其上市后的表现有所帮助。
然而,不可否认的是,FDA近年来批准新药在上市后第5年的整体销售额呈现增长趋势。主要原因可能是:一方面获批新药数量明显增加;另一方面,部分单品的高销售额进而拉升了年度批准新药的整体销售额。
小公司创新性强,大公司商业化更强
03
小型生物制药公司比大型生物制药公司拥有更好的研发设备,更具有创新性,并能开发同类首创(First-in-Class)或同类最优(Best-in-Class)的产品,其中小型生物制药公司开发的产品50%以上是创新产品。
通常认为公司规模是创新的障碍,但在新药品的商业化和生命周期管理方面,却成为其成功关键的推动力。
只有极少数新兴生物制药公司推出其首款产品超出了分析师的销售预期,这突显了对于首次上市新产品的较小型公司而言,商业执行具有很大的挑战性。
与小型生物技术公司相比,大型制药公司具有更好的资源配置能力,将新产品商业化更为成功。大型制药公司新产品的销售额平均峰值比小型生物技术公司高出50%。
在心血管,传染病和免疫学领域推出药物的小型生物技术公司面临着特别高的障碍,因为它们必须将这些产品推销给全科医生和专家。小型生物技术公司往往低估了对不同的医生群体的教育和处方行为习惯改变面临的巨大挑战。
后记
近年来,我国生物制药公司创新能力不断增强【中国创新药迎来收获季:11款获批产品一览】,越来越多的企业开始对走向发达国家市场跃跃欲试,其开发的新药在那些地区即将申请上市或者已经获批上市,在发达市场进行产品商业化同样面临着不小的挑战。【百济神州CEO欧雷强谈与诺华达成PD-1交易】
新药上市后商业化的一些关键经验值得参考:
1
尽早制定上市计划:即使对于拥有出色产品的公司,缺乏推行新产品上市计划准备也可能导致未来市场表现欠佳。因此,生物制药公司在首次获得新药批准之前至少36个月开始考虑制定市场推广计划。同样重要的是,要确保有一个跨职能的团队来支持和跟踪对新产品成功上市至关重要的各种事情。
2
对上市的挑战要切合实际:作为上市过程的一部分,生物制药公司的管理层需要严肃地考虑产品在终端可及性的障碍,尤其是适应症针对的是一些规模较大的初级保健或以医院为重点的新药。在不同适应症和治疗领域,定价和报销压力,以及与主要利益相关者的接触以及竞争压力差异很大,并且会明显影响药物应用的范围和速度。
3
认真考虑伙伴关系:由于资源和能力有限,较小的生物制药公司在进行推广新药时的成功率不及大型生物制药公司。对于生物制药公司管理层来说,重要的是要对产品商业化选择进行战略性思考,并仔细评估合作机会。
4
管理投资者的期望:生物制药公司应彻底审视新药的预测假设,并及时征求外部专家意见,以管理投资者对实现现实和可实现目标的期望。目标患者人数的小幅夸大,市场准入水平的错误判断或新竞争动态的错误描述可能会大大推高新药的销售预测,使市场期望与上市计划工作不一致。
说明:
1
分析师的“预期”
为第一到第三年的实际累计销售额,占预期该三年期间累计销售额的80%至120%。
2
生物制药公司规模“定义”
小型公司是指其新药上市时市值低于50亿美元的公司
中型公司是指其新药上市时市值在50亿美元和400亿美元之间的公司
大型公司是指其新药上市时市值超过 400亿美元的公司
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..