2月22日,是中国首个生物类似药获批2周年的日子。两年前的今天,国家药品监督管理局批准复宏汉霖研制的汉利康(利妥昔单抗注射液)上市注册申请,主要用于非霍奇金淋巴瘤的治疗。
5家企业9款产品上市,阿达木类似药最多
两年过去,我国已有9款生物类似药获批上市,其中复宏汉霖和信达生物各收获3款,成为生物类似药上市赢家,百奥泰、齐鲁制药和海正博锐各收获1款。
国内已上市的生物类似药
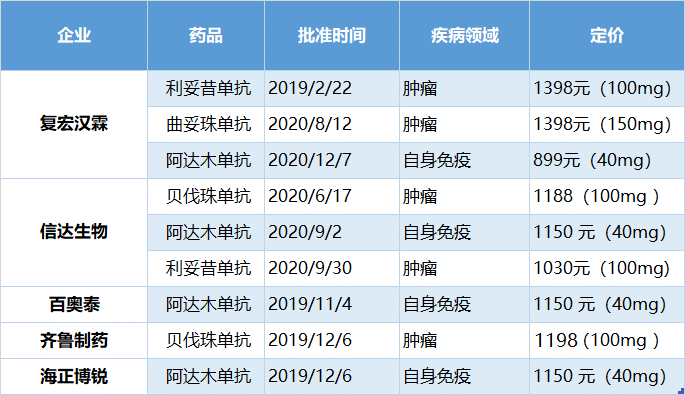
复宏汉霖是我国第一家拿下生物类似药的企业,其开发的利妥昔单抗是中国按照《生物类似药研发与评价技术指导原则(试行)》上市的首个生物类似药。据复宏汉霖财报披露,复宏汉霖2019年实现利妥昔单抗类似药销售分成收入7900万元,授权许可收入860万元。
2020年,复宏汉霖再次拿下2款生物类似药,分别是汉曲优(曲妥珠单抗)和汉达远(阿达木单抗)。并且,其曲妥珠单抗类似药也获得欧盟批准,是首个中欧双批的国产单抗生物类似药。
信达生物在2020年先后斩获3款生物类似药,分别是达攸同(贝伐珠单抗)、苏立信(阿达木单抗)以及达伯华(利妥昔单抗)。
2020年1月,信达生物将其贝伐珠单抗类似药在美国和加拿大的商业化权益授权给Coherus Bioscences。根据协议条款,该项合作的首付款、里程碑付款累计4500万美元,信达还将获得双位数百分比的销售分成。一年后信达生物宣布与印度尼西亚公司Etana签订合作协议,授予Etana该药物在印度尼西亚的独家许可。在该项合作中,信达生物将获得开发和销售里程碑付款以及双位数比例的净销售额提成,具体财务条款暂未披露。
百奥泰、齐鲁及海正的3款生物类似药皆于2019年批准。2020年8月,百济神州以最高至1.65亿美元引进贝伐珠单抗类似药(BAT1706)相关知识产权及其在中国地区的授权、分销、供货等产品权益。2021年1月,百奥泰宣布该药物在美国FDA上市许可申请获得受理。
据业内流传的消息,齐鲁制药安可达(贝伐珠单抗)2020年销售额约18亿元,考虑到齐鲁贝伐珠单抗较低的价格,18亿这个数字已经非常惊人,可以说是生物类似药中的销量翘楚。
法规不断完善,外推适应证需谨慎
2006年,仿制药和生物类似物领域的巨头山德士研发的重组人生长激素 Omnitrope(参照药Genotropin)通过欧盟药品评审委员会批准上市,成为国外第一款上市的生物类似物,拉开了全球生物类似物研发的序幕。
欧盟从“创新”与“仿制”间寻找突破点,率先开展系统的制度探索,成为全球第1个建立生物类似药法律体系的地区,是生物类似药时代的先行者。至今欧盟已为生物类似药的发展建立了较为完整的监管框架,为全球生物类似药产业的发展提供了经验。截止到2月20日,欧盟共批准了74款生物类似药,其中包括32个单克隆抗体药物,其中仅阿达木单抗类似药就有11款。
美国虽然并不是最早建立生物类似药法规及技术指南的国家,但美国制定了一系列《生物制品价格竞争与创新法案》、《患者保护和平价医疗法案》、《FDA紫皮书》等法规为FDA审批生物类似药构建了完善的法规体系,间接促进了该国生物类似药的研发和上市。2015年3月6日,美国批准了第一个生物类似药——山德士研发的非格司亭。截止到2月20日,FDA共批准了29款生物类似药,其中阿达木单抗类似药占6款。
回归到CDE的定义,生物类似药是指在质量、安全性和有效性方面与已获准注册的参照药具有相似性的治疗用生物制品,包括单抗、重组蛋白、血液制品等。生物类似药的氨基酸序列原则上应与参照药相同,宿主细胞和表达体系原则上与参照药类似。
考虑到生物制品具有分子量大、结构复杂、生物活性对其结构完整性依赖性强、生产工艺复杂等特点,因此,随着国内外生物类似药研发和评价的不断深入,生物类似药的相似性评价及适应证外推的科学标准成为业界备受关注的重点领域。
此前CDE曾发文,参照药已在国内获批多个适应证的,如果候选药通过比对研究证实了与参照药临床相似,可以考虑外推至参照药的其他适应证。适应证外推需根据品种特点和相似性研究数据的充分性个案化考虑。外推的适应证,应当是临床相关的病理机制和/或有关受体相同,且作用机理以及靶点相同的;临床比对试验中,选择了合适的适应证,并对外推适应证的安全性和免疫原性进行了充分的评估。
随着行业对生物类似药的认知逐渐清晰,立法部门对此的监管也正趋于不断完善。据笔者统计,药审中心先后发布了12份与生物类似药相关的指导原则及征求意见稿。其中不乏贝伐珠单抗、利妥昔单抗、曲妥珠单抗等多个热门药物生物类似药的临床试验指导原则,为此类产品研发的临床方案设计及具体操作提供了详细参考依据。
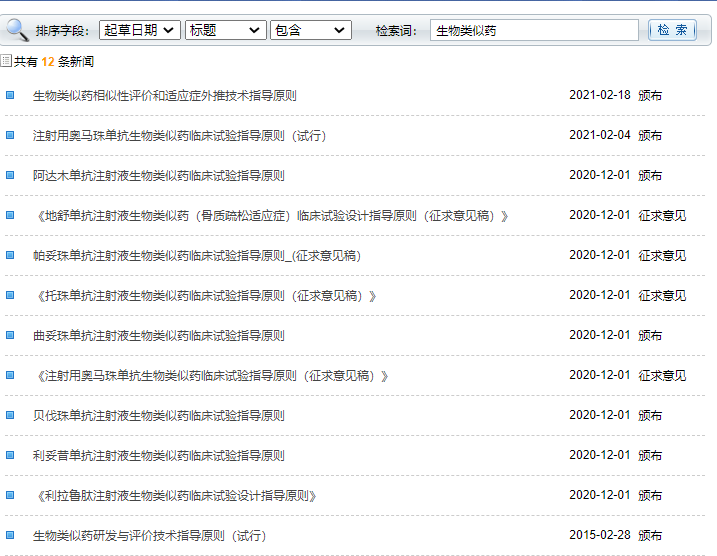
2月18日,CDE即发布了《生物类似药相似性评价和适应证外推技术指导原则》,旨在进一步规范和指导生物类似药的研发和评价,同时在为其集中带量采购铺路。尤其是明确了“生物类似药不能自动外推参照药的全部适应证”、“适应证外推应根据产品的特点和目标适应证特点个案化考虑”,即要想获批,必须就每个适应证单独提交申请和相关证据。这也意味着,生物类似药在外推适应证方面需要更加谨慎。
贝伐珠类似药竞争激烈,集采渐近
除上述获批的5家企业外,国内目前还有多家企业的多款生物类似药已经申报上市或处于III期临床阶段,其中有部分预计可以在2021年获得批准。从品种上看,贝伐珠单抗将成为竞争最激烈的品种。
国内处于后期研发阶段的生物类似药
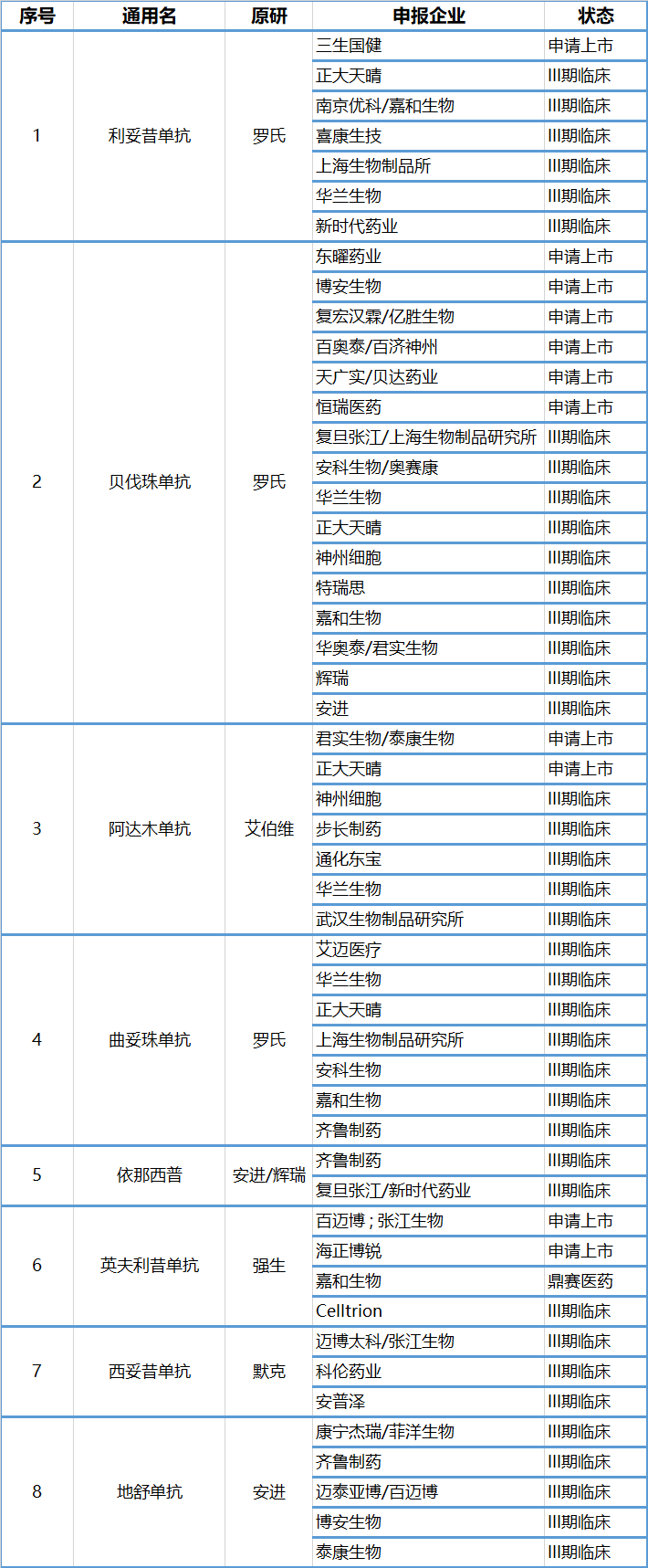
我国生物类似药审批政策逐渐与国际接轨,增加医保覆盖和医保降价谈判进一步提高了患者的可及性。按通用名确定的医保目录以及对应的医保药品支付标准中,生物类似药和原研药品属于同通用名,理论上可以相互替换。
根据国家医保局在答复第十三届全国人大三次会议“关于加快银屑病等疾病医疗保障水平的建议”时明确,正在研究生物制品集中采购相关政策,生物类似药并非集中带量采购的禁区,将适时开展集中带量采购。
今年1月28日,国务院发布的《关于推动药品集中带量采购工作常态化制度化开展的意见》要求,“逐步覆盖国内上市的临床必需、质量可靠的各类药品,做到应采尽采”,在次日(1月29日)召开的国务院政策例行吹风会上,医保局领导又进一步强调“生物类似药跟化药的仿制药质量评价方式上有差别,但是它有严格的质量标准,下一步纳入集采是毫无疑义的。”
对此也有分析师认为,生物类似药主要分布在肿瘤和自免等领域,国内渗透率提升空间巨大,以价换量的市场仍然远超普通仿制药。目前国内销售额最高的抗体药物是曲妥珠单抗,在进入医保后才超过了50亿元,与全球近80亿美元的销售峰值相比差距较大,国内的渗透率仍然远低于欧美。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..