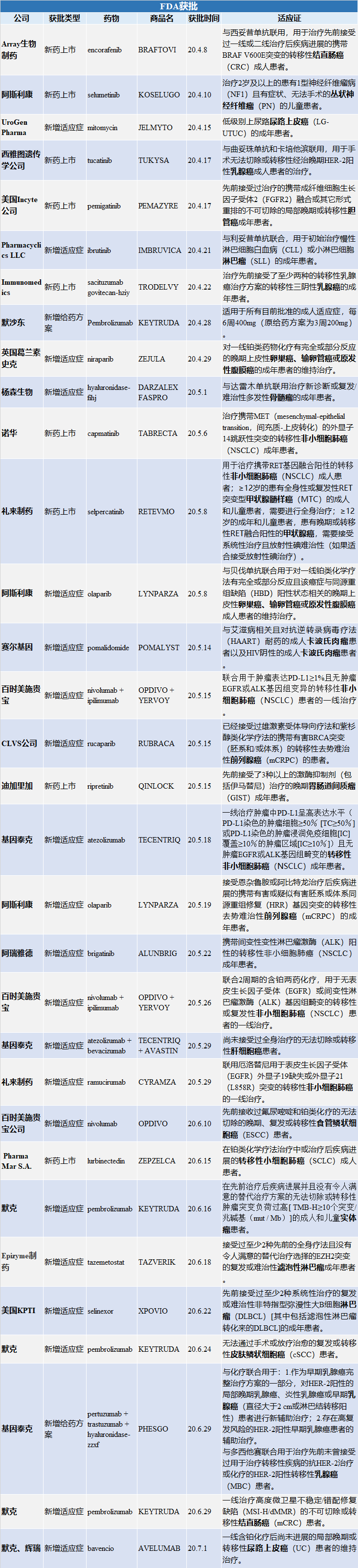
虽然新冠疫情仍在持续,但国际上对新药的审批和上市却丝毫没有放慢脚步,我们汇总了第二季度获得FDA、NMPA批准的抗肿瘤相关药物,其中FDA共批准了32款抗肿瘤药物,9款为新药上市,21款为新增适应症;NMPA共批准了10款抗肿瘤药物,5款为新药上市,4款为新增适应症,所覆盖领域包括非小细胞肺癌、乳腺癌、结直肠癌、胆管癌、胃肠道间质瘤等多个癌种。越来越多靶向药物的获批上市助力了肿瘤精准医学的快速发展,也为晚期肿瘤患者带来了更多的福音。
FDA获批
NMPA获批
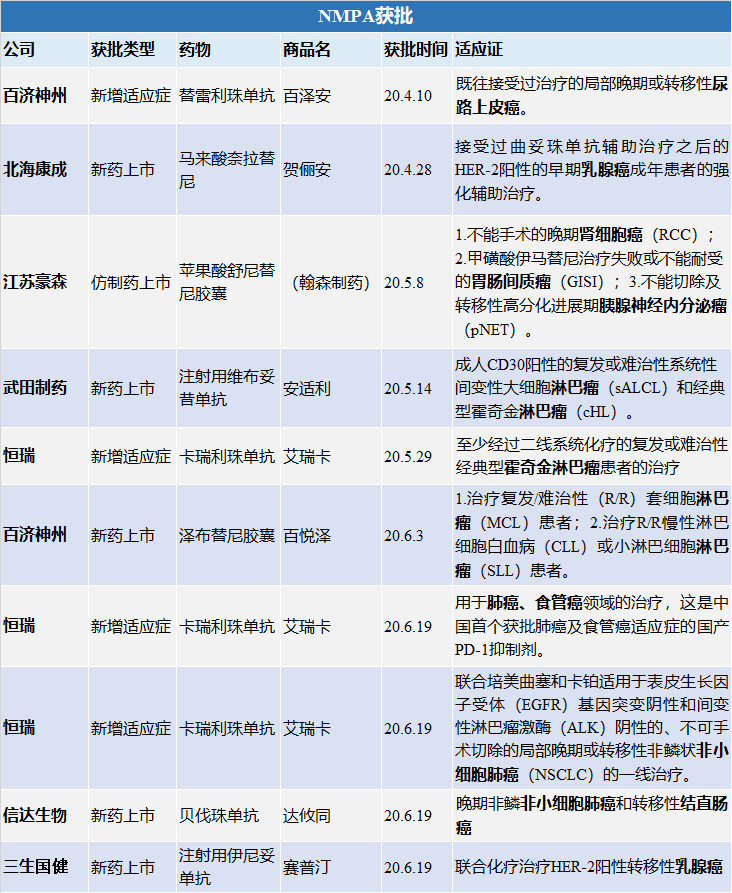
FDA新药上市
01
【Array生物制药】
康奈菲尼(encorafenib,商品名:BRAFTOVI)
与西妥昔单抗联用,用于治疗先前接受过一线或二线治疗后疾病进展的携带BRAF V600E突变的转移性结直肠癌(CRC)成人患者。
临床试验:BEACON CRC(NCT02928224)
患者情况:采用随机、多中心、主动控制、开放标签的临床试验,招募先前接受过一线或二线治疗后疾病进展的携带BRAF V600E突变的转移性结直肠癌(CRC)患者。对入组患者进行随机分配,试验组(220例)接受“康奈菲尼(300 mg 口服 qd)+西妥昔单抗”联合治疗,对照组(221例)接受“伊立替康+西妥昔单抗”联合治疗。
疗效数据:
“康奈菲尼+西妥昔单抗”试验组的中位OS为8.4个月(95% CI: 7.5, 11.0),对照组为5.4个月(95% CI:4.8,6.6,HR=0.60,95% CI: 0.45,0.79,p=0.0003)。试验组的中位PFS为4.2个月(95% CI:3.7,5.4),对照组为1.5个月(95% CI:1.4,1.7,HR=0.40,95%CI:0.31,0.52,p
试验组与对照组的ORR分别为20%(95% CI: 13%,29%)和2%(95% CI: 0%,7%)。
试验组的中位DOR为6.1个月(95% CI: 4.1,8.3),对照组未达到中位DOR(95% CI: 2.6, NR)。
不良反应:最常见的不良反应(≥25%)为疲劳,恶心,腹泻,痤疮性皮肤炎,腹痛,食欲下降,关节痛和皮疹。
02
【阿斯利康】
司美替尼(selumetinib,商品名:KOSELUGO)
用于治疗2岁及以上的患有1型神经纤维瘤病(NF1)且有症状的、无法手术的丛状神经纤维瘤(PN)的儿童患者。
临床试验:SPRINT(NCT01362803)
疗效数据:患者每日两次口服selumetinib单药治疗,结果显示,客观缓解率(ORR)达到了66%(n = 33/50;95%CI:51,79)。所有患者都有部分缓解(PR),反应持续时间(DoR)≥12个月的患者高达82%。
不良反应:最常见的不良反应(≥40%)是呕吐,皮疹,腹痛,腹泻,恶心,皮肤干燥,疲劳,肌肉骨骼疼痛,发烧,痤疮,口腔炎,头痛,甲沟炎和瘙痒。
03
【西雅图遗传学公司】
图卡替尼(tucatinib,商品名:TUKYSA)
与曲妥珠单抗和卡培他滨联用,用于手术无法切除或转移性经治晚期HER-2阳性乳腺癌成人患者的治疗。
临床试验:HER-2CLIMB(NCT02614794)
患者情况:招募了612例先前接受过曲妥珠单抗、帕妥珠单抗和曲妥珠单抗-美坦新偶联物治疗的HER-2阳性转移性乳腺癌患者。试验组(410例)患者接受“图卡替尼(300mg bid)+曲妥珠单抗+希罗达”治疗;对照组(202例)患者接受“安慰剂+曲妥珠单抗+希罗达”治疗。
疗效数据:
试验组患者(接受图卡替尼治疗)的中位PFS为7.8个月(95% CI: 7.5,9.6),对照组患者为5.6个月(95% CI: 4.2,7.1),HR=0.54(95% CI:0.42,0.71,P中位OS为21.9个月(95% CI: 18.3,31.0),对照组为17.4个月(95% CI: 13.6,19.9),HR=0.66(95% CI:0.50,0.87,P=0.00480)。
试验组和对照组的可测量疾病患者的确定ORR分别为40.6%(95% CI: 35.3,46.0)和22.8%(95% CI: 16.7,29.8)(p=0.00008)。
不良反应:最常见的不良反应(≥20%)是腹泻,掌-跖红肿,恶心,疲劳,肝毒性,呕吐,口腔炎,食欲下降,腹痛,头痛,贫血和皮疹。图卡替尼还可引起严重的腹泻和肝毒性。
04
【美国Incyte公司】
培米加替尼(pemigatinib,商品名:PEMAZYRE)
用于先前接受过治疗的携带成纤维细胞生长因子受体2(FGFR2)融合或其它形式重排的不可切除的局部晚期或转移性胆管癌成年患者。pemigatinib是全球首个并且唯一一个获批上市的胆管癌靶向药物。
临床试验:FIGHT-202(NCT02924376)
患者情况:多中心、开放标签、单臂临床试验,招募了107名无法切除的局部晚期或转移性胆管癌患者,患者接受“培米加替尼(Pemigatinib) 13.5mg 口服 每日一次”治疗,连续口服14天,之后停药7天。
疗效数据:
以总体反应率(ORR)和反应持续时间为主要疗效结果指标。在107例患者中,ORR为36%(95% CI: 27%,45%),其中包括3例完全缓解。中位DOR为9.1个月,38例患者中有24例(63%)反应持续时间≥6个月,有7例患者(18%)的反应持续时间≥12个月。
不良反应:最常见的不良反应(≥20%)是高磷血症,脱发,腹泻,指甲毒性,疲劳,消化不良,恶心,便秘,口腔炎,干眼,口干,食欲下降,呕吐,关节痛,腹痛,低磷血症,背部疼痛和皮肤干燥。眼毒性和高磷血症是培马加替尼的重要风险。
05
【Immunomedics公司】
sacituzumab govitecan-hziy(商品名:TRODELVY)
用于治疗先前接受了至少两种的转移性乳腺癌治疗方案的转移性三阴性乳腺癌的成年患者。
临床试验:IMMU-132-01(NCT 01631552)
患者情况:多中心、单臂临床试验,108名入组患者患者在21天的治疗期内,第1和8天接受sacituzumab govitecan-hziy治疗,治疗剂量为10mg/kg。每8周进行一次肿瘤成像,患者接受治疗直至疾病进展或不能耐受治疗。
疗效数据:整体缓解率(ORR)为33.3%(95% CI: 24.6,43.1)。中位反应持续时间为7.7个月(95% CI: 4.9,10.8)。
不良反应:最常见的不良反应(≥25%)为恶心,中性粒细胞减少,腹泻,疲劳,贫血,呕吐,脱发,便秘,皮疹,食欲下降和腹痛。Sacituzumab govitecan-hziy还可引起严重的中性粒细胞减少和腹泻。
06
【诺华】
卡马替尼(capmatinib,商品名:TABRECTA)
用于治疗携带MET(mesenchymal-epithelial transition,间充质-上皮转化)的外显子14跳跃性突变的转移性非小细胞肺癌(NSCLC)成年患者。
临床试验:GEOMETRY mono-1 trial (NCT02414139)
患者情况:
多中心、非随机、开放标签、多队列研究,招募97位确定携带MET外显子14跳跃性突变的转移性NSCLC患者,患者接受“卡马替尼 400mg PO bid”治疗,直至疾病进展或者出现无法耐受的毒性。
疗效数据:
在28名初治患者中,ORR为68%(95%CI:48,84),反应持续时间为12.6个月(95%CI:5.5,25.3)。在既往接受过治疗的69位患者中,ORR为41%(95%CI:29,53),反应持续时间为9.7个月(95%CI:5.5,13.0)。
不良反应:最常见的不良反应(≥20%)是周围水肿,恶心,疲劳,呕吐,呼吸困难和食欲下降。卡马替尼还可引起间质性肺疾病,肝毒性,光敏性和胚胎胎儿毒性。
07
【礼来制药】
selpercatinib(商品名:RETEVMO)
1.携带RET基因融合阳性的转移性非小细胞肺癌(NSCLC)成人患者;
2.≥12岁的患有全身性或复发性RET突变型甲状腺髓样癌(MTC)的成人和儿童患者,需要进行全身治疗;
3.≥12岁的成年和儿童患者,患有晚期或转移性RET融合阳性的甲状腺癌,需要接受系统性治疗且放射性碘难治性(如果适合接受放射性碘治疗)。
临床试验:LIBRETTO-001
患者情况:多中心、开放标签、多队列临床试验,使用NGS、PCR或荧光原位杂交法前瞻性地确定RET基因改变的鉴定。
疗效数据:
1.在105例既往接受过铂类药物化疗的RET融合阳性NSCLC成人患者中,整体的客观缓解率(ORR)为64%。在获得缓解的患者中,81%的患者持续缓解时间(DOR)至少为6个月。该研究还对39例RET融合阳性NSCLC初治患者进行了疗效评价,ORR为84%,58%获得缓解的患者的DOR至少为6个月。
2.在≥12岁的携带RET突变的MTC成人和儿童患者中,88例初治患者中,ORR为73%,61%获得缓解的患者DOR至少为6个月。55例经治患者的ORR为69%,76%获得缓解的患者DOR至少为6个月。
3.在治疗≥12岁的RET融合阳性甲状腺癌成人和儿童患者时,19例接受过放射性碘治疗和至少一种其它疗法治疗的患者的ORR为79%,87%获得缓解的患者DOR至少为6个月。8例只接受过放射性碘治疗的患者的ORR为100%,75%获得缓解的患者DOR至少6个月。
不良反应:最常见的不良反应(≥25%)包括实验室异常(天冬氨酸转氨酶增加、丙氨酸转氨酶增加、葡萄糖增加、白细胞减少、白蛋白减少、钙减少、肌酐增加、碱性磷酸酶增加、血小板减少、总胆固醇增加)、高血压、疲劳、水肿、皮疹和便秘。
08
【迪加里加制药公司】
瑞普替尼(ripretinib,商品名:QINLOCK)
用于治疗先前接受了3种以上的激酶抑制剂(包括伊马替尼)治疗的晚期胃肠道间质瘤(GIST)成年患者。
临床试验:INVICTUS(NCT03353753)
患者情况:多中心、随机(2:1)、双盲试验。试验组患者接受“瑞普替尼 150mg PO qd”治疗,对照组患者口服安慰剂,直至疾病进展或者出现无法耐受的毒性。
疗效数据:
与对照组(口服安慰剂)相比,试验组(口服瑞普替尼)的PFS在统计学上有显著改善(HR 0.15; 95% CI: 0.09,0.25; p中位PFS为6.3个月(95% CI: 4.6,6.9),而对照组为1.0个月(95% CI: 0.9,1.7)。试验组的ORR为9%(95% CI: 4.2,18),而对照组为0%(95% CI: 0,8)。试验组的中位OS为15.1个月(95% CI: 12.3,15.1),对照组为6.6个月(95% CI: 4.1,11.6),HR=0.36(95% CI: 0.21,0.62)。
不良反应:最常见的不良反应(≥20%)为脱发,乏力,恶心,腹痛,便秘,肌痛,腹泻,食欲下降,掌-跖红斑和呕吐。瑞普替尼的其他重要风险包括新发的原发性皮肤恶性肿瘤,高血压和心脏功能障碍。
09
【Pharma Mar S.A.】
lurbinectedin(商品名:ZEPZELCA)
用于治疗在铂类化学疗法治疗中或治疗后疾病进展的转移性小细胞肺癌(SCLC)成人患者。
临床试验:PM1183-B-005-1(NCT02454972)
患者情况:多中心、开放标签、多队列的临床试验,105名患者患者接受"Lurbinectedin 3.2 mg/m2静脉输注q3w"治疗,直至疾病进展或出现无法接受的毒性。
疗效数据:在105例患者中,ORR为35%(95%CI:26%,45%),中位反应持续时间(DoR)为5.3个月(95%CI:4.1、6.4),独立审查委员会(IRC)评估的ORR为30%(95%CI:22%,40%),中位DoR为5.1个月(95%CI:4.9,6.4)。
不良反应:最常见的不良反应(≥20%)、包括实验室异常(骨髓抑制、乏力、肌酐增加、丙氨酸转氨酶增加、葡萄糖增加)、恶心、食欲下降、肌肉骨骼疼痛、白蛋白减少、便秘、呼吸困难、钠减少、天冬氨酸增加氨基转移酶、呕吐、咳嗽、镁减少和腹泻。
NMPA新药上市
01
【北海康成】
马来酸奈拉替尼(商品名:贺俪安)
用于接受过曲妥珠单抗辅助治疗之后的HER-2阳性的早期乳腺癌成年患者的强化辅助治疗。
获批背景:
奈拉替尼是全球首个且唯一用于HER-2阳性早期乳腺癌强化辅助治疗的小分子药物,其作用靶点广泛,通过胞内不可逆结合,同时抑制HER1/HER-2/HER4信号通路。在ExteNET的III期研究中,5年随访数据表明:患者在接受曲妥珠单抗治疗后,继续口服一年奈拉替尼进行强化辅助治疗,能够降低27%的复发风险,而对于同时具有雌激素/孕激素受体阳性(ER/PR 阳性)的患者,使用奈拉替尼能够降低5年复发风险达42%,获益更为显著。
02
【武田制药】
注射用维布妥昔单抗(商品名:安适利)
用于治疗成人CD30阳性的复发或难治性系统性间变性大细胞淋巴瘤(sALCL)和经典型霍奇金淋巴瘤(cHL)。
获批背景:
维布妥昔单抗在中国的获批是基于三项临床研究SG035-0004、SG035-0003、C25007的数据。在SG-035-0004研究中,针对复发或难治性间变大细胞淋巴瘤,58例患者中97%的复发或难治性系统性间变性大细胞淋巴瘤患者可实现肿瘤缩小,其5年生存率提高至60%;在SG035-0003研究中,94%的复发或难治性经典型霍奇金淋巴瘤的患者可实现肿瘤缩小,其中位总生存期(mOS)从历史27.6个月提升至40.5个月;在C25007研究中,在既往至少接受一次化疗方案且开始维布妥昔单抗治疗时不适合进行干细胞移植(SCT)或多药化疗的复发或难治性经典型霍奇金淋巴瘤患者(n=60)中,客观缓解率(ORR)为50%(95% CI,37: 63%)
03
【百济神州】
泽布替尼胶囊(商品名:百悦泽)
用于治疗:
1.复发/难治性(R/R)套细胞淋巴瘤(MCL)患者;
2.R/R慢性淋巴细胞白血病(CLL)或小淋巴细胞淋巴瘤(SLL)患者。
获批背景:
I期BGB-3111-206研究数据显示,泽布替尼用于治疗复发/难治性(R/R)MCL的ORR达84%,包括59%的完全缓解以及24%的部分缓解。III期SEQUOIA研究C组数据显示,泽布替尼对于17p染色体缺失的初治CLL/SLL患者ORR达92.7%,部分缓解(PR)率为78.9%,伴有淋巴细胞增多的PR率为11.9%,完全缓解(CR)率为1.9%。
04
【信达生物】
贝伐珠单抗(商品名:达攸同)
用于治疗晚期非鳞非小细胞肺癌和转移性结直肠癌。
获批背景:
达攸同抗肿瘤的原理机制是通过阻断血管内皮生长因子VEGF,抑制肿瘤的血管新生,切断肿瘤区域的供血,抑制肿瘤的生长和转移,诱导肿瘤细胞凋亡,从而达到抗肿瘤的治疗效果。这是信达生物继达伯舒 (信迪利单抗注射液)之后第二个上市的单克隆抗体药物,并且信达生物正在进行的达攸同联合达伯舒治疗晚期肝细胞癌的Ib期初步临床试验结果,将于今年ASCO年会上公布。
05
【三生国健】
注射用伊尼妥单抗(商品名:赛普汀)
联合化疗用于治疗HER-2阳性的转移性乳腺癌。
获批背景:
这是中国自主研发上市的首个创新抗HER-2单抗药物。体外研究显示,伊尼妥单抗的Fab段与曲妥珠单抗一致,通过Fc段修饰和生产工艺优化,具有更强ADCC效应,更好地实现了抗HER-2单抗药物的治疗目标——既可以阻断HER-2通路,直接抑制肿瘤细胞增殖和生长;又可以诱导ADCC效应,通过机体免疫系统识别和杀伤肿瘤细胞。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..