根据世界卫生组织的统计,罕见病并不罕见:全球范围内,约有5000-8000种罕见病。将这些患者加在一起,总人数已接近4亿。也就是说, 我们身边每不到20个人里,就有1名罕见病患者。 遗憾的是,在那么多罕见病里,仅有不到10%有已批准的治疗药物或方案。不过随着对罕见病理解的不断加深,监管政策的大力扶持,以及研发企业的高度重视,在 最近的十多年里,全球范围内的罕见病治疗格局发生了巨大的变化。 在今天的这篇文章里,药明康德内容团队将以美国FDA的“孤儿药资格”(Orphan Drug Designation)为切入点,和各位读者聊聊这些年来的积极进展。
5000多个孤儿药资格
曾经,罕见病是“无药可治”的同义词。在1983年的《孤儿药法案》出台前,整整10年的时间里,仅有10种罕见病药物上市。而在1983年1月1日至2019年10月31日这段时间内,其官方数据库显示,美国 FDA共颁发了5219个“孤儿药资格”(注: 同一药物/疗法针对不同适应症,可以获得多个孤儿药资格), 最终获批的药物数量为843个,可谓是天壤之别。
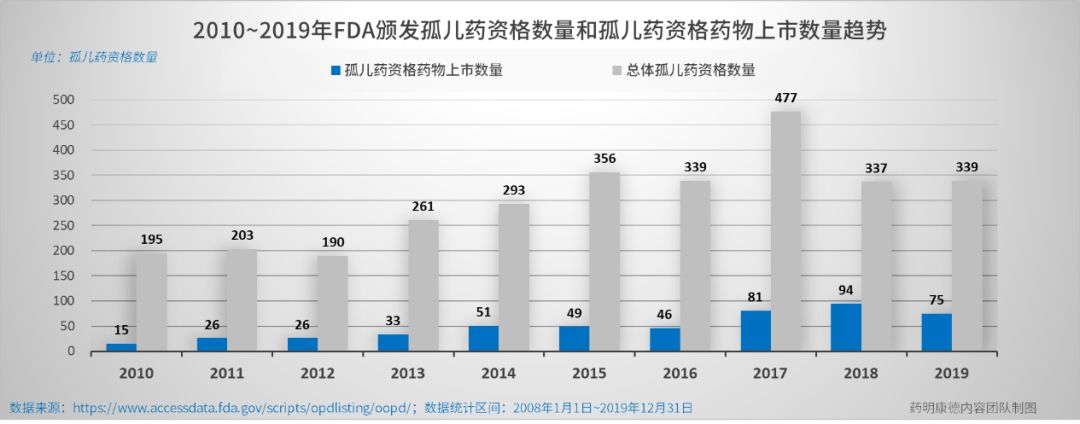
值得一提的是,在孤儿药的研发热潮之下,业界对于罕见病的热情正维持在高位。过去的10年里,FDA颁发的“孤儿药资格”数量以7%的年复合增长率逐年增加,2017年创下历史最高,总量达到477个,较2010年翻了2.5倍,可见越来越多的创新药物研发正集中到罕见病领域。曾获“孤儿药资格”的药物获批上市的数量以16%的年复合增长率快速上升,2018年全年共有94款(注:针对不同适应症,一款药物可多次获批)。2019年,这一数字也达到了75款。
近一半的孤儿药占比率
2010年至今,美国FDA共批准了380个新药上市,与上一个十年相比,数量增幅达到60%( 此处统计的新药包括CDER批准的NME,以及CBER批准的基因疗法、细胞疗法和重组疫苗)。 其中获得孤儿药资格认定的上市新药达到165个,占近十年FDA获批新药总数的43%。
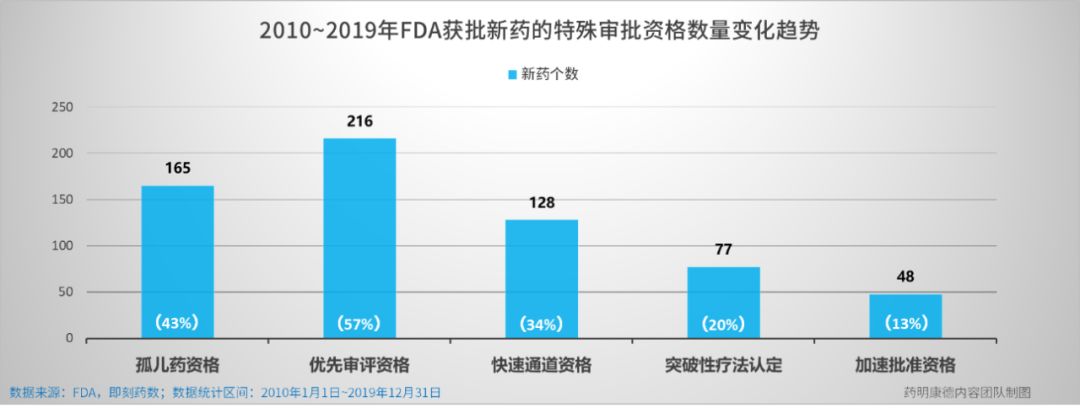
过去的10年里,FDA新药获批数量以7%的年复合增长率在逐年增加,与此同时,获得孤儿药资格的新药数量以年复合14%的速度迅猛上升,每年孤儿药占比率更是不断攀高, 2018年创下历史最高,孤儿药占比率达到58%。
罕见病实现重大突破
在过去的10年间, 共有54款同时获得突破性疗法和孤儿药资格的FDA新药,覆盖42种疾病,其中我们发现很多难治罕见病都实现了治疗上的突破,譬如在《中国第一批罕见病目录》的121种疾病里,已有11种罕见病迎来了FDA批准的新药,总数达15款,且 70%的上市时间都集中在2017和2018年,侧面见证了加快孤儿病或罕见病新药上市申请这一政策的巨大成效。
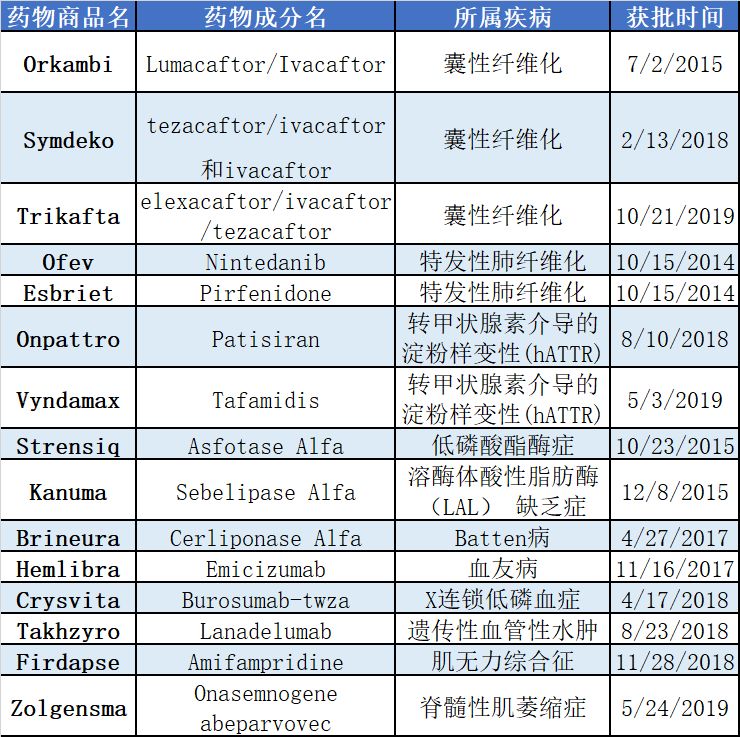
▲《中国第一批罕见病目录》中,已有11种罕见病具有FDA批准的上市新药(数据来源:公开资料,药明康德内容团队制图)
结语
综上所述,在过去的10年里,罕见病治疗领域有着喜人的发展。无论是获批药物的数量,还是医药企业的研发热情,都维持在高位。但我们也需要意识到,罕见病的数目庞大,还有大量的空白需要去创新、去突破。这也给很多开发小分子药物和生物制品的传统医药公司,或是专攻基因疗法的生物技术新锐留下了巨大的发展空间。我们期待未来将有更多罕见病治疗药物出现,造福全球的罕见病患者。
注:本文旨在介绍医药健康研究进展,不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
数据来源:即刻药数、FDA官网
参考资料:
[1] 葛琳, 魏翠洁, 史录文, et al.(2018),中国罕见病用药现状研究,北京医学,DOI:CNKI:SUN:BJYX.0.2018-05-016
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..