半个多世纪前,年轻的李文渝(Virginia Man-Yee Lee)孤身一人来到伦敦,前往英国皇家音乐学院主修钢琴表演。如同那个时代许多出身于中产家庭的女性一样,她的人生道路早早被家人所规划:学成之后,她将凭借才华赢得某位豪门公子的青睐,随后相夫教子,扮演好传统所赋予的角色。

▲李文渝教授(Courtesy of Dr. Virginia Man-Yee Lee;Credit:Penn Medicine)
在异国,这名十多岁的亚洲女孩感到无比的迷惘。她清楚地知道,这不是她想要的人生。但除了遵循父母之命,还有什么其他选择呢?她的心里没有答案。那时的李文渝不会想到,几十年后,她会成为全球神经退行性疾病领域当之无愧的先驱。她更不会想到,今日她会走过“科学突破奖” (Breakthrough Prize)的红毯,接过“生命科学突破奖”的奖杯。这是有着“科学界奥斯卡”之称的重磅奖项,奖金额约为诺贝尔奖的三倍,为全球科学奖项之最。
从钢琴表演到生物化学
李文渝于1945年出生于重庆,这座山城的名字也正是“渝”字的由来。她的父亲是一名生活在美国的华人,在二战期间志愿加入空军,回到中国抗击日本的侵略。在一次战斗中,他的座机被击落,本人也因此负伤,却如同小说情节一般,由此结识了李文渝的母亲。两人婚后共育有三个子女,李文渝是家中的小女儿。
二战结束之后,他们全家移居香港:父亲在香港与美国西海岸之间来回经商,母亲则在家照顾孩子。10多岁那年,李文渝的大部分亲人都跟随父亲去了美国,只有她和一名哥哥留在香港的祖母家,以完成高中学业。“所以在我成长的过程中,身边没有多少可以学习的榜样,也没有太多人管我和指导我。” 在药明康德内容团队的专访中,李文渝教授说道:“学习是我唯一能做的事情。”
在母亲的安排下,高中毕业后,李文渝前往英国学习钢琴表演。离开英国时,她却带着生物化学的硕士学位。说到这一令人惊讶的转变,李文渝教授向我们袒露了选择背后的思考:“我不想学钢琴。在高中时我就很喜欢科学,所以就跑去伦敦的大学里学科学。一开始我选的是化学,但后来我觉得纯化学有点枯燥,最后改成了生物化学。”
“硕士毕业之后,我觉得想要有足够的钱来养活自己,还是要读一个博士。” 李文渝教授回忆道。她先是在加州大学旧金山分校(UCSF)获得了生物化学的博士学位,又前往荷兰与波士顿接受更多训练。也正是在波士顿,她遇上了自己一生的伴侣——约翰·特罗扬沃斯基(John Trojanowski),他是一位优秀的神经病理学家。
“约翰是那个真正鼓励我去追求科学职业的人,” 李文渝教授说道:“我们那一代的女性,很多都不知道自己真正想做什么。我的丈夫告诉我,你有足够的天赋和勇气,应该去尝试科学道路。他给了我很多自信,我们之间也合作得非常愉快。”
然而命运并不想让她的科学生涯一帆风顺。在从事科学工作的最初几年,李文渝教授走得有些磕磕绊绊。她先是在一家药企度过了并不愉快的两年时光,又在加入宾夕法尼亚大学后,面临着科研资金短缺的风险。为了给自己“留条后路”,她特地在沃顿商学院补读了一个MBA的学位,以防“将来有一天失业”。
想象中的失业并没有到来。相反,神经退行性疾病领域的一颗新星正在冉冉升起。
唯一的女性得主
在宾夕法尼亚大学,李文渝教授与特罗扬沃斯基教授夫妇将研究方向定为神经退行性疾病。当时,阿尔茨海默病的社会负担正逐渐呈现,吸引了无数科学家的关注。“30多年前,我们对神经退行性疾病背后的致病蛋白一无所知。我们不知道阿尔茨海默病的沉积里头有着β-淀粉样蛋白,不知道神经原纤维缠结里是tau蛋白,也不知道路易小体里有α-突触核蛋白,” 李文渝教授回忆道:“但我和John的技能非常互补,所以我们决定合作,看看能不能从不同的角度去做出贡献,找到疾病背后的致病分子。”
1991年,这支团队很快迎来了突破。在阿尔茨海默病患者大脑里,他们用一系列生化和免疫的方法,证实神经原纤维缠结里的特异性蛋白正是tau。这项研究刊登在了顶尖学术期刊《科学》上,刷新了人们对tau蛋白的认知。

▲这项研究刷新了人们对tau蛋白的认知(图片来源:参考资料[1])
而这只是这支高产团队深入研究神经退行性疾病的一个开端。2000年左右,他们将注意力移向了一种叫做额颞叶痴呆(frontotemporal lobar degeneration,缩写FTLD)的疾病上。“当时我们发现只有一半患者的神经原纤维缠结里有tau蛋白的积聚,这个现象让我们很惊讶。如果剩下一半患者的大脑病变里没有tau蛋白,那是什么导致了他们的疾病呢?” 李文渝教授问道。
经过数年的纯化与分析,他们找到了一种叫做TDP-43的蛋白质。抗体结合实验证实,这种蛋白在患者的病灶处有着大量积聚。随后,这支团队用基因改造的方法,开发了一种小鼠动物模型,使其表达突变的TDP-43。果不其然,这些动物表现出了和人类患者类似的痴呆症状。进一步的分析则确认,无论是在突变的小鼠还是人类的患者中,TDP-43都失去了正常的细胞核定位,出现在了细胞质中。这是一种RNA结合蛋白,参与了转录和翻译的调控,与常见的α-突触核蛋白或tau蛋白的功能截然不同。这也是人类首次发现RNA结合蛋白在神经退行性疾病中的作用。
在tau蛋白与TDP-43蛋白外,李文渝教授与特罗扬沃斯基教授夫妇也在α-突触核蛋白上做出了许多突破性的发现。“我们把合成的α-突触核蛋白纤维注射入了野生型小鼠的大脑内,发现它们能够在细胞之间传播,并产生类似于路易小体的结构。这是我们最重要的发现之一。” 李文渝教授评论道。这个实验尽管简洁,却提供了有力的科学依据,让我们能够确认“路易小体产生”与“多巴胺能神经元退化”之间的因果关系,是帕金森病领域的重大突破。它在2012年同样登上了《科学》杂志。
2018年,这支团队又在《自然》杂志上公布了另一个重磅发现:在帕金森病和多系统萎缩(multiple system atrophy)中,患者的脑区里虽然都有大量α-突触核蛋白积聚,两者的结构与性质却迥然不同。“我们发现同样是α-突触核蛋白,其不同的变异体(strain)可能由于翻译后修饰的不同会产生不同的折叠构象,导致不同的疾病形态,” 李文渝教授解释道:“所以不同的神经退行性疾病,也有可能是致病蛋白的不同变异体所导致的,这改变了我们过去的简单认知。”

▲李文渝教授是今年“生命科学突破奖”5名得主中唯一一名女性(图片来源:“科学突破奖”官方网站)
过去10多年来在神经退行性疾病领域的一系列重量级发现和突破,吸引了2017年“科学突破奖”得主Huda Zoghbi教授的关注。在她的推荐下,李文渝教授摘得了“生命科学突破奖”的桂冠,获奖评语是“发现了额颞叶痴呆和肌萎缩侧索硬化症(ALS)中TDP-43蛋白的聚集,并揭示帕金森病和多系统萎缩中,不同类型细胞内α-突触核蛋白具有不同形式” 。值得一提的是,在今年获奖的5位杰出生物学家里,李文渝教授是唯一的女性。
未来在哪里?
从tau蛋白,到TDP-43蛋白,再到α-突触核蛋白,“很多人可能会惊讶,我为什么要研究那么多不同的蛋白,为什么要同时研究那么多不同的神经退行性疾病。”在李文渝教授看来,这是因为它们有共同的致病机理——无论是阿尔茨海默病、帕金森病、还是额颞叶痴呆,都存在许多致病蛋白的积聚。
正是由于有着研究多种疾病、多种致病蛋白的丰富经验,李文渝教授对这些疾病的复杂性有着深刻的认识。聊到最近一些阿尔茨海默病治疗中的进展,她表示“靶向β-淀粉样蛋白的做法的确有一定科学基础,看起来有其合理性。”这是因为我们发现这些蛋白很早就会在患者的大脑里积聚,远早于症状出现的时间。“他们可能在60多岁出现痴呆症状,但在40多岁时,大脑里就有β-淀粉样蛋白的沉积了。所以人们很自然会想到,如果能减少β-淀粉样蛋白的产生,就可以缓解后续的症状。”
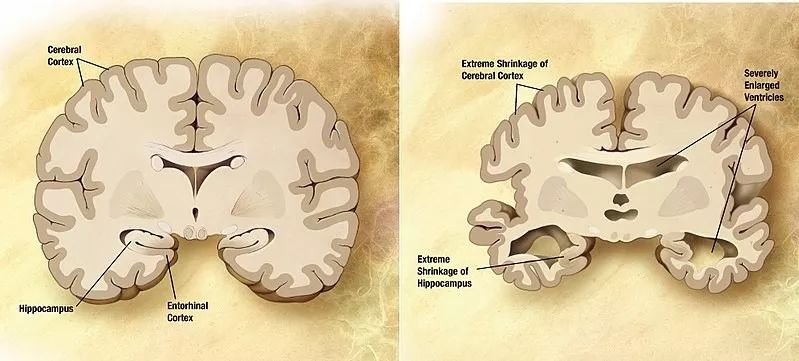
▲治疗阿尔茨海默病等神经退行性疾病,关键可能是“组合疗法”和“生物标志物”(图片来源:[Public domain])
李文渝教授认为这个理论看起来很直接,但可能把事情想得太简单了。“如果这些药物真的能取得成功,那我会感到很高兴,” 李文渝教授说道:“但在我看来,这些神经退行性疾病背后的机理应该更加复杂。当然,在小鼠实验里,我们取得了很好的治疗效果,但人类是一种完全不同的生物,很难想象同样简单的治疗就能取得成功。如果靶向β-淀粉样蛋白的疗法没有效果,我们也应该去看看大脑里的其他致病蛋白。”
而神经退行性疾病的未来,可能属于两个关键词:组合疗法与生物标志物。组合疗法指同时靶向不同的致病蛋白,比如在治疗阿尔茨海默病时,需要同时针对tau蛋白和β-淀粉样蛋白等不同靶点。“这些都是目前容易想到的靶点,但我们还需要其它新的靶点,这会取得非常不一样的结果。”
而生物标志物的寻找则可能更为重要。对于很多神经退行性疾病来说,一大难点在于寻找到患者。如果能用成像的方法,或是血清检测的手段找到疾病的生物标志物,对整个领域会有很大的帮助。“这不但能让我们做出清楚的临床诊断,还可以知道治疗是不是起了效果,” 李文渝教授说道:“但在生化上,这样的生物标志物非常难研究。所以这一块需要所有人的参与和合作。”
在基础研究方面,李文渝教授与中国科学技术大学的申勇教授课题组,以及香港科技大学的叶玉如(Nancy Ip)教授课题组有着合作。而在临床疗法的开发上,一家名为AC Immune的医药公司也已与其达成合作协议,开发针对TDP-43的抗体与小分子药物,缓解FTLD患者的病情。“我们研究了许多90岁以上的老年人,TDP-43在他们的大脑里有很多积聚。在海马区中,这个趋势尤为明显。” 李文渝教授补充道。
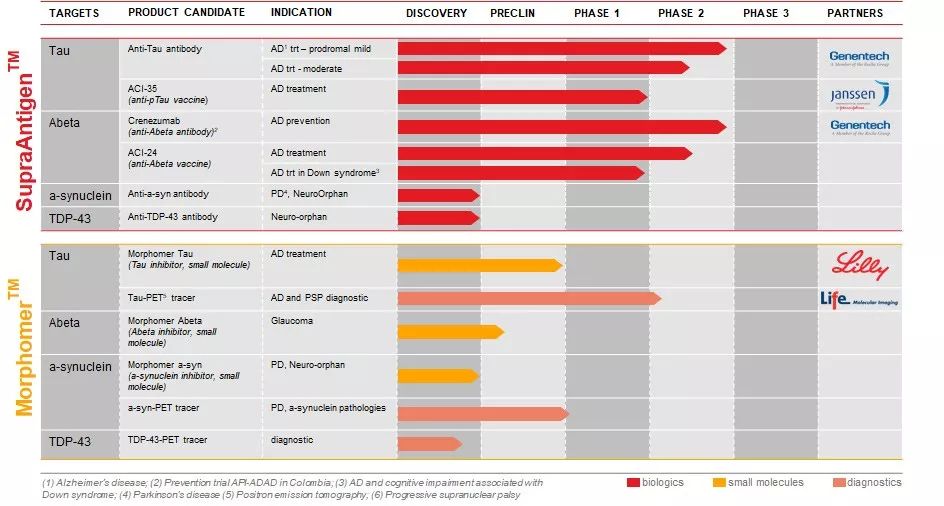
▲AC Immune公司正在开发针对TDP-43的药物(图片来源:AC Immune官方网站)
而在科研院所与医药公司之外,李文渝教授指的“所有人”还包括患者及其家属。“在美国,许多患者家庭希望得到真正的诊断,因此同意做大脑解剖研究,确认病因,这给科学家的工作带来了宝贵的资源。出于传统文化的原因,过去中国患者不大习惯对大脑进行解剖。但随着年轻一代思想的逐渐开放,这一现象有望在未来得到改善。这也将给大脑研究带来突破,让中国成为一个脑科学研究的大国。”
诚然,神经退行性疾病极为复杂,很难预测未来会发生些什么,但“如果大家都能齐心协力,就有机会推进这个领域的发展”。在李文渝教授看来,如果一家公司的研究方向遭受挫折,其他公司可以选择不同的路径,从其他角度进行探索。“如果说在探索的道路上,何时能取得成果,我相信答案会是‘现在’,因为现在的疾病模型要比过去出色许多,” 李文渝教授说道:“我期待更多医药公司能进入这个领域,启动临床试验,并在5-10年里观察到一些积极的疗效。”
后记
现年74岁的李文渝教授是宾夕法尼亚大学神经退行性疾病研究中心的主任,她的丈夫特罗扬沃斯基教授则是联合主任,两人每天都还奋战在科研的第一线,不时由于科学上的观点分歧进行善意而激烈的探讨。熟识他们的朋友,往往为其旺盛的科学激情所折服。
如今,这对夫妇正将他们的科学热情传递给未来的学者。“我们的实验室里有许多年轻人,最年轻的还只是高中生。我的想法是让他们尽早接触科学,让他们看看是不是感兴趣,是否考虑把科学作为职业。如果他们不喜欢科学,那也没有问题,因为没有人会对所有事情都感兴趣。但我至少让他们有机会接触一下这个环境。”在年轻时缺少选择的李文渝教授,想要让年轻人少走一些弯路。

▲李文渝教授与约翰·特罗扬沃斯基教授执掌了宾夕法尼亚大学的神经退行性疾病研究中心(Courtesy of Dr. Virginia Man-Yee Lee;Credit:Penn Medicine)
对于年轻的女性科学家,李文渝教授也鼓励她们勇敢地涉足科学领域:“在你职业生涯的某一阶段,有可能是刚刚获得第一份工作的时候,会有生养孩子的压力,这会带来很多困难。但只要过了这个阶段,当孩子长大后,依然可以有30-40年的时光来做出很好的科研。科学发现的喜悦无以伦比,而且还能帮助到别人。这真的很有趣,也会给你带来很大的成就感。”
[1] VM Lee et al., (1991), A68: a major subunit of paired helical filaments and derivatized forms of normal Tau, Science, DOI: 10.1126/science.1899488
[2] Mark S Forman et al., (2007), TDP-43: A Novel Neurodegenerative Proteinopathy, Curr Opin Neurobiol, DOI: 10.1016/j.conb.2007.08.005
[3] Kelvin C. Luk et al., (2012), Pathological α-Synuclein Transmission Initiates Parkinson-like Neurodegeneration in Non-transgenic Mice, Science, DOI: 10.1126/science.1227157
[4] Chao Peng et al., (2018), Cellular Milieu Imparts Distinct Pathological α-Synuclein Strains in α-Synucleinopathies, Nature, DOI: 10.1038/s41586-018-0104-4
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..