随着仿制药质量和疗效一致性评价等政策的出台,临床试验的关注度不断提高。
1、药物类别
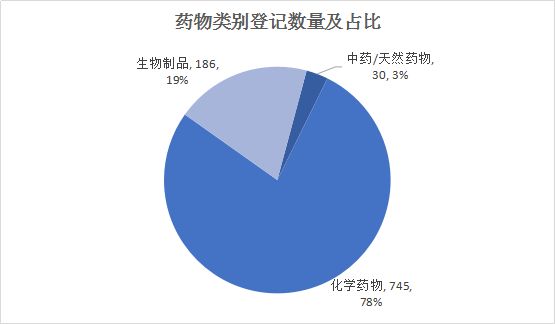
2019年上半年,CDE药物临床试验登记平台总共公示961个临床试验。其中,化学药物 745 个,生物制品 186 个,中药/天然药物 30个。
2、国内试验和国际多中心试验
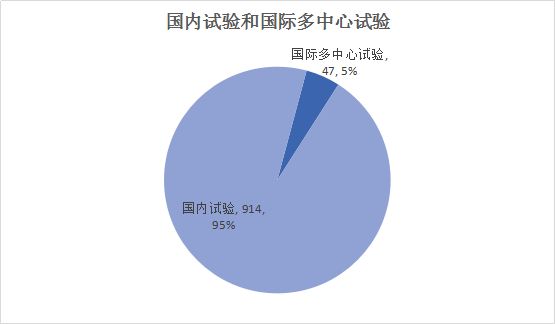
目前药物临床试验平台中的临床试验多以国内试验为主,2019年上半年总计47个国际多中心试验,大多都是3期试验,主要研究安全性和有效性。从
药品来看,基本均为新药临床试验。值得一提的是,许多国内
企业尤其是创新药企业开始重视国际多中心试验。如:青岛百洋制药有限公司、上海复宏汉霖生物技术股份有限公司、上海海和药物研究开发有限公司、益方生物科技(上海)有限公司、苏州爱美津制药有限公司、药华
医药股份有限公司、百济神州(北京)生物科技有限公司、上海恒瑞医药有限公司、上海岸迈生物科技有限公司、百奥泰生物制药股份有限公司。
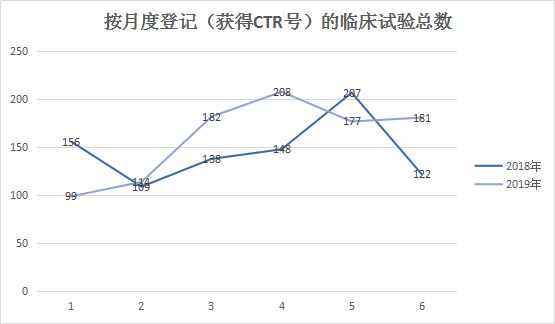
3、按月度登记(获得CTR号)的临床试验总数
临床试验登记数量来看,2019年上半年同比增加较多,其中4月更是达到了208个临床试验,与2018年5月的最高值207持平。
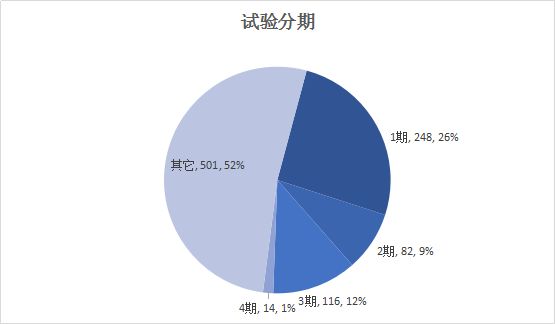
4、试验分类和分期
这里对试验分类和分期就不做太多分析,主要是因为一致性评价的开展,和常规临床试验登记规律有一定不同。
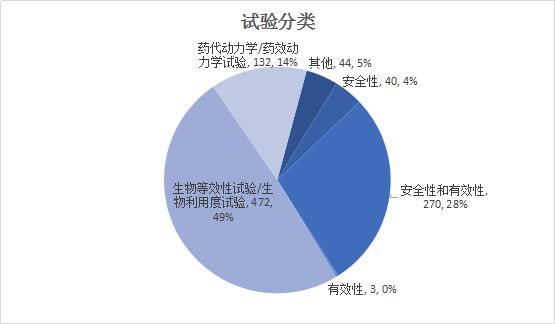
试验分类
试验分期
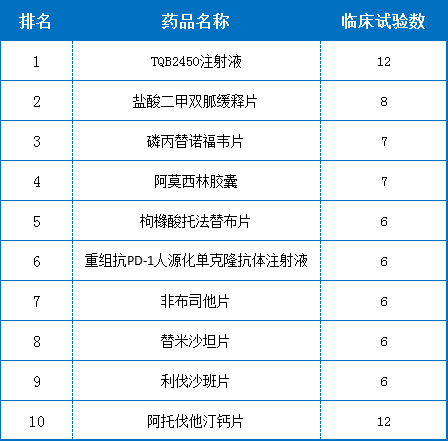
5、2019上半年临床试验最受关注的药品TOP10
对药品的临床试验登记情况统计发现,2019上半年最受关注的药品为TQB2450注射液,其次是盐酸二甲双胍缓释片。TQB2450注射液是正大天晴集团研发的创新型抗PD-L1单克隆抗体药物,由该公司附属公司南京顺欣制药有限公司申请,注册分类为治疗用生物制品。TQB2450注射液拥有结构、配方及工艺等多项自主知识财产权。
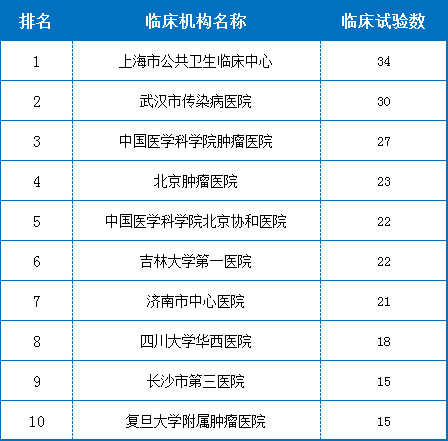
6、最忙碌的临床试验机构
简单看一下2019上半年最忙碌的临床试验机构,开展试验最多的是上海市公共卫生临床中心。与去年不同点在于,去年一致性评价的品种更多,所以很多
医院接的临床试验出现了大幅度上升。
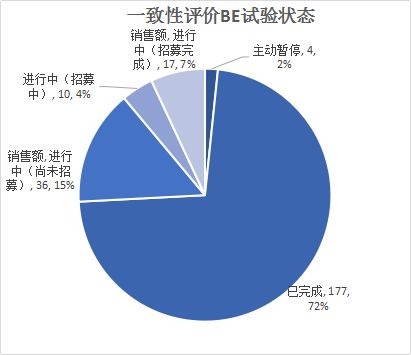
7、一致性评价BE试验
2019年上半年,仿制药一致性评价已登记的BE试验185个,比2018年同期下降24.18%。登记的BE试验主要格局如下:BE试验已经有177个完成了,同时还有15%尚未招募。
BE试验登记数量最多的药品分别是阿莫西林胶囊(9)、盐酸二甲双胍缓释片(5)和替米沙坦片(5)。
综上所述:纵观2019上半年已公示的临床试验,可以发现生物等效性试验所占比重较大,专业的临床试验机构承接的临床试验较多。
数据来源:CDE药物临床试验登记与公示平台、药智数据中国临床试验数据库