日本卫材的仑伐替尼是国内近10年来首个获批一线治疗晚期肝癌的药物,自此打破索拉非尼垄断中晚期肝癌一线治疗的地位。据悉,仑伐替尼国内正式供货不满2个月,其销售额就达到31亿日元(人民币近2亿元)。从治疗效果看,仑伐替尼优于索拉非尼,有望成为晚期肝癌一线标准治疗,目前国内市场已有恒瑞医药、石药集团、正大天晴、湖南科伦制药等8家药企研发或仿制该产品。
供药不足2个月,销售额达到31亿日元
仑伐替尼(也称乐伐替尼)是一种口服多靶点激酶抑制剂(TKI),可抑制VEGFR-1,2,3、FGFR-1,2,3,4、PDGFR、RET、KIT等多个靶点。该产品由日本卫材研发,最早于2012年8月在日本被授予孤儿药治疗甲状腺癌,2015年先后在美国、欧盟正式获批上市,目前已获批的适应症包括晚期甲状腺癌、肾癌、肝细胞癌,此外还有脑胶质瘤、非小细胞肺癌等适应症的临床试验正在进行中。
图1:2014-2017年甲磺酸仑伐替尼胶囊全球销售情况(单位:百万日元)

(来源:米内网跨国上市公司销售库)
据米内网跨国上市公司销售库数据,仑伐替尼上市后销售额一路看涨,2017年达到322亿日元,同比去年增长50.14%。业界对该产品普遍看好,预计其年销售峰值将突破10亿美元。
卫材向CDE提交仑伐替尼(肝癌适应症)的上市申请于2017年11月3日获得承办受理,并于2017年12月18日以“具有明显治疗优势创新药”为由纳入优先审评;2018年9月,该产品获得国家药监局批准进口,用于治疗既往未接受过全身系统治疗的不可切除的肝细胞癌患者,并于2018年11月9日向患者供药,2018年度在中国销售额为31亿日元。
仑伐替尼在中国的售价为16800元/盒,30粒/盒,4mg/粒。体重60kg以下的肝癌患者,使用8mg/天(2粒);60kg及以上的患者,使用12mg/天(3粒)。此外,仑伐替尼的慈善援助政策也已确定,低保患者可以免费获得援助,低收入患者采取(2+2)+(2+x),x是小于或等于10的月数,具体援助药品数量根据个体疾病进展情况而定,这意味着,体重60kg以下的肝癌患者一旦进入援助项目,全年的用药只需购买4个月,折算每月平均花费11200元。
对比全球首个多靶点TKI,仑伐替尼疗效优异
索拉非尼是全球首个获批上市的口服多靶点激酶抑制剂,由拜耳研发,最早于2005年12月获得FDA批准上市,用于治疗晚期肾癌,2007年先后在欧洲、美国获批治疗肝细胞癌,2008年7月获得国家药监局批准进入中国市场,用于治疗不能手术的晚期肝癌患者。索拉非尼是首个有明确证据显示能够改善晚期肝癌患者生存期的系统治疗药物,也是国内肝细胞癌患者的临床一线标准用药。
图2:2014-2017年甲苯磺酸索拉非尼片全球及国内销售情况
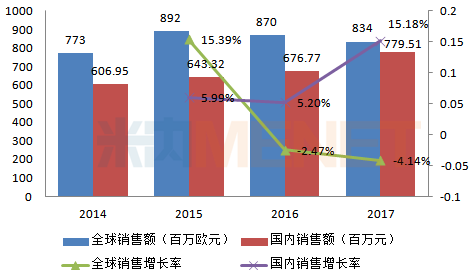
注:国内销售额指中国公立医疗机构终端销售额
(来源:米内网数据库)
据米内网数据,由于受到竞品冲击,2016年开始,索拉非尼全球销售额走“下坡路”,下滑幅度持续加大,2018年实现全球销售收入712百万欧元,同比去年下滑14.63%。反观国内市场,索拉非尼在中国公立医疗机构终端的销售额仍保持稳定增长,被纳入2017版国家医保目录后有望进一步放量,2017年实现销售额7.8亿元,同比去年增长15.18%。
仑伐替尼为索拉非尼主要竞品,在一线治疗不可切除肝细胞癌的III期临床试验(REFLECT研究)中,全球954例晚期肝癌患者,仑伐替尼与索拉非尼头对头对照试验,仑伐替尼客观缓解率达到索拉非尼3倍(40.6%VS12.4%),无进展生存期比索拉非尼高1倍(7.3个月VS3.6个月),中位总生存期比索拉非尼具有优势(13.6个月VS12.3个月)。
全球954例晚期肝癌患者中有288名为大中华地区患者,基于该亚组人群分析结果,仑伐替尼客观缓解率明显优于索拉非尼(43.8%VS13.2%),无进展生存期比索拉非尼高(8.4个月VS3.6个月),中位总生存期比索拉非尼具有较大优势(15个月VS10.2个月)。
从研究结果看,在主要研究终点(总生存期OS)上,仑伐替尼非劣效于索拉非尼,其他次要研究终点(包括无进展生存期PFS、进展时间TTP、客观缓解率ORR等),仑伐替尼均超越索拉非尼。这是继索拉非尼上市10年来,首个在晚期肝癌一线治疗中取得阳性结果的III期临床研究,仑伐替尼有望成为晚期肝癌一线标准治疗。
在说明书中,使用仑伐替尼治疗的患者最常见的5种不良反应是高血压(45%)、疲劳(44%)、腹泻(39%)、食欲下降(34%)和体重下降(31%),这与索拉非尼已知的副作用一致。
8家药企布局,恒瑞最早获批临床,正大天晴首家提交仿制申请
表1:甲磺酸乐伐替尼胶囊国内研发情况
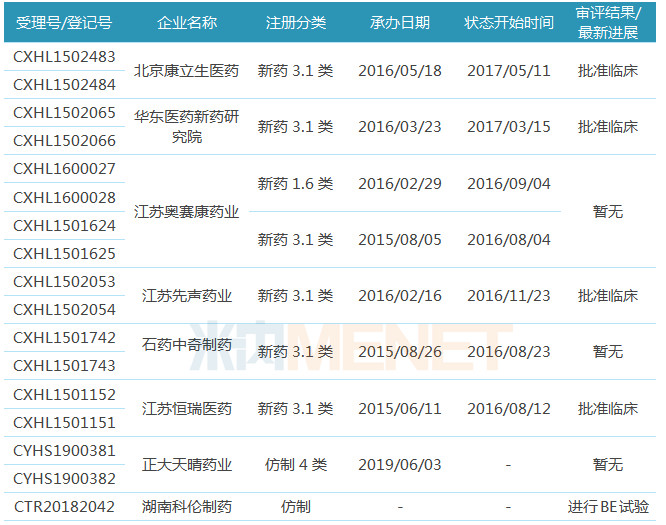
(来源:米内网数据库)
据米内网MED中国药品审评数据库2.0,目前国内有6家药企按新药3.1类或新药1.6类提交甲磺酸乐伐替尼胶囊的临床申请,其中有4家药企的产品已经获批临床,分别为北京康立生医药、华东医药集团新药研究院、江苏先声药业、江苏恒瑞医药,其中恒瑞医药的产品最早获批临床。
据米内网中国药品临床试验公示库数据,目前国内有2家药企针对乐伐替尼/仑伐替尼登记人体生物等效性试验(BE试验)。正大天晴药业的乐伐替尼针对的适应症为局部复发或转移,进展性,放射性碘-难治性分化型(乳头状/滤泡状/Hürthle细胞)甲状腺癌,该产品的BE试验于2018年5月8日在国内入组,2018年6月19日在国内完成BE试验,目前已按仿制4类提交上市申请;湖南科伦制药的仑伐替尼针对的适应症为不能切除的肝细胞癌,于2019年1月11日进行登记,目前还处于“进行中(招募中)”状态。
目前原研厂家卫材的仑伐替尼在国内获批上市的适应症为肝细胞癌,甲状腺癌适应症暂时还未获批上市,正大天晴的产品有望成为首个仑伐替尼仿制药,且是首个获批用于治疗甲状腺癌的仑伐替尼。
来源:米内网数据库、药物简讯
注:数据统计截至6月6日,如有疏漏,欢迎指正!
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..