虽然中国政府迫使全球最大制药公司下调畅销药品价格,但它们对在华业务感到乐观,原因是扩大的国家医保和加快的审批提振了它们在中国这个全球第二大药品市场的销售。
在华销售额最大的两家海外制药公司——阿斯利康(AstraZeneca)和辉瑞(Pfizer)均表示,上季度在华销售额同比增长24%。
与去年分别为15%和16%的增幅相比,这是一次大幅提高。阿斯利康首席执行官帕斯卡尔•索里奥(Pascal Soriot)在电话会议上对投资者表示:“这是突如其来的非常不错的表现。”
中国欧盟商会(EU Chamber of Commerce in China)今年6月表示,所有在华欧洲企业中,制药企业最为乐观,83%的制药企业对增长持乐观态度。
上海美国商会(American Chamber of Commerce in Shanghai)的数据显示,制药行业表示乐观的企业比例较去年增长了40%,是所有行业中态度转变最大的。从事制药、医疗器械、生命科学的企业中87%的企业对商业前景表示“乐观”。
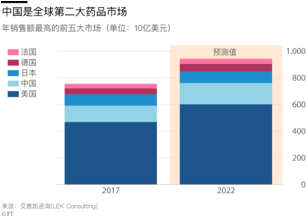
总部位于伦敦的艾意凯咨询(LEK Consulting)的数据显示,中国去年的药品销售额达到1230亿美元。该公司预计,随着中国日益富裕和老龄化的人口变得更容易罹患癌症等慢性病,现在直至2022年中国医药市场将以每年超过5%的速度增长。
过去20年,跨国医药公司在中国的增长主要通过高价出售专利保护到期的品牌药物实现,因为中国本土药企在药品质量上无法与之匹敌。中国是辉瑞仅次于美国和日本的第三大市场。

但由于需要重新进行临床试验等额外要求,跨国药企的创新药很难获得批准,它们往往需要在发达市场上市后再等7年才能在中国销售。
近年来,随着中国政府推动数百种专利保护到期的品牌药物降价——作为将它们纳入国家医保计划的条件——跨国公司在华增长出现放缓。
但是制药商们如今发现,纳入国家医保促进了它们的药品销售。例如,瑞银(UBS)的数据显示,罗氏(Roche)去年将化疗药物阿瓦斯丁(Avastin)在华的价格下调了近70%,但由于被纳入了国家医保,该药实现了约25%的收入增长。
索里奥表示:“我们的许多新药正在进入医保报销,这在加速我们的在华增长。”
另一项对跨国药企有利的因素是新药审批速度的快速提高。去年,中国政府取消了外国药企在母国已获批药物需在华重新进行临床试验才能上市的要求,而且自2014年以来将药品审批人员增加了7倍,以清理积压的申请。
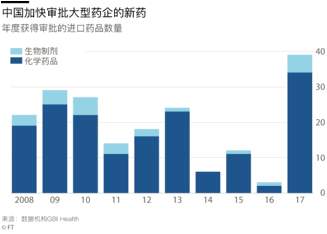

这些举措带来的效果明显。行业数据服务机构GBI Health的数据显示,去年有39种进口药品获得批准,超过之前三年的总和。
今年已有逾15种进口药物获得批准,其中包括百时美施贵宝(BMS)于6月获批的Opdivo、默克(Merck)上月获批的Keytruda以及罗氏本月获批的Alecensa。这些药物都是新一代免疫疗法的一部分,是药企在欧美的巨大营收来源。Keytruda仅用时5个月便获批。
今年在华获批的其他畅销药物还有吉利德(Gilead)于5月获批的肝炎治疗药物Epclusa,以及默克经过三年审核于4月获批的人乳头瘤病毒疫苗“加卫苗9”(Gardasil 9),相比之下,较早上市的类似疫苗经过了10年审批。
罗氏首席执行官丹尼尔•奥戴(Daniel O’Day)表示,最近一个季度在华16%的增长显示出,“中国有能力在比过去快得多的时间内让新型肿瘤类药物上市和纳入医保”。
艾意凯咨询合伙人陈玮(Helen Chen)表示,从加快的药品注册中受益最大的是生产治疗肿瘤、肝炎及罕见病药物的企业。她说:“大型制药公司是最大受益者。”
但北京方面削减医疗支出、打造世界级本土制药工业的努力,给跨国药企的未来蒙上了阴影。中国药企生产仿制药的质量正在提高,有些甚至获得了美国的认证。
花旗(Citibank)的数据显示,这使得中国本土药企的增长速度超过了海外药企,导致10家在华最大外国药企的市场份额过去几年略有下降,至略低于20%。在部分药物上,这种下滑将变得更加明显。
例如,据花旗称,赛诺菲(Sanofi)的抗凝血药物Plavix 2016年在该类药物市场占据83%的份额,但随着中国公司深圳信立泰(Salubris)的份额增长,Plavix的市场份额到2020年将会降至60%。
据花旗预测,由于中国生产的仿制药的竞争,辉瑞公司的降胆固醇药物Lipitor的市场份额预计将在同期从74%降至46%。
据花旗称,跨国公司正在向本地竞争对手出售销售额下降的药品的制造权,过去几年大约有20宗此类交易。
但分析师表示,跨国公司的专利过期药物仍有可能实现增长,因为整体市场正在增长,而且中国患者在国内药物质量丑闻后增强了对外国品牌的信任——例如最近一个月有报道称,两家中国公司销售了100万支问题疫苗。
曾担任中国国家食品药品监督管理总局局长、后任国家市场监督管理总局副局长的毕井泉策划了中国的药品审批改革,他因疫苗丑闻而辞职,这可能会减缓制药行业的增长,因为监管机构采取了更为谨慎的态度。
陈玮表示:“我们看到中国政府的态度有了一些改变,他们变得更加关注自身责任,而不是以执法和检查为导向。总的来说,这是一个可能会放缓或被逆转的好的政策趋势。”
北京方面本月表示,正在与外国公司就18种抗癌药物的价格进行谈判,其中包括诺华(Novartis)的Jakavi和辉瑞的Inlyta,这是将它们纳入国家医保的前奏。
瑞银分析师赵冰表示,这个消息显示,当前的监管体系不会受到毕井泉辞职的影响。
更长期的风险是,北京方面要求,国内仿制药必须证明其质量与外国竞争对手相当。
监管机构最初表示,要求国内制药商在今年年底前证明其等效性,否则会被迫退出市场。到目前为止,已有68种中国药物通过了测试。
由于市场上有数千种药物,行业高管们表示这个过程将持续数年时间。 但赵冰表示,一旦完成,“医院将会完全转向本地药物。对于跨国公司来说,这将是一个大问题。”
因此,跨国公司需要加快向中国销售更多专利药品的转变——这一过程因审批速度加快而变得更容易。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..