近日,歌礼在官网宣布,公司自主研发的国内首个本土原研丙肝1类新药达诺瑞韦钠片(又称丹诺瑞韦钠片,商品名戈诺卫)获国家药品监督管理局批准上市。2017年至今,国内共有5个药企的6款丙肝药物获批上市,除了歌礼,其余均为跨国企业。此外,在已纳入优先审评药品名单中,除了已获批上市的,还有18个受理号(涉及11个品种)为丙肝药物,其中3个为进口品种。
黑马歌礼“出线”
国内首个本土丙肝新药上市
6月13日,歌礼宣布其自主研发的丙肝1类新药达诺瑞韦钠片(又称丹诺瑞韦钠片,商品名戈诺卫)已获国家药监局批准上市,据米内网MED药品审评数据库2.0数据,歌礼的达诺瑞韦钠片已处于审批完毕-待制证状态。
图1:丹诺瑞韦钠片审评审批情况

(来源:米内网MED药品审评数据库2.0)
戈诺卫是歌礼首个获批上市的产品,也是国内首个本土企业自主研发的丙肝DAA(直接抗病毒)药物。2017年1月3日,戈诺卫上市申请受到CDE受理,受理号为CXHS1600012,2017年10月30日,该受理号进入三合一审评序列,2018年6月11日,国家药监局审批完毕,批准生产,从申请上市到获批上市一共经历了524天的时间。
图2:丹诺瑞韦钠片审评时间轴

(来源:米内网MED药品审评数据库2.0)
今年5月,歌礼正式向港交所提交IPO申请书,在港股IPO新规中,允许尚未盈利的生物科技公司赴港上市的条件之一就是拟上市生物科技公司于建议上市日期前至少6个月得到相当数额的第三方投资,并至少有1只核心产品已通过概念开发流程。对于歌礼来说,戈诺卫的上市无疑是公司冲刺IPO的有力支撑。
十一届全国人大常委会副委员长、中国工程院院士、国家重大新药创制科技专项技术总师桑国卫说:“非常高兴中国首个本土原研丙肝创新药戈诺卫获批上市。这是国家重大新药创制科技专项的一项重大成果,表明了中国医药企业创新能力正在不断加强,并在重大疾病防治领域取得突破。”
戈诺卫的上市打破了国内丙肝药物市场被跨国药企垄断的局面,在歌礼之前,国内已有吉利德、艾伯维、百时美施贵宝、默沙东等跨国企业的抗丙肝药物获批上市,虽然戈诺卫的上市时间迟了一些,但日后若能成功进入医保目录,凭借着价格优势,或许能替代原研产品抢占大部分市场。
跨国企业纷纷转战中国
5药企鏖战,谁将称霸?
丙肝是一种由丙型肝炎病毒(HCV)感染引起的病毒性肝炎,据世界卫生组织发布的《2017年全球肝炎报告》数据,目前全球大约有3.25亿人感染慢性乙肝病毒或丙肝病毒。随着乙肝疫苗的普及与应用,乙肝的患病率有所下降,相比于乙肝的防控策略,丙肝尚无疫苗可预防,其发病率呈现急剧上升趋势。中国是“丙肝大国”,基因1型、2型、3型及6型病例占所有丙型肝炎病毒病例的96%,这推动丙肝药物市场不断扩容。
表1:2017年至今国内获批上市的丙肝DAA药物
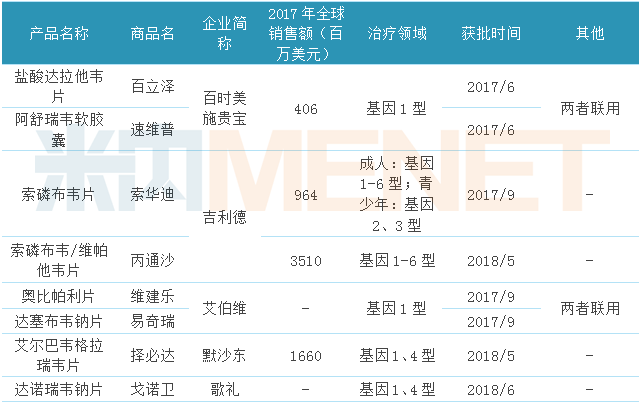
(来源:米内网数据库)
自2017年以来,国内陆续有丙肝DAA药物获批上市,分别归属于百时美施贵宝、吉利德、艾伯维、默沙东、歌礼,其中百时美施贵宝、艾伯维的两款药物均为联合用药,歌礼丙肝新药的上市打破了国内丙肝药物市场被跨国药企垄断的局面。
吉利德:索磷布韦片、索磷布韦/维帕他韦片
索磷布韦片(商品名索华迪),属于抗丙肝病毒的核苷类聚合酶抑制剂,2013年12月在美国上市,适用于部分丙肝基因分型,治愈率达90%以上,索华迪2017年的全球销售额为964百万美元,相比前几年销量大幅下滑。
图3:2014-2017年索磷布韦片全球销售情况(单位:百万美元)
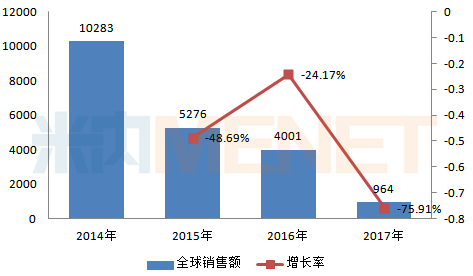
(来源:米内网跨国上市公司销售库)
2017年9月,索华迪在国内获批上市,同年11月,吉利德公布索华迪在国内的最终定价为19660元/瓶,销售规格为28片/瓶,按照每三个月为一个疗程来计算,则一个疗程的价格为58980元,目前还是自费项目。
索磷布韦/维帕他韦片(商品名丙通沙),是中国首个获批的泛基因型、每日一次、针对慢性丙型肝炎病毒的单一片剂,适用于基因1-6型HCV成人患者。据五项国际多中心3期临床研究数据,在很难治愈的患者群体(包括经治患者,以及代偿期或失代偿期肝硬化患者)中,SVR12(定义为完成治疗后的第12周,检测不出HCVRNA)的总体实现率为92%-100%。
图4:2016-2017年索磷布韦/维帕他韦片全球销售情况(单位:百万美元)
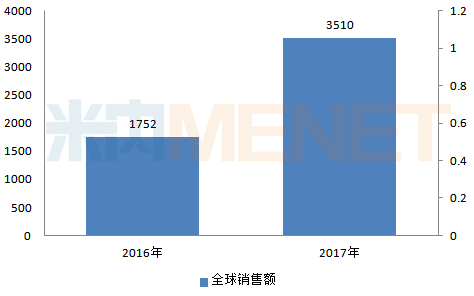
(来源:米内网跨国上市公司销售库)
丙通沙于2016年在美国及欧盟获批上市,至今已获得54个国家上市批准,其2017年的全球销售额为3510百万美元,同比去年增长100.34%。
百时美施贵宝:盐酸达拉他韦片+阿舒瑞韦软胶囊
盐酸达拉他韦片(商品名百立泽),属于抗丙肝病毒的NS5A抑制剂,阿舒瑞韦软胶囊(商品名速维普)是施贵宝公司研发的第二代蛋白酶抑制剂,达拉他韦片与阿舒瑞韦胶囊的全口服联合疗法已于2014年在日本获批,成为日本第一个应用于临床的全口服、不含干扰素的治疗丙肝基因1型患者、包括失代偿肝硬化丙肝患者的临床方案。2017年在全球销售额为406百万美元,同比去年有大幅下降。
图5:2014-2017年盐酸达拉他韦片+阿舒瑞韦软胶囊全球销售情况(单位:百万美元)
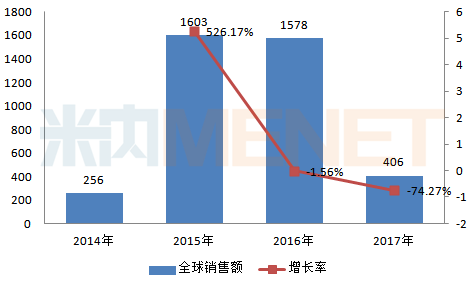
(来源:米内网跨国上市公司销售库)
百时美施贵宝的“阿舒瑞韦”+“达拉他韦”组合于2017年6月在国内获得批准上市后,马上就与上海医药和保险机构合作开展了“按疗效付费”创新保险项目等市场推广工作。根据纳入中国大陆患者的临床研究结果,该联合治疗方案针对基因1b型慢性丙肝患者的治愈率达91%~99%,安全性与耐受性良好。
艾伯维:奥比帕利片+达塞布韦片
奥比帕利片(商品名维建乐)是由奥比他韦、帕利瑞韦、利托那韦3种药物组成的抗丙肝病毒复方制剂,达塞布韦片(商品名易奇瑞)属于非核苷类聚合酶抑制剂。维建乐联合易奇瑞的方案目前已在全球70多个国家和地区获批,用于临床治疗基因1型慢性丙肝患者。
维建乐联合易奇瑞的治疗方案包含了3种直接抗病毒药物,即NS5A抑制剂、NS3/4A蛋白酶抑制剂和NS5B聚合酶非核苷类似物抑制剂,可针对丙肝病毒生命周期的3个主要靶点,抑制丙肝病毒的复制。2017年9月,该治疗方案在国内获批上市,并于2018年3月经国家药品监督管理局批准,疗程由原先的12周缩短至8周。
默沙东:艾尔巴韦格拉瑞韦片
艾尔巴韦格拉瑞韦片(商品名择必达),由艾尔巴韦和格拉瑞韦组成的固定剂量复方片剂,采用每天一片、12周疗程治疗基因1、4型初治或经治复发慢性丙肝患者。2017年在全球销售额为1660百万美元,同比去年增长199.1%。
图6:2016-2017年艾尔巴韦格拉瑞韦片全球销售情况(单位:百万美元)
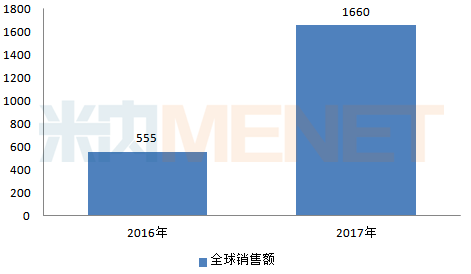
(来源:米内网跨国上市公司销售库)
歌礼:达诺瑞韦钠片
达诺瑞韦钠片(商品名戈诺卫)是歌礼开发的具有自主知识产权的新一代NS3/4A蛋白酶抑制剂,在中国大陆地区完成的III期临床试验结果显示,经过12周治疗,在基因1型非肝硬化患者中治愈率(SVR12)达97%;在基因4型非肝硬化患者中的治愈率达100%。
歌礼创始人吴劲梓曾表示:“如果戈诺卫的新药证书今天批下来,我保证21天后让中国的丙肝患者吃上能够治愈丙肝的药物。”歌礼真的能用21天让中国丙肝患者吃上达诺瑞韦钠片吗?让我们一起拭目以待。
除了已经获批的戈诺卫,歌礼开发的另一款抗丙肝1类新药拉维达韦(新一代全基因型NS5A抑制剂)也已完成II/III期临床研究,临床研究表明,拉维达韦联合戈诺卫®组成的首个中国原研全口服无干扰素方案,在基因1型非肝硬化患者中治愈率(SVR12)达99%,且针对基线发生NS5A耐药突变的患者,100%实现SVR12。
竞争白热化
11个丙肝药物将加速上市
表2:已纳入优先审评的丙肝药物

(来源:米内网MED药品审评数据库2.0,截止至6月20日,如有疏漏,欢迎指正)
据米内网MED药品审评数据库2.0数据,在已纳入优先审评产品中,去除已经获批上市的,目前处于申请临床/申请上市的丙肝药物有11个,包括进口药品3个,涉及吉利德、艾伯维等跨国药企,其中吉利德的来迪派韦索磷布韦片及艾伯维的格卡瑞韦哌仑他韦片目前已处于申请上市状态。这些丙肝药物获得优先审评的资格,将有助于加快研发进程及上市速度。
此外,据米内网全球药物研发库数据,国内企业太景生物科技、银杏树药业、常州寅盛药业、北京瑞云海生物等多家企业均有丙肝药物处于不同研发阶段,未来国内丙肝市场竞争日趋激烈。
来源:米内网数据库、公司官网等
关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..