2016年度药品检查报告
CFDA · 2017年5月
◆ ◆ ◆ ◆

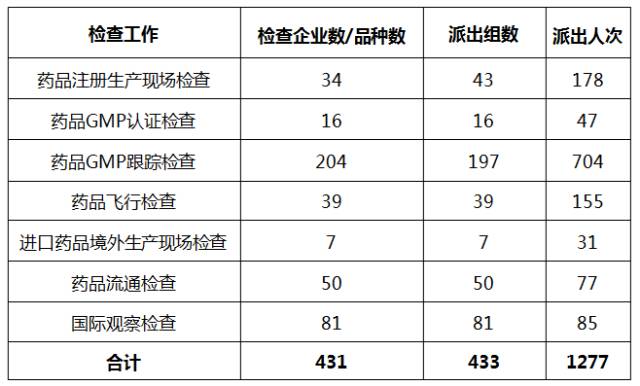
2016年完成各类药品检查任务一览表

“
药品注册生产现场检查
”
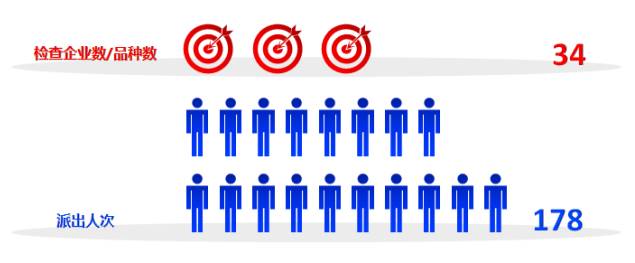
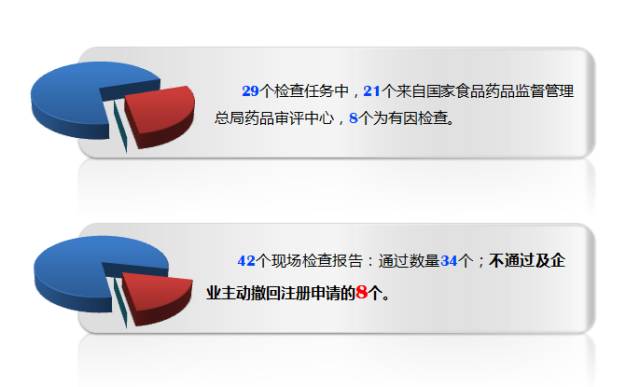
发现主要问题
1. 数据可靠性问题
2. 工艺验证不充分,生产工艺不稳定
3. 生产工艺或关键工艺参数、内包材与核定内容不一致,未进行研究评估
4. 未进行必要的偏差调查
“
药品GMP认证检查
”

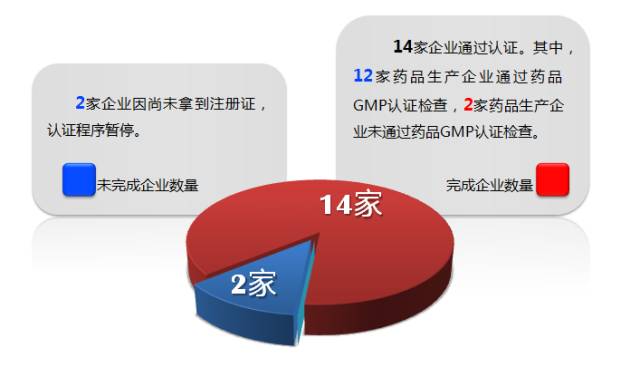

5 家企业收到告诫信

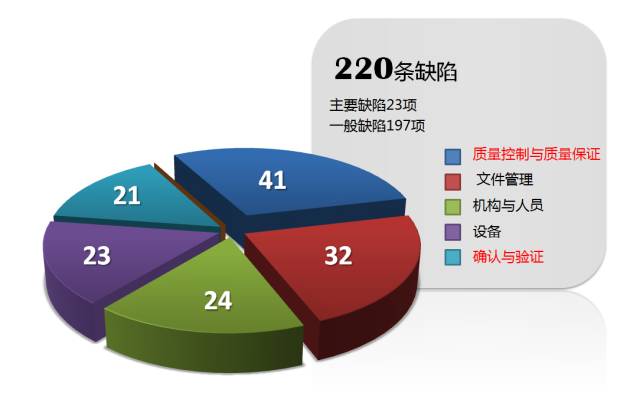
发现主要问题
不通过认证企业两家,均为体外诊断试剂生产企业:
质量管理体系方面。
确认与验证工作方面。
“
药品GMP跟踪检查
”
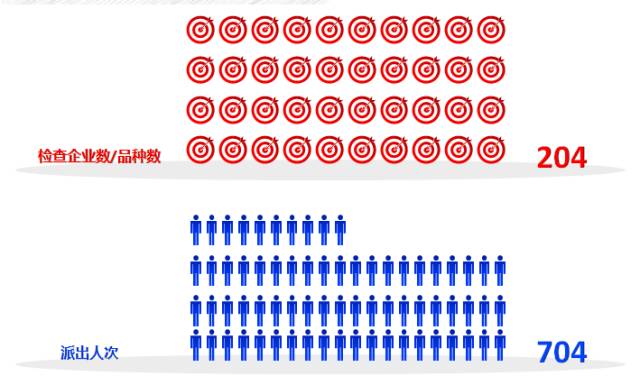
详细数据
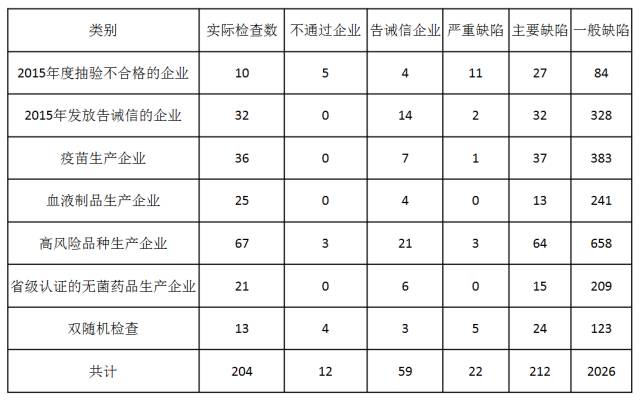
204家次检查共发现2260条缺陷项,其中严重缺陷22项,主要缺陷212项,一般缺陷2026项。与2015年GMP认证、跟踪检查相比严重缺陷数目有所增加。
发现主要问题
在高风险品种专项检查的企业中品种长期停产或未通过药品GMP(2010年修订)认证的现象比较突出,检查发现的一些共性问题如下:
个别存在生产工艺与注册工艺不一致问题。
数据可靠性问题仍然存在,包括伪造生产记录,检验记录中套用图谱、擅自修改数据问题,生产、设备、物料记录中相关内容不符等问题。
工艺验证不充分,特别是变更生产批量后未进行工艺验证的问题较多。
数据管理的规范性问题突出,主要体现在系统权限设置、审计追踪功能、文件和数据的修改及删除权限等未进行控制,以及对删除数据和选择使用的数据没有合理控制和解释。
计算机化系统、确认和验证两个附录的实施情况与法规要求存在一定差距,发现问题较多。
对偏差和变更的管理较薄弱,主要体现在对发生的偏差不能有效识别并记录,对变更缺少必要的评估和验证。
“
药品飞行检查
”
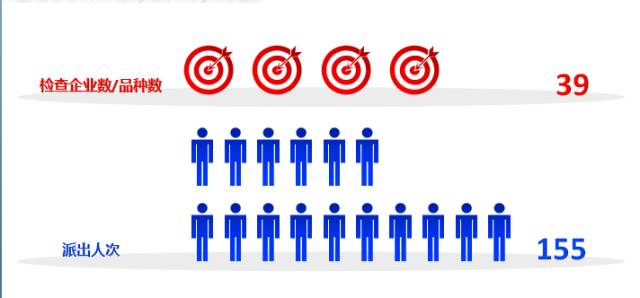
涉及北京、江苏、广东等20个省(市)
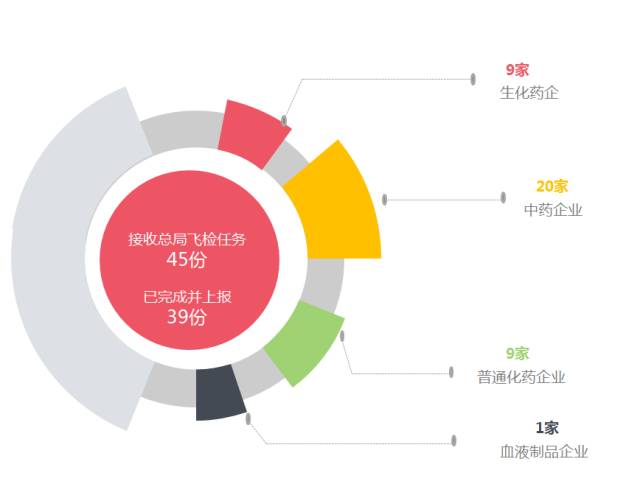
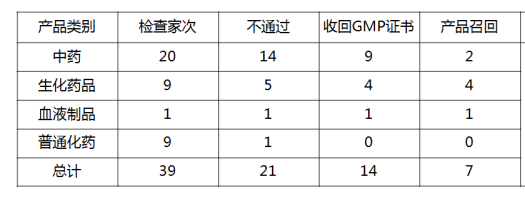
发现主要问题之中成药
1.中成药生产企业
(1)擅自改变工艺问题较为突出。
(2)中药材、中药饮片物料管理混乱。
(3)对购入的中药材、中药饮片不能严格全检,且数据可靠性存在问题。
2.人工牛黄
部分企业不能按照药品GMP要求组织生产,尤其是对人工牛黄上游产业链供应商审计和管理要求严重不足,供应商的加工场所卫生环境恶劣,原材料来源无法溯源,加工过程不可控。
3.中药饮片
购进中药材或炮制后产品的含量检测问题突出,染色、增重问题时有发生,批生产记录真实性存疑。
发现主要问题之生化药品企业
“单唾液酸四己糖神经节苷脂钠”的检查
2016年共检查4家生产企业,发现其在原料质量和供应商管理方面存在一定的风险。主要问题包括:
(1)供应商管理有待提高,企业对供应商的管理不能保证有效的追溯性。
(2)对原料冷链运输监控的电子数据管理不够。
“注射用促肝细胞生长素”的检查
2016年共检查4家生产企业,其中2家企业被收回《药品GMP证书》,对另外2家企业发出了告诫信。主要问题包括:
(1)编造记录文件;
(2)数据可靠性问题;
(3)与注册生产工艺不一致;
(4)无法有效保证肝脏原料的质量。
10家企业被建议立案调查
“
进口药品境外检查
”
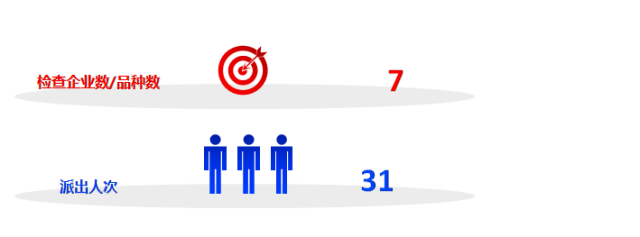
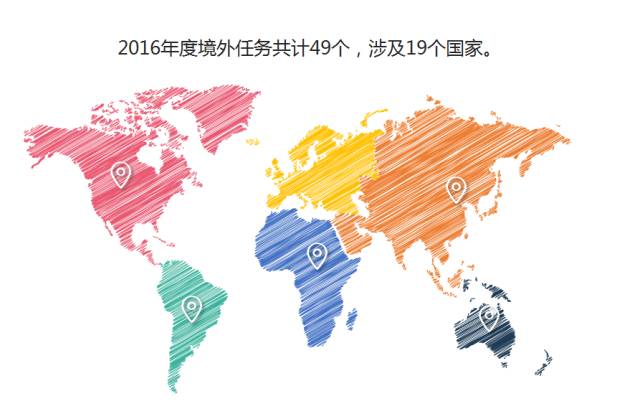

发现主要问题:
已检查的7个品种中,3个品种不通过,不通过率较往年有所提高。检查共发现缺陷117项,其中严重缺陷3项,主要缺陷18项。
问题主要集中在质量控制与质量保证、物料系统、变更管理等方面;严重缺陷主要为生产工艺一致性以及数据可靠性问题。
主要及严重问题如下:
1.实际生产工艺、生产场地等与注册申报不一致,重大变更等情况未向我国进行申报却已执行。
2.数据可靠性存在重大问题,严重影响产品质量。
3.非现场检查处理品种数量增多。
“
药品流通检查
”
检查数据

检查结果
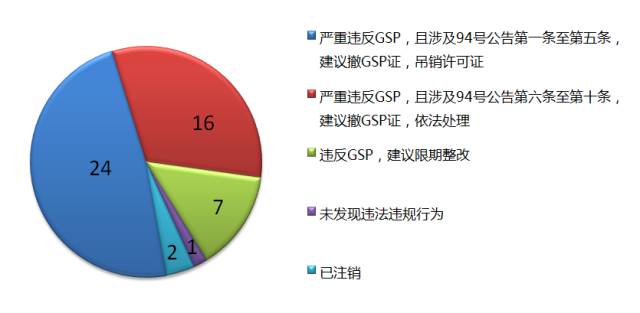

主要问题

存在主要问题:
1.未按规定对药品储存、运输、进行温湿度监测。
2.购销药品时,证(许可证书)、票(发票、随货同行票据)、账(实物账、财务账)、货(药品实物)、款(货款)不能相互对应一致;药品未入库,设立账外账,药品未纳入企业质量体系管理,使用银行个人账户进行业务往来等情形。
3.伪造药品采购来源,虚构药品销售流向,篡改计算机系统、温湿度监测系统数据,隐瞒真实药品购销存记录、票据、凭证、数据等,药品购销存记录不完整、不真实,经营行为无法追溯。
药品流通企业GSP缺陷主要集中于总则、储存与养护、销售等方面。主要存在问题:
1.未依法经营,存在虚假、欺骗行为。
企业擅自变更经营注册地址;在经营许可范围外设仓库储存药品;为他人违法经营药品提供条件;虚构药品采购来源及销售流向;藏匿票据、提供虚假资料;自查报告不真实;纳税申报表造假;篡改温湿度监测数据等。
2.未按规定储存药品,未对库房温湿度进行有效监测、调控。
3.购销药品时,票、帐、货、款不一致,特药销售未执行国家规定。
“
国外机构GMP观察检查
”
主
要
数
据
观察检查81家次,涉及企业76家,涵盖浙江、山东等20个省(市),其中浙江、山东、江苏、广东、湖北、海南、河北占80%。
本年度观察检查共涉及172个药品,包括119个原料药、23个口服固体制剂、19个注射剂、5个生物制品,及6个其他产品。
在81家次检查中涉及原料药的检查共62次,约占全部检查次数的69%,涉及口服固体制剂的检查12次,约占全部检查次数13%。其中原料药占比最大,其次是口服固体制剂,其他剂型出口相对较少。与2015年相比,其他剂型(包括无菌制剂、生物制品等)接受检查的比例有了一定的提升,占比由2015年的10%上升至18%,
2016年检查观察涉及的检查机构包括世界卫生组织(WHO)、欧洲药品质量理事会(EDQM)、美国食品药品监督管理局(US FDA)、德国汉堡健康及消费者保护部(BGV)、巴西卫生监督局(ANVISA)、法国国家医药健康安全管理局(ANSM)等12个国际组织或国外药品监管部门。
主要
问题
1
9家药企未通过国外监管/检查机构的现场检查:世界卫生组织(WHO)4家
欧洲药品质量理事会(EDQM)4家
美国食品药品监督管理局(US FDA)1家
2
与2015年相比,不通过比率有所上升(增长约3%)。
3
在9家未通过检查的企业中,多数严重缺陷项均涉及数据可靠性问题(包括重复测试至合格、修改系统时间后检测、删除数据、删除审计追踪记录、选择性使用数据、修改电子数据名称、试进样、记录不及时、记录不真实、数据和记录缺失、文件记录控制不足等),部分企业涉及到物料标准制定不合理、避免交叉污染的措施不足等方面。
4
2016年观察检查工作中共记录发现的缺陷项1108项,依据我国2010版GMP正文章节对缺陷项进行分类分析发现:质量控制与质量保证、文件管理、设备、物料与产品、确认与验证、厂房与设施六个类别的缺陷占了全部缺陷的88%。
5
与2015年相比,文件管理部分缺陷由第4位上升至第2位,在目前企业逐渐加强数据可靠性管理的环境下仍增长了约7%(由10.5%增加至17.3%),充分体现出当前国外检查对数据可靠性的关注程度与严格要求。
6
“质量控制与质量保证”部分提出的缺陷占总缺陷数的27.3%,位居首位;“文件管理”部分出现的缺陷居于第二位;“设备”部分出现的缺陷居于第三位。
图解/中国健康传媒集团
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..