小核酸抗体偶联药物(Antibody-oligonucleotide conjugates,AOC)利用抗体将治疗性寡核苷酸递送至特定细胞或组织,将抗体的组织特异性优势,与小核酸的靶点特异性优势相结合,可一定程度上用于解决目前小核酸药物仅能通过脂质纳米颗粒(LNP)、N-乙酰半乳糖胺(GalNAc)递送系统靶向肝脏的问题。
本篇文章主要从全球AOC市场布局出发,分析AOC在研公司现状及未来发展趋势和关注点,希望对关注核酸药物和偶联药物领域的各位研究者有所帮助。
全球AOC药物市场布局
小核酸药物在当前医药行业中非常火热,但在递送技术的创新层面依然存在困境,已上市的小核酸药物仅能针对肝脏靶点。目前,小核酸的非肝靶向递送在国外已引起诸多公司的关注,Avidity Biosciences的AOC于2021年11月首次进入临床研究,至今已在超过30例病人身上完成给药。Dyne Therapeutics的AOC药物也于2022年9月启动临床病人入组。AOC结合了小核酸的靶点特异性和抗体等大分子药物的组织特异性两大优点。
目前全球在研AOC的公司主要有:Avidity Biosciences、Dyne Therapeutics、Tallac Therapeutics、Denali Therapeutics等
❖ Avidity Biosciences
公司总部位于美国加州,通过抗体寡核苷酸偶联物(AOCs TM )平台,将单克隆抗体的特异性与寡核苷酸疗法的精度结合起来,能够递送给以前无法达到的组织和细胞类型,以靶向以前RNA疗法无法治疗的疾病,并更有效地针对疾病的潜在遗传驱动因素。Avidity公司的AOC平台能够偶联各种类型的寡核苷酸,包括siRNA和磷酰二胺吗啉代寡核苷酸(phosphorodiamidate morpholino oligomer, PMO),这种灵活性能够使得该公司根据不同的疾病类型设计不同的AOC药物。与传统寡核苷酸疗法相比,AOC具有更好的药代动力学特性和更具特异性的生物分布,而且可以避免使用脂质体递送寡核苷酸带来的毒副作用。
AOC 1001通过Avidity Biosciences 的AOC平台所生产,由一款靶向1型转铁蛋白受体(TfR1)的单克隆抗体和一种靶向DMPK mRNA的siRNA偶联而成,旨在降低强直性肌营养不良症1型(Myotonic dystrophy type 1, DM1)患者成纤维细胞中异常DMPK mRNA水平,从根本上解决DM1。临床前研究数据显示,AOC 1001能够成功将siRNA递送到肌肉细胞中,导致DMPK mRNA在多种肌肉(包括骨骼肌、心肌和平滑肌)产生持久的剂量依赖性降低。
AOC1020是一种靶向DUX4的siRNA抗体偶联物。DUX4(Double Homeobox 4)属于双同源盒转录因子。同源盒基因在进化上是高度保守的,对于发育的调控至关重要。AOC1020通过降低DUX4的表达来达到治疗面肩肱型肌营养不良症(Facioscapulohumeral muscular dystrophy, FSHD)的目的。目前已经处于1/2期临床试验阶段,该药是基于公司的RNA平台技术设计的首款AOC药物,适应症为杜氏肌肉营养不良症(Duchenne Muscular Dystrophy, DMD)。DMD是一种肌营养不良蛋白缺乏引起的X染色体隐性遗传神经肌肉病。目前DMD尚无有效治愈手段,基因替代、外显子跳跃、基因组编辑、终止密码子通读等基因治疗逐步成为研究热点。

Avidity Biosciences 管线(来自官网)
❖ Dyne Therapeutics
总部位于美国马萨诸塞州,是一家针对严重肌肉疾病开发靶向治疗的生物制药公司。公司主要聚焦三大罕见肌肉疾病,包括DM1、DMD和FSHD。凭借其专有的 FORCE™ 平台,Dyne 正在开发新型寡核苷酸疗法。FORCE™ 平台以 TFR-1 受体为靶点(TFR-1 受体在肌肉细胞表面高度表达),通过将抗体与治疗严重肌肉疾病的寡核苷酸连接来设计治疗分子。
DYNE-251是针对携带51号外显子跳跃突变的DMD患者开发的抗体偶联寡核苷酸药物,其由PMO与Fab片段结合组成。DYNE-251可以靶向结合目标肌肉组织中高度表达的转铁蛋白受体1(TfR1),通过促进外显子的跳跃,使肌肉细胞产生短且具有功能的肌肉营养不良蛋白,从而阻止或逆转疾病的进程。
DYNE-101用于治疗DMD的I/II期临床试验正在进行中。DYNE-101由与反义寡核苷酸(ASO)结合的抗原结合片段抗体(Fab)组成,以实现肌肉组织的靶向递送,目的是减少细胞核中有毒的DMPK RNA,释放剪接蛋白,允许正常mRNA处理和正常蛋白的翻译,并有可能阻止或逆转疾病。
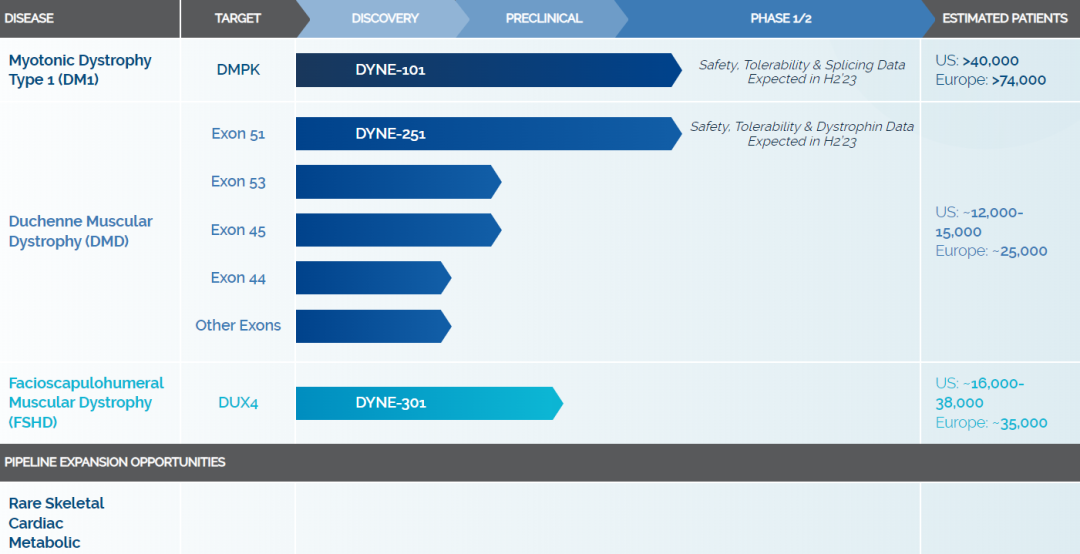
Dyne Therapeutics管线(来自官网)
❖ Tallac Therapeutics
总部位于美国加州,致力于开发一种使用抗体-免疫激活剂偶联物进行靶向免疫激活的技术,利用先天性和适应性免疫力开发抗癌疗法, 产品线基于其新颖的Toll样受体(TLR)激动剂抗体偶联药物(TRAAC)平台。
TAC-001是一种全身递送的药物,是一种由强效的T-CpG与CD22抗体结合的AOC,通过与CD22结合将T-CpG递送给B细胞,进而导致TAC-001的内化以及TLR9信号、B细胞激活,产生一系列免疫反应。TAC-001引发的先天性和适应性免疫反应在检查点抑制剂耐药和难治性肿瘤模型中显示出强大、治愈和持久的单药抗肿瘤活性。
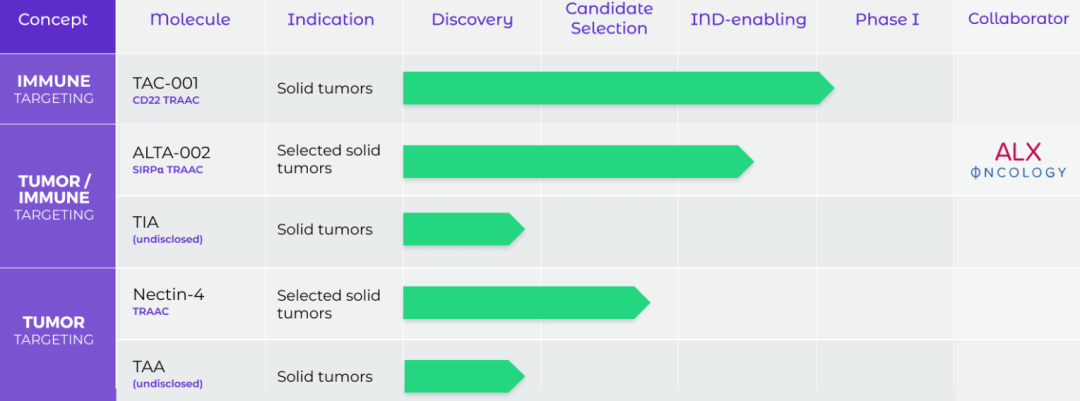
Tallac Therapeutics管线(来自官网)
AOC的未来关注点
小核酸药物与小分子化药和抗体药相比较具有显著优势,将成为今后主流药物。小核酸药物可覆盖更多靶点和可应用更多的临床适应症,具有更大的市场空间。稳定性修饰以及高效递送系统的开发很好的解决了siRNA靶向递送问题,治疗领域从以往的罕见病到一些常见病,应用范围逐渐扩大。
但小核酸药物整体研发仍处于早期阶段,尤其是技术平台和专利平台需加快建设。小核酸药物技术难点仍有待多层突破,尤其是靶向递送和有效作用需加快研发。仍需要开展大量研究来确定抗体与小核酸的最佳结合方式,并筛选受体靶点,以识别对所需组织和细胞类型具有特异性的受体,从而提供最佳疗效,同时避免细胞毒性作用。在高效的肝靶向以外,小核酸药物迈向更广泛的组织类型中仍有待于递送工具的拓展。
AOC作为一种简便、特异性高、不良反应小的组合式创新递送手段,提供了更多的可能性;我们期待AOC作为一种新型偶联药物在多种疾病的治疗领域取得更多的突破。
参考文献
[1] Kalina Paunovska, et al. Drug delivery systems for RNA therapeutics. Nat Rev Genet. 2022 May;23(5):265-280. doi: 10.1038/s41576-021-00439-4.
[2]. Julien Dugal-Tessier, et al. Antibody-Oligonucleotide Conjugates: A Twist to Antibody-Drug Conjugates. J Clin Med. 2021 Feb 18;10(4):838. doi: 10.3390/jcm10040838.
[3]. Victor Lehot, et al. Non-specific interactions of antibody-oligonucleotide conjugates with living cells. Sci Rep. 2021 Mar 15;11(1):5881. doi: 10.1038/s41598-021-85352-w.
[4]. K Sreedurgalakshmi, et al. Cetuximab-siRNA Conjugate Linked Through Cationized Gelatin Knocks Down KRAS G12C Mutation in NSCLC Sensitizing the Cells Toward Gefitinib. Technol Cancer Res Treat. 2021 Jan-Dec;20:15330338211041453. doi: 10.1177/15330338211041453.
[5]. Nicole Bäumer, et al. Antibody-coupled siRNA as an efficient method for in vivo mRNA knockdown. Nat Protoc. 2016 Jan;11(1):22-36. doi: 10.1038/nprot.2015.137.
[6]. Hua Lu, et al. Site-specific antibody-polymer conjugates for siRNA delivery. J Am Chem Soc. 2013 Sep 18;135(37):13885-91. doi: 10.1021/ja4059525.
[7]. Patrick J Kennedy, et al. Antibodies and associates: Partners in targeted drug delivery. Pharmacol Ther. 2017 Sep;177:129-145. doi: 10.1016/j.pharmthera.2017.03.004.
[8]. Guizhi Zhu, et al. Aptamer-Drug Conjugates. Bioconjug Chem. 2015 Nov 18;26(11):2186-97. doi: 10.1021/acs.bioconjchem.5b00291.
[9]. Tsukasa Sugo, et al. Development of antibody-siRNA conjugate targeted to cardiac and skeletal muscles. J Control Release. 2016 Sep 10;237:1-13. doi: 10.1016/j.jconrel.2016.06.036.
[10]. Asher Mullard. Antibody-oligonucleotide conjugates enter the clinic. Nat Rev Drug Discov. 2022 Jan;21(1):6-8. doi: 10.1038/d41573-021-00213-5.
四川省医药保化品质量管理协会关于2026
各会员单位: 当前,制药行业正..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..