诺诚健华和渤健“联姻”失败,对国内药企来说显然是意料之外。
2月15日,诺诚健华公告称,渤健已通知公司,双方决定终止此前关于其核心产品奥布替尼的合作和许可协议。此前诺诚健华回应称,渤健已向诺诚健华一次性支付不可退还和不予抵扣的首付款1.25亿美元,协议终止不会影响首付款及其他相关已确认收入。
截至2月16日收盘,诺诚健华科创板跌18.37%,成交额6.03亿元。H股盘中一度跌超30%,收跌27.34%。
关于合作终止背后的原因,这两天已经有太多分析文章,在此不再赘述,我们更想讨论的是,在国内药企频次越来越高的license out交易背景下,这起半途终止的合作,对于其他正在准备产品“出海”的药企有什么启示和提醒?
2023年刚过去的一个多月,包括恒瑞、石药、在内的10家药企对外进行了license out交易,总额超50亿美元。这是已经公布完成交易的,还在准备“冲刺”海外市场的BD数量只会更多。
渤健和诺诚健华的消息犹如前方路口的红灯亮起,让正一心火热的药企们停下来想一想,接下来该往哪走?
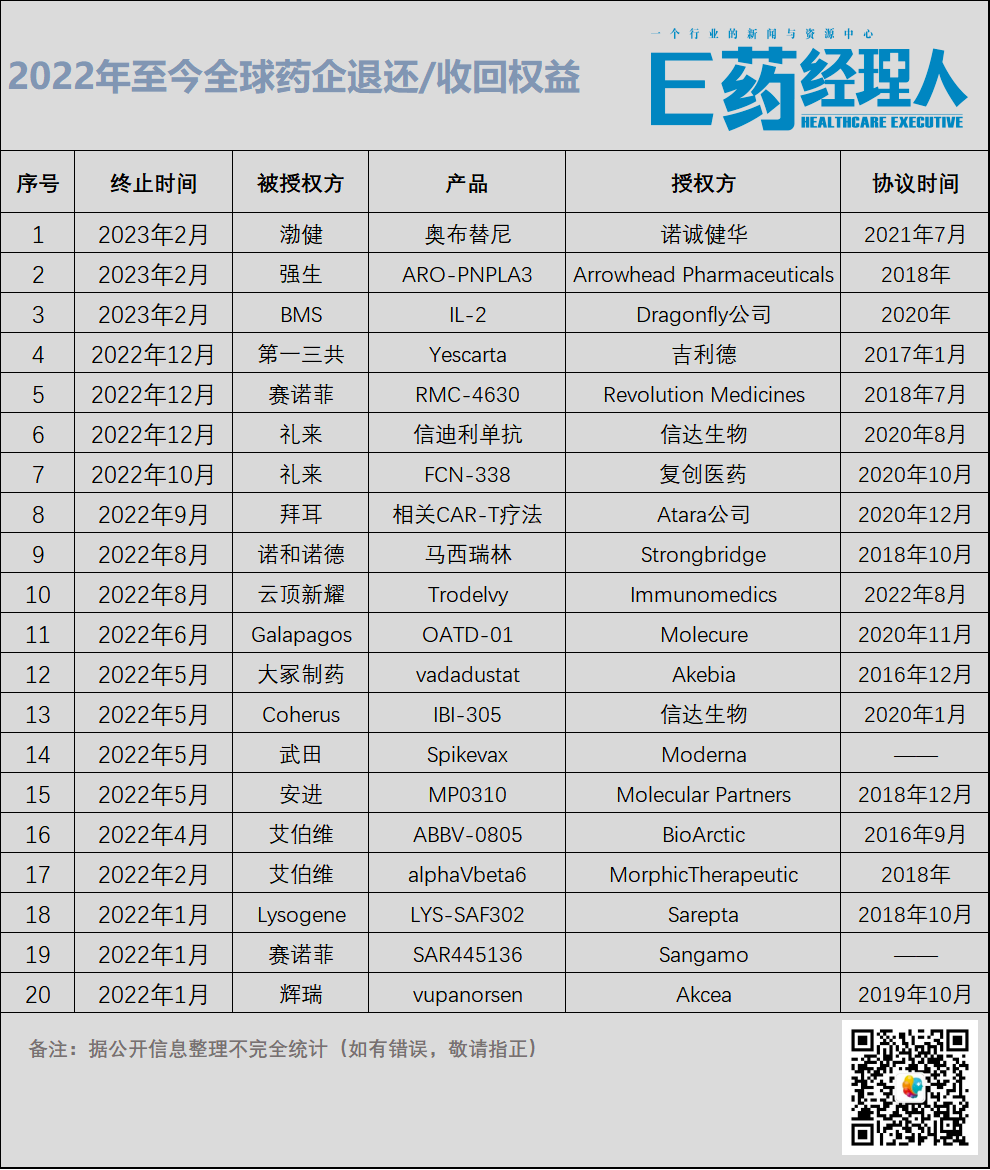
超20起“退货”,原因是什么?
类似“退货”事件并非个例。在诺诚健华BTK抑制剂“被退货”同一天,基于战略研发组合审查后,强生将siRNA药物ARO-PNPLA3全部权利退还给Arrowhead。
“大家也不要反应过度。”有业内人士直言,虽然“退货”事件对于一个公司而言,肯定难免会受到较大影响,但实际这是一个常态性事件,“市场如此反应”,核心问题是对License in/out这个模式不够了解。
一名医药行业BD同样认为,随着近两年BD交易的增多,“退回”事件发生将会频繁起来,这本身就是一个国内国外会非常普遍的现象。
据E药经理人不完全统计,单2022年至今,国内外就发生了超过20起类似产品“退货”事件。涉及对象不单是国内药企与跨国药企或Biotech之间,全球药企之间互相“退货”也比比皆是,有国内药企“退货”跨国药企,如云顶新耀终止与吉利德全资子公司关于ADC药物的协议。
对这20余起“退货”事件分析来看,原因主要可归纳于产品本身临床数据不佳、监管不顺以及授权方和被授权方公司战略调整等因素。
就拿授权产品本身临床或审批不顺,便引发了多起“被退”事件。一方面是授权产品安全性或有效性数据不佳,临床遭遇打击,而遭受“退货”。单2022年,一众药企产品便“败”在安全性问题上,如因受试患者死亡,拜耳退出与Atara 6.7亿美元CAR-T疗法合作协议等;因IIb期研究(TRANSLATE-TIMI 70)数据不佳,辉瑞退出Ionis子公司Akcea反义疗法vupanorsen的全球开发工作,归还vupanorsen的所有权益。
与此同时,“监管审批”也是影响双方合作无法“继续”的一大拦路虎。如国内较为熟悉的案例,在信达生物PD-1“闯关”失利后,双方基于商业决策和未来发展的衡量,礼来终止合作并归还信迪利单抗的所有海外权益。同样,因FDA在CRL中表示已提交的数据显示vadadustat的治疗风险高于治疗收益,大冢制药宣布终止与Akebia合作开发该药相关协议。
“新药研发本来就是九死一生的事情。”上述业内人士表示,过程中会遇到各种难处,“10个有9个大概率不成功,因无法成药只能退回来” 。
排除产品本身原因,授权双方公司战略调整,也成为“退货”事件频发的一大主因。在资本寒冬下,砍管线已成为常态,全球药企均未幸免于难,跨国药企动作频出,仅聚焦潜力较大、回报率高的产品。“MNC管线太多了,授权产品不一定能够排到前列,而最后淘汰一批产品可能觉得价值不高了,或者是跟自身的战略方向不一致,原因太多了。”
一批药企基于管线战略调整,而“退回”了相应产品。有的企业因临床开发的数量和排列的优先级发生变化,聚焦业务发生转移,未来重点发生转移,选择“退货”归还。
举例来看,单赛诺菲2022年退货就不止一单。2022年1月,赛诺菲把镰状细胞病候选药物SAR445136的完全控制权归还给Sangamo,表示将把未来的重点放在同种异体通用基因组医学方法上,而不再是自体个性化细胞疗法。同年12月,对最近的投资组合审查和优先做出排序之后,终止与Revolution公司SHP2抑制剂RMC-4630的开发和商业合作权利。
此外,在战略管线评估后,安进退回Molecular Partners公司旗下4-1BB/FAP激动剂MP0310的全球权益;因管线策略发生调整,礼来终止与复星医药子公司复创医药合作开发Bcl-2抑制剂FCN-338;因战略和投资组合评估,Galapagos终止与Molecure达成的合作协议,不再负责哮喘新药OATD-01的全球开发和商业化工作。
还有的因“授权交易的管线交易进度不尽如人意”而主动收回。2022年5月,信达生物收回了与Coherus公司贝伐珠单抗生物类似药IBI-305美国和加拿大的商业化权益,原因则在于该药在北美市场动态以及受疫情持续影响开发延误。
“相关负责人都走了,旗下产品没办法,只能退。”药企相关主要人事变动亦会促使产品退回概率加大,有的因CEO或产品重要负责人变化,公司整个策略产生大的调整,“这种情况大家自己收回来,反而更好。”
对于授权双方,“收回/退回权益”不见得是一件坏事。“管线要是不受重视,而导致进展较慢,反而被竞争对手超过,失去先机,对于产品才是打击。”
亦有业内人士表示,还有很多当时交易本身就不理性,两三年前大家一窝蜂涌进“License in/out”,有的着眼于增加估值,有的想增加一下现金流,从而导致了很多“不合适的引进”。
对于BD,还需要注意什么呢?
人、价格、产品都是关键点
“一个BD交易能不能做成,我认为关键要看投后管理和承接。交易早期的工作大家其实大差不差,承接和管理才是见功夫的时候。”一位从事多年BD工作的高管苑宁表示。
如前文所述,那些被退回的交易,有相当比例的交易在推进过程中双方出现了分歧,或者是出现了BD团队项目负责人的变动,以及公司发生调整之后项目进展缓慢。
“比如说,重要岗位BD人员的离开,基本都会经历资源被带走,或者需要审批的一个过程,直接或间接的影响了项目的进度。”苑宁表示。
而且,BD的流动率相对研发之类的岗位来说,特别大。“正常情况是两年一换,大家都要凭项目来刷职业履历。真正能够留到自己的项目注册上市,走到最后阶段的BD人非常少。”在一家创新药企长期从事BD的穆颖说道。
她对E药经理人表示,留住BD人才对所有企业来说都很棘手。“因为引进项目之后需要管理,我们经常开完会说‘就像生了孩子需要养,养不好压力是很大的’,所以大家都愿意换平台。”
如果切换到License out角度,其实交易方BD团队除专业性外,稳定性也很重要。有些公司会在BD团队的考核中设置一些激励机制,比如给走到最后阶段的项目一个非常重大的里程碑激励。“一定程度上可以帮助你判断这个公司的文化。”
“价格当然是很重要的因素,以前火热的时候,为了拿到项目,可能价格上会有些冲动,后续拿到了,但最后会出现商业化回报达不到要求,以前还能在资本市场找补,现在可能没有什么机会从资本市场去弥补了。”在MNC从事BD的段风表示,MNC购买权益后因此退单的情况有不少。
在他看来,每家公司所坚守的价值和估值的底线不一样,不要只参考一家公司,把所有同类型交易的公司都看一遍,划出一个区间,来框定资金。“比如说首付款,要和其他竞争公司有可比性;在里程碑的设定上,对一些很关键的里程碑有一些回报指标,比如技术转移、临床节点、药效数据等,这是对比较新的项目。对于me too的项目来讲,可能就更多地会设定接近于上市,甚至会对销售有一些要求。”而对License out方,也可据此来判断对方是否是真正想将你的产品推上市。
此外,还要判断你的产品是否与对方的管线契合,是否是对方的重要管线。苑宁表示,无论是License in还是License out,一定要坚持在熟悉的领域赚自己认知范围,以及自己的资源和相应的竞争优势内的钱。而且在熟悉的领域要争取做的更快,让这个故事能够一直延续下去。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..